三氯化铈
| 三氯化铈[1] | |||
|---|---|---|---|

| |||
| |||
| IUPAC名 Cerium(III) chloride Cerium trichloride | |||
| 别名 | 氯化铈(III) | ||
| 识别 | |||
| CAS号 | 7790-86-5(无水) 16651-27-7(六水) 18618-55-8(七水) | ||
| PubChem | 24636 | ||
| ChemSpider | 23038 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | VYLVYHXQOHJDJL-DFZHHIFOAZ | ||
| ChEBI | 35458 | ||
| 性质 | |||
| 化学式 | CeCl3 | ||
| 外观 | 白色潮解粉末 | ||
| 密度 | 3.97 g/cm3 | ||
| 熔点 | 817 °C (无水物) 90 °C (七水合物分解) | ||
| 沸点 | 1727 °C | ||
| 溶解性(水) | 100 g/100 ml | ||
| 溶解性(其他) | 可溶于乙醇、丙酮 | ||
| 结构 | |||
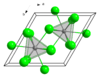
| 晶体结构 | 六方晶系,hP8 | ||
| 空间群 | P63/m, No. 176 | ||
| 危险性 | |||
| 警示术语 | R:R36/37/38 | ||
| 安全术语 | S:S26, S36 | ||
| 欧盟分类 | 刺激性 (Xi) | ||
| 闪点 | 不可燃 | ||
| 致死量或浓度: | |||
LD50(中位剂量)
|
2111 mg/kg (大鼠经口)[2] | ||
| 相关物质 | |||
| 其他阴离子 | 三氟化铈 三溴化铈 三碘化铈 | ||
| 其他阳离子 | 氯化镧 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
三氯化铈,别名氯化铈、氯化铈(III),化学式CeCl3。
性质[编辑]
无色易潮解块状结晶或粉末。露置于潮湿空气中时,迅速吸收水分生成组成不定的水合物。[3]易溶于水,可溶于乙醇和丙酮。[4]
水合物直接在空气中加热时会发生少量水解。[5]若在真空中加热七水合物数小时逐渐至140°C,则可得到无水三氯化铈,根據Encyclopedia of Reagents for Organic Synthesis,在70-100°C時晶體已經可以脫去大量的水,可在此溫度維持一段時間再提升溫度,加熱時並須同時使用攪拌子攪拌晶體,最後所生成產物為粉狀固體,可以儲存於乾燥箱中,使用前需再加熱抽真空除水。[4][6][7]用此法制得的无水三氯化铈可能还含有少量水解产物CeOCl,但已经可与有机锂试剂和格氏试剂共用,用于有机合成。
纯的无水三氯化铈可通过①将水合物在高真空中和4~6倍氯化铵存在下缓慢加热至400°C,[5][8][9][10]或②将水合物与过量氯化亚砜共热3小时而制得。[5][11]此外还可以通过单质铈与氯气化合制备无水三氯化铈。[12][13]它一般通过在高真空下高温升华纯化。
制备[编辑]
将稀土硫酸铵复盐与氢氧化钠反应,转化为氢氧化稀土。再用空气将后者中的铈氧化为四价铈,以稀盐酸浸出使铈富集,再经溶解、萃取、结晶,制得三氯化铈。
用途[编辑]
用作制取铈和其他铈盐的原料、石油催化剂,以及有机合成中的路易斯酸等。三氯化铈可作三氟甲磺酸铈的制取原料,后者是有机合成中的路易斯酸,用于傅-克酰基化反应。三氯化铈自身也是一种路易斯酸,用于傅-克烷基化反应。[14]
七水合三氯化铈与硼氢化钠共用时可作为Luche还原反应[15]中的试剂。该反应是有机合成中将α,β-不饱和酮还原的常用方法之一。例如,香芹酮在三氯化铈和硼氢化钠共同作用下,可以控制只有羰基双键被还原,生成(1),而不产生(2);而无三氯化铈时,产物则为(1)和(2)的混合物。
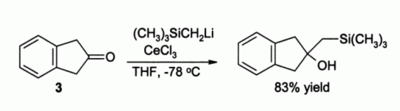
另一例子是用三氯化铈促进的酮的烷化反应。此法避免了使用有机锂试剂时产生的烯醇负离子。[6]
参考资料[编辑]
- ^ Record of Cer(III)-chlorid in the GESTIS Substance Database from the IFA.
- ^ 存档副本 (PDF). [2009-11-27]. (原始内容 (PDF)存档于2007-09-27).
- ^ Alfa 和 Strem 等主要试剂生产商在产品目录上将三氯化铈水合物的化学式标为 CeCl3·xH2O。 Aldrich 则提供七水物。
- ^ 4.0 4.1 Paquette, L. A. Coates, R. M.; Denmark, S. E. (eds.) , 编. Handbook of Reagents for Organic Synthesis: Reagents, Auxiliaries and Catalysts for C-C Bond Formation. New York: Wiley. 1999. ISBN 0471979244.
- ^ 5.0 5.1 5.2 Edelmann, F. T.; Poremba, P. Herrmann, W. A. (ed.) , 编. Synthetic Methods of Organometallic and Inorganic Chemistry VI. Stuttgart: Georg Thieme Verlag. 1997. ISBN 3131030216.
- ^ 6.0 6.1 Johnson, C. R.; Tait, B. D. A cerium(III) modification of the Peterson reaction: methylenation of readily enolizable carbonyl compounds. Journal of Organic Chemistry. 1987, 52 (2): 281–283. ISSN 0022-3263.
- ^ Dimitrov, Vladimir; Kostova, Kalina; Genov, Miroslav. Anhydrous cerium(III) chloride — Effect of the drying process on activity and efficiency. Tetrahedron Letters. 1996, 37 (37): 6787–6790. doi:10.1016/S0040-4039(96)01479-7.
- ^ Taylor, M. D.; Carter, P. C. Preparation of anhydrous lanthanide halides, especially iodides. Journal of Inorganic and Nuclear Chemistry. 1962, 24 (4): 387–391. doi:10.1016/0022-1902(62)80034-7.
- ^ Kutscher, J.; Schneider, A. Inorg. Nucl. Chem. Lett. 1971, 7: 815. 缺少或
|title=为空 (帮助) - ^ Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements. New York: Pergamon Press. 1984. ISBN 0080220568.
- ^ Freeman, J. H.; Smith, M. L. The preparation of anhydrous inorganic chlorides by dehydration with thionyl chloride. Journal of Inorganic and Nuclear Chemistry. 1958, 7 (3): 224–227. doi:10.1016/0022-1902(58)80073-1.
- ^ Druding, L. F.; Corbett, J. D. Journal of the American Chemical Society. 1961, 83: 2462–2467. ISSN 0002-7863. 缺少或
|title=为空 (帮助) - ^ Corbett, J. D. Rev. Chim. Minerale. 1973, 10: 239. 缺少或
|title=为空 (帮助) - ^ Mine, Norioki; Fujiwara, Yuzo;Taniguchi, Hiroshi. Trichlorolanthanoid (LnCl3)-catalyzed Friedel-Crafts alkylation reactions. Chemistry Letters. 1986, 15 (3): 357–360. doi:10.1246/cl.1986.357.
- ^ Luche, Jean-Louis; Rodriguez-Hahn, Lydia; Crabbé, Pierre. Reduction of natural enones in the presence of cerium trichloride. Journal of the Chemical Society, Chemical Communications. 1978: 601–602. doi:10.1039/C39780000601.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||