馬可尼可夫法則
馬可尼可夫法則(英語:Markovnikov's Rule / Markownikoff's Rule),又稱馬氏規則,是有機化學中一個基於柴瑟夫規則的區域選擇性經驗規則,其內容即:當發生親電加成反應(如鹵化氫和烯烴的反應)時,親電試劑中的正電基團(如氫)較傾向加在連氫最多(取代最少)的碳原子上,而負電基團(如鹵素)則會加在連氫最少(取代最多)的碳原子上。[1]這個規則是由俄國化學家馬可尼可夫在1870年提出的。[2][3]
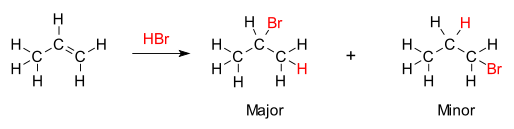
除烯烴、炔烴與水、鹵素、鹵化氫、次鹵酸、酸、醇、酚加成的反應外,烯烴的羥汞化反應、烷氧汞化-去汞反應也是符合馬可尼可夫法則的。
解釋[編輯]
馬可尼可夫法則的原因是親電加成反應中生成了較為穩定的碳正離子。加上一個H+的碳原子會使其他碳原子上引入一個正電荷,形成一個碳正離子。由於誘導效應和超共軛效應,取代基(碳上連接的碳或給電子基團)越多的碳正離子越穩定。而加成反應的主要產物會由一個更加穩定的中間體產生。所以烯烴加溴化氫時,溴化氫中的氫總是加在連氫最多的碳上,而鹵素基團加在連氫最少的碳上。然而,其它比較不穩定的碳正離子仍然存在,通過它們生成的產物是不符合馬可尼可夫法則的,通常是反應的副產物。
這個規則可以概括為「氫多加氫」、「富者愈富,而窮者愈窮」、化學中的馬太效應等等:連氫多的碳會得到另外的氫,而連氫少的碳會得到另外的取代基。對於其他不對稱親電試劑也是如此。正電基團加到取代少的碳上,負電基團加到取代多的碳上。
六十年後的認可[編輯]
馬可尼可夫用於證明其規則的一個反應是碘化氫和溴乙烯的加成。根據他的規則,鹵素原子將會加在已經有一個鹵素的碳上。而這個產物(1-碘-1-溴乙烷)是偕鹵化物水解反應的產物。用潮濕的氧化銀處理這個產物則會得到乙醛,證明了產物的結構。

有人[3]認為,在1869年馬可尼可夫的論文是粗心的,因為他自己沒有做很多實驗。這個規則僅僅作為了一個四頁長的腳註出現在了一篇26頁的文章中。因此他的規則經過了大約60年才被廣泛認可。
反馬可尼可夫法則[編輯]
很多反應的區域選擇性性質都與馬可尼可夫法則所做的預測相悖,這些反應稱為反馬可尼可夫法則的反應(Anti-Markovnikov reactions)。氫加到含氫較少的碳原子上,鹵素等負電基團加成到了含氫較多的碳原子上。
反馬可尼可夫法則的一個例子是吸電子基團取代的烯烴與親電試劑的反應。受誘導效應影響,當烯烴雙鍵碳上連有-CF3等吸電子基時,直接與這些基團相連的碳原子帶有部分負電荷,它所形成的碳正離子是不穩定的。雖然親電加成仍然符合電性規律,但是H+會加到靠近吸電子基的雙鍵碳上,生成反馬可尼可夫法則的產物。
硼氫化-氧化反應也是常見的反馬可尼可夫法則反應之一。這個反應中硼原子是親電性的(δ+),傾向於取代較少的雙鍵碳結合,使該碳原子帶有部分負電荷,將正電荷留給另外一個雙鍵碳,(部分)形成較穩定的碳正離子。

反馬可尼可夫法則的反應也包括不以碳正離子作為中間體的反應,比如烯烴和鹵化氫的自由基加成反應。以HBr為例, 是鏈增長中與烯烴發生加成的試劑,而只有溴加到取代少的碳上時,才能形成較為穩定的自由基。自由基的穩定性與碳正離子類似,取代越多的自由基越穩定。形成的自由基從另一分子HBr奪取氫,反應的總體結果是氫加到了取代較多的碳原子上。
反馬可尼可夫法則的性質也可以發生在炔烴的親電加成反應上。比如苯乙炔和水的反應,在金的催化下,會得到苯乙酮,而在釕配合物的催化下,則會得到異構體苯乙醛[4]:

由於碳正離子會發生重排,故重排後生成的產物也往往不符合馬可尼可夫法則。下圖中單一構型的1在四氯化鈦催化下重排,會生成外消旋體2a和2b。 [5]

這些產物可以被解釋為:1中羥基離去生成了一個三級碳正離子A,而這個三級碳正離子會重排成二級碳正離子B。氯可以從兩邊進攻這個碳正離子,從而得到兩種差向異構體。
參考資料[編輯]
- ^ Additions to Alkenes: Regiochemistry. [2009-03-08]. (原始內容存檔於2020-02-19).
- ^ W. Markownikoff. Ueber die Abhängigkeit der verschiedenen Vertretbarkeit des Radicalwasserstoffs in den isomeren Buttersäuren. Annalen der Pharmacie. 1870, 153 (1): 228–259. doi:10.1002/jlac.18701530204.
- ^ 3.0 3.1 Was Markovnikov’s Rule an Inspired Guess? Peter Hughes 1152 Journal of Chemical Education · Vol. 83 No. 8 August 2006
- ^ Highly Active in Situ Catalysts for Anti-Markovnikov Hydration of Terminal Alkynes. Aurélie Labonne, Thomas Kribber, and Lukas Hintermann Org. Lett.; 2006; 8(25) pp 5853 - 5856; (Letter) doi:10.1021/ol062455k
- ^ TiCl4 Induced Anti-Markovnikov Rearrangement Mugio Nishizawa, Yumiko Asai, and Hiroshi Imagawa Org. Lett.; 2006; 8(25) pp 5793 - 5796; (Letter) doi:10.1021/ol062337x.



