硼氢化-氧化反应
在有机化学中,硼氢化-氧化反应是烯烃与硼烷加成,再被氧化生成醇的两步有机化学反应。[1][2][3] 氢和羟基通过顺式加成生成顺式产物。硼氢化-氧化反应是一个反马氏反应,羟基加成到取代基较少的碳上。在有机合成中,这是一个常用的反应。
反应一般按如下形式进行:

该反应常用四氢呋喃(THF)作为溶剂,有时也用其他的极性非质子溶剂。它分为两步:在第一步中,甲硼烷(BH3)与双键加成生成烷基硼,称为烯烃的硼氢化反应。第二步中,烷基硼在碱性条件下与过氧化氢作用生成醇,BH2基团被氧化为羟基,这一步称为烷基硼的氧化反应。
硼氢化反应[编辑]
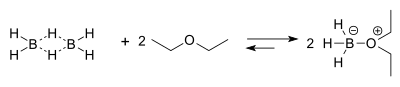
反应中使用的硼烷为乙硼烷(B2H6),常温下以有毒无色气体形式存在。在乙硼烷中,有两个氢原子各以一对电子与两个硼原子成BHB氢桥键(三中心两电子键)。电子的离域使硼原子达到八隅体结构,同时降低了硼的亲电性。由于含有空余的p轨道,乙硼烷是一个强的路易斯酸。由于迅速的二聚反应,并不存在单独的BH3分子。然而,当乙硼烷溶于醚或胺中时,可以形成稳定的配合物,其中氧原子或氮原子作为路易斯碱提供孤对电子与硼形成配位键。这些物质的性质与硼烷相同。BH3的四氢呋喃或乙醚溶液通常比乙硼烷气体使用更方便,因此在实验室中较为常见。
硼烷与烯烃的加成是一个协同反应,双键的断裂与新键的生成同时进行。过渡态理论可以更清楚地显示反应的历程:
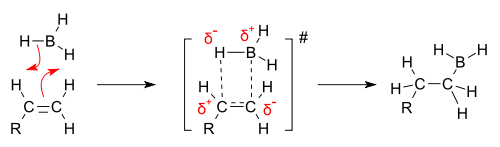
由于该含硼基团将被羟基取代,所以第一步是立体决定的一步。硼将加成在与较少取代基相连的碳上。在过渡态中,多取代的碳上带有少量正电荷,类似碳正离子。一般而言,多取代的碳上带正电荷比少取代的碳稳定。如果硼烷进攻另一个多取代的碳,将是少取代的碳带上正电荷,不利于稳定。但有时在空间位阻的影响下,硼烷也会加成到少取代的碳上。
硼烷将继续进行类似的反应直到所有的三个氢原子被烃基所取代,即一分子硼烷可与三分子烯烃进行反应。所以有时使用只有一个氢原子的硼烷(R2BH)进行反应,例如一种被广泛用于硼氢化反应的硼氢化试剂9-BBN,它与烯烃反应有选择性,可以只进攻位阻较小的双键。
硼烷一般与烯烃进行顺式加成,即加到双键的同一边。例如甲基环戊烯与硼烷生成反式产物。 [4]
氧化反应[编辑]
在第二步氧化反应中,过氧根离子进攻硼原子。烷基迁移到氧原子上生成构象保持的产物。

炔烃也可进行硼氢化-氧化反应,产物是醛或酮。为使反应停留在与一个硼烷加成的一步,通常使用带有较大取代基的硼烷,如二(二仲异戊基)硼烷。[5]在第二步如果与氯胺反应可得到胺。[6]与溴和碘反应可得到相应的卤代烷。使用甲酸可以得到烷烃。
参见[编辑]
参考资料[编辑]
- ^ Loudon, Marc G. Addition Reactions of Alkenes.. Organic Chemistry Fourth Edition. New York: Oxford University Press. 2002: 168–172. ISBN 0-19-511999-1.
- ^ Organic Chemistry Help. Hydroboration of alkenes. http://www.chemhelper.com/hydroboration.html (页面存档备份,存于互联网档案馆)
- ^ Organic Chemistry Portal. Hydroboration (including recent literature). https://www.organic-chemistry.org/namedreactions/brown-hydroboration.shtm (页面存档备份,存于互联网档案馆)
- ^ Hydroboration. IX. The Hydroboration of Cyclic and Bicyclic Olefins-Stereochemistry of the Hydroboration Reaction Herbert C. Brown, George Zweifel; J. Am. Chem. Soc.; 1961; 83(11); 2544-2551. doi:10.1021/ja01472a027
- ^ Catecholborane (1,3,2-benzodioxaorole) as a new, general monohydroboration reagent for alkynes. Convenient synthesis of alkeneboronic esters and acids from alkynes via hydroboration Herbert C. Brown, S. K. Gupta; J. Am. Chem. Soc.; 1972; 94(12); 4370-4371. doi:10.1021/ja00767a072
- ^ The Reaction of Organoboranes with Chloramine and with Hydroxylamine-O-sulfonic Acid. A Convenient Synthesis of Amines from Olefins via Hydroboration Herbert C. Brown, Wolfgang R. Heydkamp, Eli Breuer, and William S. Murphy J. Am. Chem. Soc.; 1964; 86(17) pp 3565 - 3566; doi:10.1021/ja01071a036
