乙醚
| 乙醚 | |
|---|---|

| |

| |
| IUPAC名 Ethoxyethane 乙醚 | |
| 別名 | 二乙基醚,乙氧基乙烷,二乙醚 |
| 識別 | |
| CAS編號 | 60-29-7 |
| SMILES |
|
| Beilstein | 1696894 |
| Gmelin | 25444 |
| UN編號 | 1155 |
| EINECS | 200-467-2 |
| ChEBI | 35702 |
| 性質 | |
| 化學式 | C4H10O |
| 莫耳質量 | 74.12 g·mol−1 |
| 外觀 | 無色液體 |
| 氣味 | 刺激性氣體,帶甜味 |
| 密度 | 0.7134 g/cm3(液體) |
| 熔點 | −116.3 ℃(156.9 K, −177.3 ℉) |
| 沸點 | 34.6 ℃(307.8 K, 94.3 ℉) |
| 溶解性(水) | 6.05 g/100 mL (20℃)[1] |
| 蒸氣壓 | 440 mmHg (58.66 kPa,20 °C )[2] |
| 折光度n D |
1.353 (20 ℃) |
| 黏度 | 0.224 cP(25℃) |
| 結構 | |
| 偶極矩 | 1.15 D(氣體) |
| 熱力學 | |
| ΔfHm⦵298K | (−271.2±1.9) kJ/mol |
| ΔcHm⦵ | (−2732.1±1.9) kJ/mol |
| S⦵298K | 253.5 J/(mol·K) |
| 熱容 | 172.5 J/(mol·K) |
| 危險性 | |
| 警示術語 | R:R12 R19 R20/22 R66 R67 |
| 安全術語 | S:S9 S16 S29 S33 |
| MSDS | External MSDS |
GHS危險性符號 
| |
| GHS提示詞 | 危險 |
| H-術語 | H224, H302, H336 |
| P-術語 | P210, P233, P240, P241, P242, P243, P261, P264, P270, P271, P280, P301+312, P303+361+353, P304+340 |
| 主要危害 | 極度易燃,對皮膚有害,在空氣和光線作用下分解為易爆的過氧化物[2] |
| NFPA 704 | |
| 閃點 | −45℃[3] |
| 自燃溫度 | 160℃[3] |
| 爆炸極限 | 1.9-48.0% [4] |
| 相關物質 | |
| 相關醚類 | 甲醚 甲乙醚 |
| 相關化學品 | 二乙硫醚 丁醇異構體 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
乙醚(英語:Ether,也稱依打)是一種醚類有機化合物,結構簡式為(可簡寫為[註 1])。乙醚是一種無色易燃、極易揮發的液體,遇火花、靜電、高溫、氧化劑(如過氯酸、氯氣、氧氣、臭氧等)時,有燃燒爆炸的危險;其氣味刺激,帶有甜味,曾被用作吸入性全身麻醉劑,也是常見的毒品加工原料。乙醚亦是一種實驗室常用的微極性有機溶劑,與空氣隔絕時相當穩定,長期儲存時與氧氣接觸會逐漸形成易爆的氫過氧化乙醚混合物[註 2]。乙醚稍溶於水,易溶於乙醇、苯、氯仿、石油醚。
歷史[編輯]
傳說乙醚可能是由公元8世紀的賈比爾[5]或拉蒙·柳利在1275年合成的[5][6]。1540年,文藝復興時期的醫生瓦勒留斯·科爾杜斯首次具體描述了乙醚的合成方法,他將乙醚稱為甜礬油(oleum dulce vitrioli)[註 3],科爾杜斯透過蒸餾乙醇和礬油[註 4]製備乙醚,並簡單介紹了這種物質的藥用性質[5]。大約在同一時期,帕拉塞爾蘇斯在狗身上發現了這種物質可用作鎮痛劑[5]。1729年,奧古斯特·西格蒙德·弗羅貝尼烏斯將這種物質命名為乙醚(ether)[7]。人們曾經認為乙醚是某種硫化合物,直至約19世紀才被證明是錯誤的[8]。
製備[編輯]
實驗室中,在濃硫酸作用下於140℃加熱,可由乙醇經分子間失水製得乙醚[9]:
該反應中醇在酸性條件下質子化形成𨦡鹽(a),接著與醇中的氧原子發生親核取代,同時質子化的羥基以水的形式離去,然後再去質子化得到醚。
CH3CH2OH + H+ CH3CH2H2 (a)
CH3CH2H2 + HOCH2CH3 (CH3CH2)2H (CH3CH2)2O
此反應需要嚴格控制反應溫度,並不斷添加乙醇,如果反應溫度達到170℃,則反應的產物會以乙烯為主。
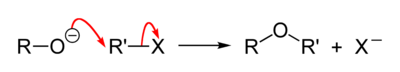
另一種製備醚的方法是Williamson醚合成,反應是鹼金屬醇鹽和鹵烷在無水條件下的親核取代反應[10]:
除硫酸外,磷酸、對甲苯磺酸、氧化鋁、氯化鋅、三氟化硼等酸性催化劑都能用於醇分子間失水反應[11]。大部分乙醚是乙烯氣相水合製備乙醇時的副產物,該工藝使用固相磷酸催化劑催化[12]。工業上,常用γ-氧化鋁作為催化劑,在300℃下脫水生成乙醚,此法可以用於製備一些高級醚[13]:
用途[編輯]
- 可用作生產纖維素塑膠如醋酯纖維的溶劑。[12]
- 乙醚的十六烷值高,因其揮發性強、閃點低而可與石油餾分組合為發動機啟動液。
- 可用作蠟、脂肪、油、香料、生物鹼、軟膠等的溶劑。
- 乙醚在水中的溶解度小,可作液-液萃取的溶劑;可以用於提取青蒿素。[14]
- 乙醚曾作為吸入麻醉藥使用(使用前必須以碘化鉀醋酸溶液驗純,以確定無過氧化物),但因恢復期長且不良反應多,現今更傾向使用氟代醚麻醉藥如地氟醚和七氟醚。[15]
- 曾有說法稱有不法分子使用浸有乙醚的毛巾捂人口鼻,迅速使被害人昏迷後偷搶財物,後經指出這是虛假的傳言,理由是吸入乙醚蒸汽使人昏迷所用的時間太長,且易使被害者有生命危險。[16]
- 乙醚曾被用作娛樂性藥物,在19世紀30年代的美國曾舉行過被稱為「乙醚狂歡」的公共娛樂活動,人們吸食乙醚或笑氣以達到亢奮狀態[17]。20世紀初的波蘭農民流行在飲料中添加數滴(kropki)乙醚,蘭科人會將它倒入牛奶、甜水或橙汁中,裝在烈酒杯中飲用[18]。
安全性[編輯]
乙醚極易燃,久置又能形成易爆的混合物。乙醚蒸汽會與空氣形成易燃的混合物,即使不是明火,也可能被加熱板、電弧、蒸汽管道所點燃[19]。
乙醚對光和空氣敏感,傾向於以過氧化物的形式存在,可以形成具有爆炸性的過氧乙醚[19]。過氧乙醚沸點更高,並且在乾燥的時候可能發生爆炸。市售乙醚中會加入微量的抗氧化劑2,6-二三級丁基對甲酚(BHT);與氫氧化鈉一同儲存會沉澱出氫過氧化醚。乙醚中的水和過氧化物可使用鈉和二苯甲酮蒸餾,或是透過活性氧化鋁柱去除。[20]
備註[編輯]
參考書籍[編輯]
- 邢其毅等. 《基础有机化学》第四版 上册. 北京大學出版社. 2017a (中文(中國大陸)).
- 邢其毅等. 《基础有机化学》第四版 下册. 北京大學出版社. 2017b (中文(中國大陸)).
參考文獻[編輯]
- ^ Merck Index, 10th Edition, Martha Windholz, editor, Merck & Co., Inc, Rahway, NJ, 1983, page 551
- ^ 2.0 2.1 NIOSH Pocket Guide to Chemical Hazards. #0277. NIOSH.
- ^ 3.0 3.1 Ethyl Ether MSDS. J.T. Baker. [2010-06-24]. (原始內容存檔於2012-03-28).
- ^ Carl L. Yaws, Chemical Properties Handbook, McGraw-Hill, New York, 1999, page 567
- ^ 5.0 5.1 5.2 5.3 Toski, Judith A; Bacon, Douglas R; Calverley, Rod K. The history of Anesthesiology. In: Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K. Clinical Anesthesia 4 (Lippincott Williams & Wilkins). 2001: 3. ISBN 978-0-7817-2268-1.
- ^ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. McGraw-Hill's PCAT. McGraw-Hill. 2008-11-12: 39 [2011-05-25]. ISBN 978-0-07-160045-3.
- ^ VIII. An account of a spiritus vini æthereus, together with several experiments tried therewith. Philosophical Transactions of the Royal Society of London. 1730, 36 (413): 283–289. S2CID 186207852. doi:10.1098/rstl.1729.0045.
- ^
 Chisholm, Hugh (編). Ether. Encyclopædia Britannica 9 (第11版). London: Cambridge University Press: 806. 1911.
Chisholm, Hugh (編). Ether. Encyclopædia Britannica 9 (第11版). London: Cambridge University Press: 806. 1911.
- ^ Cohen, Julius Berend. A Class-book of Organic Chemistry, Volume 1. London: Macmillan and Co. 1920: 39.
the structure of ethyl alcohol cohen julius diethyl ether.
- ^ 邢其毅等 2017a,第319頁.
- ^ 邢其毅等 2017a,第322頁.
- ^ 12.0 12.1 Ethers, by Lawrence Karas and W. J. Piel. Kirk‑Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. 2004.
- ^ Ethyl Ether, Chem. Economics Handbook. Menlo Park, Calif: SRI International. 1991.
- ^ 胡淼; 錢國平; 蘇寶根; 鮑宗必; 任其龍. 硅胶柱层析纯化青蒿素. 華西藥學雜誌. 2005, (04): 283–285. doi:10.13375/j.cnki.wcjps.2005.04.001 (中文(中國大陸)).
- ^ Hill, John W. and Kolb, Doris K. Chemistry for Changing Times: 10th Edition. p. 257. Pearson: Prentice Hall. Upper Saddle River, New Jersey. 2004.
- ^ 楊思瑞. 女大生校園遭化學物襲擊 同班男同學落網. 中央通訊社. 2016-11-28 [2023-08-04]. (原始內容存檔於2023-08-04) (中文(臺灣)).
- ^ Desai SP, Desai MS, Pandav CS. The discovery of modern anaesthesia-contributions of Davy, Clarke, Long, Wells and Morton. Indian Journal of Anaesthesia. 2007, 51 (6): 472–8 [2010-09-18]. ISSN 0019-5049. (原始內容存檔於2020-08-04).
- ^ Kaszycki, Nestor. Łemkowska Watra w Żdyni 2006 – pilnowanie ognia pamięci. Histmag.org – historia od podszewki. Kraków, Poland: i-Press. 2006-08-30 [2009-11-25]. (原始內容存檔於2021-04-30) (波蘭語).
Dawniej eteru używało się w lecznictwie do narkozy, ponieważ ma właściwości halucynogenne, a już kilka kropel inhalacji wystarczyło do silnego znieczulenia pacjenta. Jednak eter, jak każda ciecz, może teoretycznie być napojem. Łemkowie tę teorię praktykują. Mimo to, nazywanie skroplonego eteru – "kropki" – ich "napojem narodowym" byłoby przesadą. Chociaż stanowi to pewną część mitu "bycia Łemkiem".
- ^ 19.0 19.1 Archived copy (PDF). [2014-02-15]. (原始內容 (PDF)存檔於2014-11-13).
- ^ W. L. F. Armarego; C. L. L. Chai. Purification of laboratory chemicals. Boston: Butterworth-Heinemann. 2003. ISBN 978-0-7506-7571-0.
外部連結[編輯]
| 維基共享資源上的相關多媒體資源:乙醚 |
- Michael Faraday's announcement of ether as an anesthetic in 1818(頁面存檔備份,存於網際網路檔案館)
- Calculation of vapor pressure(頁面存檔備份,存於網際網路檔案館), liquid density(頁面存檔備份,存於網際網路檔案館), dynamic liquid viscosity(頁面存檔備份,存於網際網路檔案館), surface tension(頁面存檔備份,存於網際網路檔案館) of diethyl ether, ddbonline.ddbst.de
- CDC – NIOSH Pocket Guide to Chemical Hazards(頁面存檔備份,存於網際網路檔案館)
| |||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|




![{\displaystyle {\ce {2EtOH ->[{H2SO4}][{140℃}] Et2O + H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/acde29f1452b32a6723fdf77fac7a60369282a6b)

![{\displaystyle {\ce {2EtOH ->[{Al2O3}][{300℃}] Et2O + H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/498e1d05de712db2c3db3ce2f58a4c20f3a46089)