氧化鋁
| 此條目體裁或許更宜作散文而非列表。 (2023年2月6日) |
| 氧化鋁 | |
|---|---|
| |

| |
| 識別 | |
| CAS號 | 1344-28-1 |
| PubChem | 9989226 |
| ChemSpider | 8164808 |
| SMILES |
|
| InChI |
|
| InChIKey | PNEYBMLMFCGWSK-UHFFFAOYAC |
| RTECS | BD120000 |
| 性質 | |
| 化學式 | Al2O3 |
| 摩爾質量 | 101.96 g·mol⁻¹ |
| 外觀 | 白色固體 |
| 密度 | 3.97 g/cm3 |
| 熔點 | 2054 °C |
| 沸點 | 2980 °C [1] |
| 溶解性(水) | 難溶 |
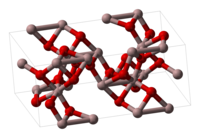
| 結構 | |
| 晶體結構 | 三方 |
| 配位幾何 | 八面體 |
| 熱力學 | |
| ΔfHm⦵298K | −1675.7 kJ mol−1 |
| S⦵298K | 50.92 J mol−1 K−1 |
| 危險性 | |
| 閃點 | 不可燃 |
| 相關物質 | |
| 其他陰離子 | 硫化鋁 硒化鋁 碲化鋁 |
| 其他陽離子 | 氧化硼 氧化鎵 氧化銦 氧化鉈 |
| 相關化學品 | 一氧化二鋁 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氧化鋁(Aluminium oxide)是白色固體,是鋁和氧的化合物,分子式為Al2O3。在礦業、製陶業和材料科學上又稱為礬土。常見純度為99.5%和96%。
1961年,通用電氣(GE)生產出了「Lucalox」,一種用於鈉燈中的透明礬土。
特性[編輯]
- 氧化鋁是一種白色固體,在礦業、製陶業和材料科學上又被稱為礬土。
- 氧化鋁在地球上的蘊藏量只僅次於氧化矽,是一種屬於陶瓷原料之一,在氧化物中鋁與氧有強力的鍵結,使得氧化鋁在氧化物當中有最高硬度,其化學穩定性高且對大部份酸性、鹼性、鹽類及熔融溶液有優秀的耐腐蝕性。
- 氧化鋁有許多同質異晶體,目前已知的有10多種,主要有3種晶型,即α-Al2O3、β-Al2O3、γ-Al2O3。其中結構不同性質也不同,在1300℃以上的高溫時幾乎完全轉化為α-Al2O3。
- 自然界中的剛玉是α形屬於六方最密堆積,熔點、硬度高,不溶於酸鹼耐腐蝕,絕緣性好。
製備[編輯]
在鋁礦的主成份鐵鋁氧石中,氧化鋁的含量最高。工業上,鐵鋁氧石經由拜耳法純化為氧化鋁:
- 加熱用氫氧化鈉溶解礦石。氧化鐵不溶,二氧化矽溶解為矽酸根(Si(OH)62−),氧化鋁溶解為鋁酸根()。
- 過濾,加酸處理,氫氧化鋁沉澱出來,再過濾。
- 強熱氫氧化鋁,可得無定形之白色氧化鋁粉末。
再由霍爾-埃羅法轉變為鋁金屬。
用途[編輯]
- 紅寶石、藍寶石的主成份皆為氧化鋁,因為其他雜質而呈現不同的色澤。紅寶石含有氧化鉻而呈紅色,藍寶石則含有氧化鐵及二氧化鈦而呈藍色。
- 氧化鋁是金屬鋁在空氣中不易被腐蝕的原因。純淨的金屬鋁極易與空氣中的氧氣反應,生成一層薄的氧化鋁薄膜覆蓋在暴露於空氣中鋁表面。這層氧化鋁薄膜能防止鋁被繼續氧化。這層氧化物薄膜的厚度和性質都能通過一種稱為陽極處理(陽極防腐)的處理過程得到加強。
- 鋁為電和熱的良導體,而氧化鋁則是電與熱的絕緣體。氧化鋁的晶體形態剛玉因為硬度高,適合用作研磨材料及切割工具
- 氧化鋁的晶體也可作為磊晶用的基材。
- 氧化鋁粉末常用作色層分析的媒介物。
- 2004年8月,在美國3M公司任職的科學家開發出以鋁及稀土元素化合成的合金製造出稱為transparent alumina的強化玻璃。
- 可以用於高速鐵路列車的緊急剎車裝置(向路軌噴灑氧化鋁粉末以增加鐵軌摩擦力)
- 多孔高表面積比的氧化鋁稱為活性氧化鋁,常用作催化劑、吸附劑、脫水劑和催化劑載體。典型的用途是作為克勞斯化學反應的催化劑。
- 耐火磚的主要成分
參考資料[編輯]
- ^ Mallinckrodt Baker, MSDS. Aluminum Oxide: Material Safety Data Sheet (A28440). [2008-03-06]. (原始內容存檔於2011-08-21).
外部連結[編輯]
- PhysicsWeb article on Transparent alumina (頁面存檔備份,存於互聯網檔案館)
- 氧化鋁字典-Guidechem.com (頁面存檔備份,存於互聯網檔案館)
- 白色氧化鋁 (頁面存檔備份,存於互聯網檔案館)
| ||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||


![{\displaystyle {\rm {Al_{2}O_{3}+3H_{2}O+2NaOH\longrightarrow 2Na[Al(OH)_{4}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/07ca41b56b6da8c712ab6a49d4731418bf02a0a6)
