三氟過氧乙酸
| 三氟過氧乙酸 | |
|---|---|

| |
| IUPAC名 trifluoroethaneperoxoic acid | |
| 別名 | 三氟過乙酸 TFPAA |
| 識別 | |
| CAS編號 | 359-48-8 |
| PubChem | 10290812 |
| ChemSpider | 8466281 |
| SMILES |
|
| InChI |
|
| InChIKey | XYPISWUKQGWYGX-UHFFFAOYAW |
| 性質 | |
| 化學式 | CF3CO3H |
| 莫耳質量 | 130.023 g·mol⁻¹ |
| 外觀 | 無色液體 |
| 沸點 | 162 °C(435 K) |
| 溶解性(水) | 反應 |
| 溶解性 | 可溶於乙腈、二氯甲烷、乙醚和環丁碸 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
三氟過氧乙酸,簡稱三氟過乙酸或TFPAA,是三氟乙酸對應的過酸,化學式 CF3COOOH。它有強氧化性,可用於酮的拜耳-維立格氧化反應。[1]它可將胺基氧化為硝基,產率較高。[2]它是有機過氧酸中反應性最高的,能夠將相對不活潑的烯烴氧化成環氧化物,而其他過氧酸則不能。[3]三氟過氧乙酸能氧化某些官能基中的氧族元素,例如把硒醚氧化成硒酮。[4]三氟過氧乙酸具有潛在爆炸性,[5]所以不能商購,但可以快速製備。[6]它作為實驗室試劑的用途是由威廉·埃蒙斯開創和開發的。[7][8]
性質[編輯]
在標準情況下,三氟過氧乙酸是沸點 162 °C的無色液體。[9]它可溶於乙腈、二氯甲烷、乙醚和環丁碸,會和水反應。[6]和其它過氧酸一樣,三氟過氧乙酸有潛在的爆炸性,需要小心處理。[5]三氟過氧乙酸不可商購,但可以在實驗室中合成,在-20 ℃下可以儲放幾個星期。[6]一些製備方法會產生有殘留過氧化氫和三氟乙酸的三氟過氧乙酸,加熱這種混合物極其危險,所以在加熱前會使用二氧化錳來使過氧化氫發生分解反應以確保安全。[6][9]
製備[編輯]
三氟過氧乙酸可以由三氟乙酸酐和90%濃過氧化氫[3]水溶液反應而成:
- CF
3COOCOCF
3 + H
2O
2 → CF
3COOOH + CF
3COOH
由於三氟乙酸酐和水反應會產生三氟乙酸,加入過量的三氟乙酸酐可以去除過氧化氫的水溶劑:[10]
- CF
3COOCOCF
3 + H
2O → 2 CF
3COOH
較稀的30%過氧化氫溶液和三氟乙酸反應,也可以合成三氟過氧乙酸。[3]
- CF
3COOH + H
2O
2 → CF
3COOOH + H
2O
尿素-過氧化氫加合物和三氟乙酸酐的反應也可以得到三氟過氧乙酸,可以避免處理純過氧化氫或高濃度過氧化氫溶液的危害。[6]這個製備方法不涉及水,所以產生的三氟過氧乙酸完全無水。[11]這是該反應的優勢,因為水在某些氧化反應中會導致副反應。[12]
- CF
3COOCOCF
3 + H
2O
2·CO(NH
2)
2 → CF
3COOOH + CF
3COOH + CO(NH
2)
2
三氟乙酸酐和過碳酸鈉 2Na
2CO
3·3H
2O
2反應,也可以產生三氟過氧乙酸。[6][13]如果合成需要緩衝溶液並且可以容忍水的存在,就可以使用這種方法。
- 3 CF
3COOCOCF
3 + 4 Na
2CO
3·3⁄2H
2O
2 → 6 CF
3COOOH + 4 Na
2CO
3 + 3 H
2O
三氟過氧乙酸也可以通過原位法合成,[14]使它能與目標底物迅速反應,而不是預先合成試劑供以後使用。
用處[編輯]

6H
5I(OOCCF
3)
2
三氟過氧乙酸主要用作氧化劑。[6][8]1953年9月,《美國化學會志》發表了威廉·埃蒙斯和阿瑟·費里斯的報告,稱這種in situ生成的試劑能夠將苯胺氧化成硝基苯。[14]在接下來的兩年中,埃蒙斯報告了該試劑的製備方法,並在該雜誌上發表了六篇關於其應用的手稿。[15][16][17]埃蒙斯被人們銘記為三氟過氧乙酸作為實驗室試劑的先驅[7]和開發者[8],此後三氟過氧乙酸已成為許多不同類型合成反應的有用試劑。
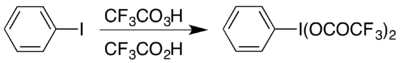
三氟過氧乙酸可以合成超價碘化合物二(三氟乙酸)碘苯 (CF
3COO)
2IC
6H
5,後者可在酸性條件下引起霍夫曼降解反應。[18]這種超價分子可以通過兩種方法製備,一種方法是從二(乙酸)碘苯製備,[19]另一種方法則是碘苯和三氟過氧乙酸和三氟乙酸的混合物反應:[18]
拜耳-維立格氧化反應[編輯]

由於其相對於類似的過氧酸和過氧化物的高酸性,三氟過氧乙酸是拜耳-維立格氧化反應中最強的試劑之一。[20]:17這個反應以於1899年報告此反應的阿道夫·馮·拜爾和維克多·維立格命名,可以把酮氧化成酯或內酯。[1]該反應被認為是通過克里格中間體進行的,[6]並且顯示出對氧原子插入位置的良好區域選擇性和化學選擇性,以及在相鄰位置保留立體化學結構。為了防止強酸性的三氟乙酸副產物造成酯產物的水解[21]和酯交換反應[22],會加入緩衝物質磷酸一氫鈉 Na
2HPO
4。[3]

環氧化[編輯]
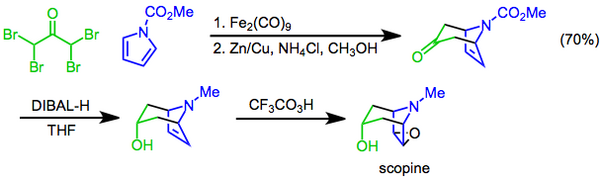
Prilezhaev反應是用過氧酸把烯烴氧化成環氧化物的反應,[23]該反應於1909年首次報告。[24]這個反應是合成莨菪烷類生物鹼莨菪品鹼的最後一步。在這種方法中,由九羰基二鐵介導的[4+3] 環加成反應用於構建雙環骨架,然後用二異丁基氫化鋁非對映選擇性還原酮來引入羥基官能基,最後用三氟過氧乙酸的Prilezhaev反應環氧化,完成莨菪品鹼的合成。[25]
三氟過氧乙酸相對於其它過氧酸的高反應性使得它可以氧化相對缺電子的烯烴(如1-己烯)和α,β-不飽和酯(如丙烯酸甲酯),這些化合物通常可以抵禦過氧酸的環氧化。[3]如果在三氟過氧乙酸中加入三氟乙酸,氧化產物就會是鄰位的羥基-三氟乙酸基結構,而不是環氧化物。這個結構經過酸性甲醇處理後會轉化成二醇,見下圖用1-十二烯合成1,2-十二烷二醇的例子:[3]

對於具有鄰近羰基官能基的烯丙醇化合物,三氟過氧乙酸產生的環氧化物可發生擴環反應,形成1,3-二氧五環的結構。[6][12]這個過程用於天然產物neosporol的全合成中:[12][26]

它的異構物sporol的合成涉及了類似的1,3-二氧五環形成過程。對於這種情況,從過氧化氫合成的三氟過氧乙酸可能含有微量的水,所以氧化產物會是半縮醛,而不是1,3-二氧五環。因此,反應使用的三氟過氧乙酸需要是從尿素-過氧化氫加合物開始合成的無水物,這樣才能使1,3-二氧五環成為主要產物。[12]1,3-二氧五環在之後會擴環成sporol中的1,3-二氧六環結構。[26]
雜原子的氧化[編輯]
三氟過氧乙酸可以氧化含有低氧化態雜原子的官能基。[6][8]常見的情況包括碘的氧化(例如前面提到用碘苯來合成超價碘化合物)、氮、硫和硒。
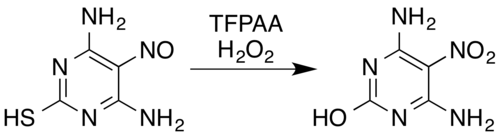
三氟過氧乙酸能把肟[6]和芳香一級胺[16]氧化成硝基化合物[8](在有吸電子基的情況下也會被氧化。舉個例子,五氟苯胺會被氧化成五氟硝基苯[27])、把亞硝胺氧化成硝胺[8][15]以及把亞硝基化合物氧化成硝基化合物或硝胺。[6]舉個例子,過氧化氫和三氟過氧乙酸的混合物會把含有亞硝基的4,6-二胺基-5-亞硝基嘧啶-2-硫醇氧化成它的硝基類似物,並把巰基替換成羥基:[6][28]
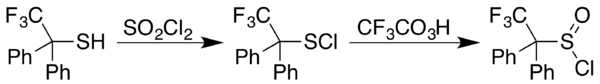
三氟過氧乙酸也能氧化氧族元素化合物。視反應條件,三氟過氧乙酸氧化硫醇(R–S–R)的產物會是亞碸(R–S(O)–R)和/或碸(R–S(O)2–R)。[6]類似的硒化合物硒醚(R–Se–R)的氧化只會產生硒代碸(R–Se(O)2–R)而不產生可分離的硒代亞碸(R–Se(O)–R)。[4]當R是芳基時,此反應特別有效。[29]合成亞磺醯氯(RS(O)Cl)的方法是先將對應的硫醇和磺醯氯(SO
2Cl
2)反應,產生硫基氯(RSCl)。之後用三氟過氧乙酸氧化,得到亞磺醯氯,例如下圖2,2,2-三氟-1,1-二苯基乙硫醇的反應:[30]
三氟過氧乙酸對噻吩的氧化有兩種競爭途徑,分別為S-氧化和環氧化。[31][Note 1]氧化的主要反應是產生亞碸,但這種亞碸會在進一步氧化之前迅速發生類似狄爾斯–阿爾德反應的二聚。反應產物中沒有找到任何S-氧化噻吩或S,S-二氧化噻吩。[6][31]這個二聚體可以繼續氧化,使其中一個S-氧化物部分轉化成S,S-二氧化物。三氟過氧乙酸對噻吩的氧化還可能發生Prilezhaev環氧化反應,[23]產物是迅速重排成異構物噻吩-2-酮的噻吩-2,3-環氧化物。[31]化學捕捉實驗[35]證明環氧化途徑不是S-氧化物中間體的副反應,而同位素標記實驗證明該環氧化物發生了1,2-負氫遷移(NIH重排反應),涉及陽離子中間體。[31]這個反應中三氟過氧乙酸的製備方法很重要,因為製備過程產生的水會抑制環氧化反應,可能是因為它充當了競爭鹼。[31]

重排氧化[編輯]
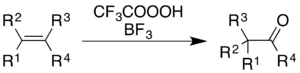
三氟過氧乙酸和三氟化硼一起使用,對烯烴和芳香環的氧化反應就伴隨著分子骨架的重排反應。[6]
對於烯烴,它的氧化產物是酮,不過反應機理不是簡單的環氧化後發生BF3催化的華格納-梅爾外因重排反應:[36]
對於芳香環的氧化,在《有機合成》中的一個例子是六甲苯氧化成2,3,4,5,6,6-六甲基-2,4-環己二烯酮:[10]

芳香環的氧化斷裂[編輯]
除了把芳香環氧化成羰基化合物(見重排氧化章節)以外,三氟過氧乙酸還能使芳香環的碳-碳鍵完全斷裂。在烷基芳香烴的氧化反應中,其它氧化劑會斷裂烷基部分並產生苯甲酸和相關化合物,而三氟過氧乙酸則會留下烷基並斷裂芳香環。[37][38]

這種對於某些鍵的選擇性使其可用於分解例如煤的複雜碳氫化合物混合物,以確定結構細節。[39][37]
含有雜原子的芳香系統對這種開環反應有抵抗力,因為雜原子的氧化會優先發生,使三氟過氧乙酸的親電攻擊對芳香環失效。舉個例子,嘌呤、吡啶和喹啉會先形成N-氧化物,[6]而像是八氟二苯駢噻吩的含硫雜環會被轉化成碸。[8][40]
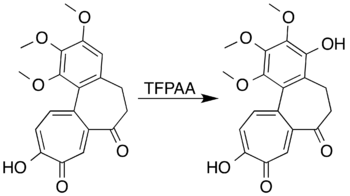
含有活化基團的芳香環會被氧化成酚,而不是發生開環反應。舉個例子,均三甲苯和三氟過氧乙酸反應的產物是均三甲苯酚(2,4,6-三甲基苯酚)。[8]研究人員試圖通過7-氧化脫乙醯胺基秋水仙素的拜耳-維立格氧化反應合成內酯,雖然反應不成功,但實現了對芳香環氧化高產率生產酚的反應:[6][41]
注釋[編輯]
參考資料[編輯]
- ^ 1.0 1.1 Kürti, László; Czakó, Barbara. Strategic Applications of Named Reactions in Organic Synthesis. Elsevier Academic Press. 2005: 28. ISBN 9780124297852.
- ^ 化工引擎. [2011-09-17]. (原始內容存檔於2013-04-25).
- ^ 3.0 3.1 3.2 3.3 3.4 3.5 Hiyama, Tamejiro. 8.2 Trifluoroacetic acid and Trifluoroperacetic acid. Organofluorine Compounds: Chemistry and Applications. Springer Science & Business Media. 2000: 255–257 [2021-12-30]. ISBN 9783662041642. (原始內容存檔於2021-12-30).
- ^ 4.0 4.1 Kataoka, T.; Yoshimatsu, M. Alkyl Chalcogenides: Selenium- and Tellurium-based Functional Groups. Ley, Steven V. (編). Synthesis: Carbon with One Heteroatom Attached by a Single Bond. Comprehensive Organic Functional Group Transformations. Elsevier. 1995: 277–296. ISBN 9780080423234.
- ^ 5.0 5.1 Carey, Francis A.; Sundberg, Richard J. 5.5 Addition Reactions Involving Epoxides. Advanced Organic Chemistry: Part A: Structure and Mechanisms 5th. Springer Science & Business Media. 2007: 503–514 [2021-12-30]. ISBN 9780387448978. (原始內容存檔於2021-12-30).
- ^ 6.00 6.01 6.02 6.03 6.04 6.05 6.06 6.07 6.08 6.09 6.10 6.11 6.12 6.13 6.14 6.15 6.16 6.17 Caster, Kenneth C.; Rao, A. Somasekar; Mohan, H. Rama; McGrath, Nicholas A.; Brichacek, Matthew. Encyclopedia of Reagents for Organic Synthesis. e-EROS Encyclopedia of Reagents for Organic Synthesis. 2012. ISBN 978-0471936237. doi:10.1002/047084289X.rt254.pub2.
|chapter=被忽略 (幫助) - ^ 7.0 7.1 Freeman, Jeremiah P. William D. Emmons: November 18, 1924 – December 8, 2001 (PDF). Org. Synth. November 14, 2002, 80: xxvii–xxix [January 21, 2017]. (原始內容 (PDF)存檔於March 16, 2015).
- ^ 8.0 8.1 8.2 8.3 8.4 8.5 8.6 8.7 Chambers, Richard D. Functional Compounds Containing Oxygen, Sulphur or Nitrogen and their Derivatives. Fluorine in Organic Chemistry. CRC Press. 2004: 242–243 [2021-12-30]. ISBN 9780849317903. (原始內容存檔於2021-12-30).
- ^ 9.0 9.1 Luxon, S. G. Hazards in the Chemical Laboratory 5th. Royal Society of Chemistry. 1992: 627. ISBN 9780851862293.
- ^ 10.0 10.1 (1968) "2,3,4,5,6,6-Hexamethyl-2,4-cyclohexadien-1-one". Org. Synth. 48; Coll. Vol. 5: 598.
- ^ Cooper, Mark S.; Heaney, Harry; Newbold, Amanda J.; Sanderson, William R. Oxidation Reactions Using Urea–Hydrogen Peroxide; A Safe Alternative to Anhydrous Hydrogen Peroxide. Synlett. 1990, 1990 (9): 533–535. doi:10.1055/s-1990-21156.
- ^ 12.0 12.1 12.2 12.3 Ziegler, Fredrick E.; Metcalf, Chester A.; Nangia, Ashwini; Schulte, Gayle. Structure and total synthesis of sporol and neosporol. J. Am. Chem. Soc. 1993, 115 (7): 2581–2589. doi:10.1021/ja00060a006.
- ^ Kang, Ho-Jung; Jeong, Hee-Sun. New Method of Generating Trifluoroperoxyacetic acid for the Baeyer-Villiger Reaction. Bull. Korean Chem. Soc. 1996, 17 (1): 5–6 [2021-12-30]. (原始內容存檔於2021-12-30).
- ^ 14.0 14.1 Emmons, William D.; FerrisEmmons, Arthur F. Oxidation Reactions with Pertrifluoroacetic Acid. J. Am. Chem. Soc. 1953, 75 (18): 4623–4624. doi:10.1021/ja01114a539.
- ^ 15.0 15.1 Emmons, William D. Peroxytrifluoroacetic Acid. I. The Oxidation of Nitrosamines to Nitramines. J. Am. Chem. Soc. 1954, 76 (13): 3468–3470. doi:10.1021/ja01642a029.
- ^ 16.0 16.1 Emmons, William D. Peroxytrifluoroacetic Acid. II. The Oxidation of Anilines to Nitrobenzenes. J. Am. Chem. Soc. 1954, 76 (13): 3470–3472. doi:10.1021/ja01642a030.
- ^ Emmons, William D.; Pagano, Angelo S.; Freeman, Jeremiah P. Peroxytrifluoroacetic Acid. III. The Hydroxylation of Olefins. J. Am. Chem. Soc. 1954, 76 (13): 3472–3474. doi:10.1021/ja01642a031.
Emmons, William D.; Pagano, Angelo S. Peroxytrifluoroacetic Acid. IV. The Epoxidation of Olefins. J. Am. Chem. Soc. 1955, 77 (1): 89–92. doi:10.1021/ja01606a029.
Emmons, William D.; Lucas, George B. Peroxytrifluoroacetic Acid. V. The Oxidation of Ketones to Esters. J. Am. Chem. Soc. 1955, 77 (8): 2287–2288. doi:10.1021/ja01613a077.
Emmons, William D.; Pagano, Angelo S. Peroxytrifluoroacetic Acid. VI. The Oxidation of Oximes to Nitroparaffins. J. Am. Chem. Soc. 1955, 77 (17): 4557–4559. doi:10.1021/ja01622a036. - ^ 18.0 18.1 Aubé, Jeffrey; Fehl, Charlie; Liu, Ruzhang; McLeod, Michael C.; Motiwala, Hashim F. 6.15 Hofmann, Curtius, Schmidt, Lossen, and Related Reactions. Heteroatom Manipulations. Comprehensive Organic Synthesis II 6. 1993: 598–635. ISBN 9780080977430. doi:10.1016/B978-0-08-097742-3.00623-6.
- ^ (1988) "Hofmann Rearrangement Under Mildly Acidic Conditions Using [I,I-Bis(Trifluoroacetoxy)Iodobenzene: Cyclobutylamine Hydrochloride from Cyclobutanecarboxamide]". Org. Synth. 66; Coll. Vol. 8: 132.
- ^ Myers, Andrew G. Chemistry 115 Handouts: Oxidation (PDF). Harvard University. [10 January 2017]. (原始內容 (PDF)存檔於2017-05-16).
- ^ Carruthers, William. 6.3 Oxidation of Olefins. Some Modern Methods of Organic Synthesis. Cambridge University Press. 1971: 259–280 [2021-12-30]. ISBN 9780521096430. (原始內容存檔於2021-12-30).
- ^ Carruthers, William. 6.5 Baeyer–Villiger oxidation of ketones. Some Modern Methods of Organic Synthesis. Cambridge University Press. 1971: 287–290 [2021-12-30]. ISBN 9780521096430. (原始內容存檔於2022-04-25).
- ^ 23.0 23.1 Hagen, Timothy J. Prilezhaev reaction. Li, Jie Jack; Corey, E. J. (編). Name Reactions of Functional Group Transformations. John Wiley & Sons. 2007: 274–281. ISBN 9780470176504.
- ^ Prileschajew, Nikolaus. Oxydation ungesättigter Verbindungen mittels organischer Superoxyde [Oxidation of unsaturated compounds by means of organic superoxides]. Ber. Dtsch. Chem. Ges. 1909, 42 (4): 4811–4815 [2021-12-31]. doi:10.1002/cber.190904204100. (原始內容存檔於2019-10-03) (德語).
- ^ Hayakawa, Y.; Baba, Y.; Makino, S.; Noyori, R. Carbon-carbon bond formation promoted by transition metal carbonyls. 19. General synthesis of tropane alkaloids via the polybromo ketone-iron carbonyl reaction. J. Am. Chem. Soc. 1978, 100 (6): 1786–1791. doi:10.1021/ja00474a021.
- ^ 26.0 26.1 Pirrung, Michael C.; Morehead, Andrew T.; Young, Bruce G. (編). 10. Neosporol, Sporol. Part B: Bicyclic and Tricyclic Sesquiterpenes. The Total Synthesis of Natural Products 11. John Wiley & Sons. 2000: 222–224 [2021-12-31]. ISBN 9780470129630. (原始內容存檔於2022-05-05).
- ^ Brooke, G. M.; Burdon, J.; Tatlow, J. C. Aromatic polyfluoro-compounds. Part VII. The reaction of pentafluoronitrobenzene with ammonia. J. Chem. Soc. 1961: 802–807. doi:10.1039/JR9610000802.
- ^ Taylor, Edward C.; McKillop, Alexander. A New Synthesis of 5-Nitropyrimidines. J. Org. Chem. 1965, 30 (9): 3153–3155. doi:10.1021/jo01020a067.
- ^ Taylor, P. C. Vinyl and Aryl Chalcogenides: Sulfur-, Selenium- and Tellurium-based Functional Groups. Ley, Steven V. (編). Synthesis: Carbon with One Heteroatom Attached by a Single Bond. Comprehensive Organic Functional Group Transformations. Elsevier. 1995: 705–736. ISBN 9780080423234.
- ^ Page, P. C. B.; Wilkes, R. D.; Reynolds, D. Alkyl Chalcogenides: Sulfur-based Functional Groups. Ley, Steven V. (編). Synthesis: Carbon with One Heteroatom Attached by a Single Bond. Comprehensive Organic Functional Group Transformations. Elsevier. 1995: 113–276. ISBN 9780080423234.
- ^ 31.0 31.1 31.2 31.3 31.4 Treiber, Alexander. Mechanism of the Aromatic Hydroxylation of Thiophene by Acid-Catalyzed Peracid Oxidation. J. Org. Chem. 2002, 67 (21): 7261–7266. PMID 12375952. doi:10.1021/jo0202177.
- ^ Mansuy, Daniel; Valadon, Philippe; Erdelmeier, Irene; López Garcia, Pilar; Amar, Claudine; Girault, Jean-Pierre; Dansette, Patrick M. Thiophene S-Oxides as new Reactive Metabolites: Formation by Cytochrome P-450 Dependent Oxidation and Reaction with Nucleophiles. J. Am. Chem. Soc. 1991, 113 (20): 7825–7826. doi:10.1021/ja00020a089.
- ^ Correia, Maria A.; Hollenberg, Paul F. Inhibition of Cytochrome P450 Enzymes. Ortiz de Montellano, Paul R. (編). Cytochrome P450: Structure, Mechanism, and Biochemistry 4th. Springer. 2015: 177–260 [2021-12-30]. ISBN 9783319121086. (原始內容存檔於2022-04-12).
- ^ Macherey, Anne-Christine; Dansette, Patrick M. Biotransformations Leading to Toxic Metabolites:Chemical Aspects. Wermuth, Camille Georges; Aldous, David; Raboisson, Pierre; Rognan, Didier (編). The Practice of Medicinal Chemistry 4th. Elsevier. 2015: 585–614 [2021-12-30]. ISBN 9780124172135. (原始內容存檔於2021-12-30).
- ^ Anslyn, Eric V.; Dougherty, Dennis A. 8.8 Miscellaneous Experiments for Studying Mechanism. Modern Physical Organic Chemistry. University Science Books. 2006: 471–482 [2021-12-30]. ISBN 9781891389313. (原始內容存檔於2021-12-30).
- ^ Hart, Harold; Lerner, Lawrence R. Oxidations with peroxytrifluoroacetic acid-boron trifluoride. IX. Direct oxidation of alkenes to ketones using peroxytrifluoroacetic acid–boron fluoride. J. Org. Chem. 1967, 32 (9): 2669–2673. doi:10.1021/jo01284a004.
- ^ 37.0 37.1 Deno, Norman C.; Greigger, Barbara A.; Stroud, Stephen G. New method for elucidating the structures of coal. Fuel. 1978, 57 (8): 455–459. doi:10.1016/0016-2361(78)90153-9.
- ^ Deno, Norman C.; Greigger, Barbara A.; Messer, Lauren A.; Meyer, Michael D.; Stroud, Stephen G. Aromatic ring oxidation of alkylbenzenes. Tetrahedron Lett. 1977, 18 (20): 1703–1704. doi:10.1016/S0040-4039(01)93253-8.
- ^ Deno, Norman C.; Curry, Kenneth W.; Greigger, Barbara A.; Jones, A. Daniel; Rakitsky, Walter G.; Smith, Karen A.; Wagner, Karen; Minard, Robert D. Dihydroaromatic structure of Illinois No. 6 Monterey coal. Fuel. 1980, 59 (10): 694–698 [2021-12-31]. doi:10.1016/0016-2361(80)90021-6. (原始內容存檔於2020-06-26).
- ^ Chambers, R. D.; Cunningham, J. A.; Spring, D. J. Polyfluoroaryl organometallic compounds. Part VIII. Synthesis of and nucleophilic substitution in octafluorodibenzofuran. J. Chem. Soc. C. 1968: 1560–1565. doi:10.1039/J39680001560.
- ^ Berg, Ulf; Bladha, Håkan; Mpamposa, Konstantinos. Stereochemical variations on the colchicine motif. Peracid oxidation of thiocolchicone. Synthesis, conformation and inhibition of microtubule assembly. Org. Biomol. Chem. 2004, 2 (14): 2125–2130. PMID 15254641. doi:10.1039/B402840F.
