伯奇還原反應
伯奇還原反應(Birch還原)是指用鈉和醇在液氨中將芳香環還原成1,4-環己二烯的有機還原反應。此反應最早由澳大利亞化學家Arthur John Birch (1915–1995)在1944年發表。[1] Birch還原的重要性在於:儘管剩下的雙鍵(非芳香性)更為活潑,該反應卻能停留在環己雙烯上,而不繼續還原。

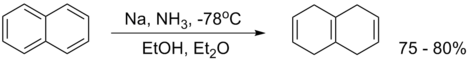
其他人也發表了很多篇關於此反應的綜述。[3][4][5][6]
反應機理[編輯]
鈉溶於液氨中會形成一個電子鹽的亮藍色溶液,化學式為[Na(NH3)x]+ e−。溶劑化電子會與芳香環加成,形成一個自由基負離子。溶液中的醇此時作為質子試劑提供一個氫原子。對大多數反應物來說,氨上的氫酸性還不夠。[7]

如果是取代芳香化合物,當取代基是羧基等吸電子基時,能夠穩定碳負離子並生成最少取代的烯烴;[8] 當取代基是推電子基團時,則生成取代最多的烯烴。[9] 熱力學不穩定的非共軛1,4-加成產物往往產率超過熱力學穩定的1,3-加成產物,這是由於共軛的戊二烯負離子中間體HOMO的最大軌道係數是在中間那個碳原子上,導致生成的1,4-環己雙烯沒有辦法經過平衡移動而生成更加熱力學穩定的產物,因此,生成的是動力學穩定產物。

Birch烷基化[編輯]
在鹵代烴的存在下,上文提到的碳負離子也可以發生親核取代反應生成新的碳-碳鍵。如下圖所示,在Birch還原中生成的負離子中間體可以被一個合適的親電試劑捕獲,例如鹵代烴:[10]

根據逆合成分析,前者即是後者的合成子。
在下圖所示反應中,1,4-二溴丁烷被加入到苯甲酸叔丁酯中,最後生成烷基化的1,4-環己雙烯產物。 [11]

參見[編輯]
參考文獻[編輯]
- ^ (a) Birch, A. J. J. Chem. Soc. 1944, 430. (b) Birch, A. J. J. Chem. Soc. 1945, 809. (c) Birch, A. J. J. Chem. Soc. 1946, 593. (d) Birch, A. J. J. Chem. Soc. 1947, 102 & 1642. (e) Birch, A. J. J. Chem. Soc. 1949, 2531.
- ^ Vogel, E.; Klug, W.; Breuer, A. 1,6-Methano-10-annulene. Organic Syntheses. 1974, 54: 11 [2008-04-24]. (原始內容存檔於2012-07-28).
- ^ Birch, A. J.; Smith, H. Quart. Rev. 1958, 12, 17. (Review)
- ^ Caine, D. Org. React. 1976, 23, 1-258. (Review)
- ^ Rabideau, P. W.; Marcinow, Z. Org. React. 1992, 42, 1-334. (Review)
- ^ Mander, L. N. Comp. Org. Syn. 1991, 8, 489-521. (Review)
- ^ March, Jerry. Advanced Organic Chemistry, Reactions, Mechanisms and Structure third Edition. John Wiley & Sons. 1985. ISBN 0-471-85472-7.
- ^ Kuehne, M. E.; Lambert, B. F. 1,4-Dihydrobenzoic acid. Organic Syntheses. 1963, 43: 22 [2008-04-24]. (原始內容存檔於2008-02-05).
- ^ Paquette, L. A.; Barrett, J. H. 2,7-Dimethyloxepin. Organic Syntheses. 1969, 49: 62 [2008-04-24]. (原始內容存檔於2008-02-05).
- ^ Taber, D. F.; Gunn, B. P.; Ching Chiu, I. Alkylation of the anion from Birch reduction of o-Anisic acid: 2-Heptyl-2-cyclohexenone. Organic Syntheses. 1983, 61: 59 [2008-04-24]. (原始內容存檔於2008-02-05).
- ^ Formation of Benzo-Fused Carbocycles by Formal Radical Cyclization onto an Aromatic Ring Derrick L. J. Clive and Rajesh Sunasee Org. Lett.; 2007; 9(14) pp 2677 - 2680; (Letter) doi:10.1021/ol070849l
