電子層

電子層,或稱電子殼或電子殼層,是原子物理學中,一組擁有相同主量子數n的原子軌道。電子層組成為一粒原子的電子序。這可以證明電子層可容納最多電子的數量為(但當第一層電子為倒数第一层只能容纳2个;倒数第1层只能容纳8个,倒数第2层只能容纳18个),這種全滿的電子層稱為「閉合殼層」。
亨利·莫塞萊和查尔斯·巴克拉的X-射線吸收研究首次於實驗中發現電子層。巴克拉把它們稱為K、L和、M(以英文字母排列)等電子層。這些字母後來被n值1、2、3等取代。它們被用於分光鏡的西格班記號法。
電子層的名字起源於波耳模型中,電子被認為一組一組地圍繞著核心以特定的距離旋轉,所以軌跡就形成了一個殼。
历史[编辑]
主电子层[编辑]
主電子層从内向外分别是:K,L,M,N,O,P以及Q,或记作1,2,3,4,5,6以及7。
亞電子層[编辑]

每个主電子層由至少一个的亚层组成,且每一个都占据了一種原子轨道,而一種可能又有多個軌域。
比如,最里面的主电子层K层有一个亚层1s;L层有两个亚层,2s和2p,2p軌域中又分成Px、Py、Pz三個軌域。M层有3s,3p和3d;N层有4s,4p,4d和4f;O层有5s,5p,5d,5f亚层,理论上可以有更多亚层,但锕系元素的电子层都只占有5f亚层的一部分。
每個亞電子層最极限电子数為4ℓ + 2 個電子,ℓ為角量子數,即:
| 亞電子層符号 | ℓ | 极限电子数 | 所位在的主電子層 | 命名來源 |
|---|---|---|---|---|
| s | 0 | 2 | 第一层(K)及以上 | sharp(锐线系) |
| p | 1 | 6 | 第二层(L)及以上 | principal(主线系) |
| d | 2 | 10 | 第三层(M)及以上 | diffuse(漫线系) |
| f | 3 | 14 | 第四层(N)及以上 | fundamental(基线系) |
| g | 4 | 18 | 第五层(O)及以上 | f 的后一个字母,(如:g,h,i......) |
| h | 5 | 22 | 第六层(P)及以上 | |
| i | 6 | 26 | 第七层(Q)及以上 |
每一層的電子數[编辑]
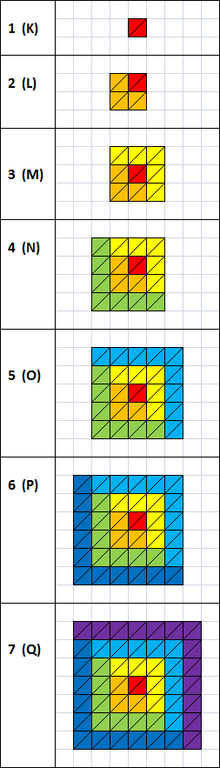
每個主電子層的极限电子数為2n2個電子,n為主量子數,即:
| 主電子層名稱 | 主量子數 | 亚电子层名称 | 亚电子层最大电子数 | 极限电子数 |
|---|---|---|---|---|
| K | 1 | 1s | 2 | 2 |
| L | 2 | 2s | 2 | 2 + 6 = 8 |
| 2p | 6 | |||
| M | 3 | 3s | 2 | 2 + 6 + 10 = 18 |
| 3p | 6 | |||
| 3d | 10 | |||
| N | 4 | 4s | 2 | 2 + 6 + 10 + 14 = 32 |
| 4p | 6 | |||
| 4d | 10 | |||
| 4f | 14 | |||
| O | 5 | 5s | 2 | 2 + 6 + 10 + 14 + 18 = 50 |
| 5p | 6 | |||
| 5d | 10 | |||
| 5f | 14 | |||
| 5g | 18 | |||
| P | 6 | 6s | 2 | 2 + 6 + 10 + 14 + 18 + 22 = 72 |
| 6p | 6 | |||
| 6d | 10 | |||
| 6f | 14 | |||
| 6g | 18 | |||
| 6h | 22 | |||
| Q | 7 | 7s | 2 | 2 + 6 + 10 + 14 + 18 + 22 + 26 = 98 |
| 7p | 6 | |||
| 7d | 10 | |||
| 7f | 14 | |||
| 7g | 18 | |||
| 7h | 22 | |||
| 7i | 26 |
電子層能量和填充順序[编辑]


儘管有時會說主電子層中的所有每個電子都具有相同的能量,但這只是一個近似值。然而,一個亞電子層中的每個電子確實具有完全相同的能量水平,之後的亞電子層比早期亞電子層的電子會具有更多的能量。這種效應足夠大,以至於與電子層相關的能量範圍可以重疊。
用主電子層和亞電子層從較低能量的亞電子層進行到較高能量的亞電子層。這遵循“n + ℓ 規則”,通常也稱為遞建原理(亦稱馬德隆規則)。具有較低 n + ℓ 值的亞電子層會比具有較高 n + ℓ 值的亞電子層之前優先填充。在 n + ℓ 值相等的情況下,首先填充具有較低 n 值的亞電子層。
正因為如此,後來的主電子層被填滿了元素週期表的大部分區域。 K電子層填充第一個週期(氫和氦),而 L電子層填充第二個週期(鋰到氖)。然而,M電子層從鈉(元素 11)開始填充,但直到銅(元素 29)才完成填充,而 N 電子層甚至更慢:它從鉀(元素 19)開始填充,但直到鐿才完成電子填充(元素 70)。 O、P 和 Q 電子層開始填充已知元素,但即使在最重的已知元素鿫(元素 118),電子也沒填完電子層。
参考资料[编辑]
- Tipler, Paul & Ralph Llewellyn (2003). Modern Physics (4th ed.). New York: W. H. Freeman and Company. ISBN 0-7167-4345-0


