石墨层间化合物


石墨层间化合物(Graphite intercalation compound,缩写GIC)又称石墨插层化合物、石墨插层复合物,是由带正电或负电的离子插入被氧化或还原的石墨层间后形成的具有二维层状结构的化合物,通式为MCx·δS。式中M表示插入石墨层间的带电荷离子、S为可能存在的与离子共插层的电中性溶剂分子。[1][2][3][4]
结构
[编辑]表征石墨层间化合物的结构,主要是指表征其层堆叠方向(c轴方向)的参数。其基本结构是由n层石墨烯与一层插层物交替堆叠,称为n阶石墨层间化合物(stage-n GIC,n一般为正整数),其中1阶为可能形成的最低阶产物。
与其他所有二维层状物质不同,石墨在插层或脱插层过程中可以连续相变并形成n≥2动力学或热力学稳定的插层化合物,这一特殊现象被称做成阶(staging)。导致成阶现象的原因是石墨烯特有的高度柔性,对应目前最为广泛接受的Daumas-Hérold模型。
组分
[编辑]所有碱金属及部分碱土金属、稀土金属可以通过固相反应与石墨形成二元1阶插层化合物,如钾、铷、铯的金属通常为MC8,对于金属如锂、锶、钙、钡、铕、镱,则通式常为XC6。[2]
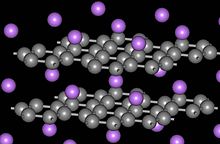
以钙为例,CaC6可由石墨与锂钙合金在350 °C加热10天制备。层间距由石墨的3.35 Å扩大到4.52 Å,碳碳键长也从石墨的1.42 Å扩大到1.444 Å。在超导石墨层间化合物中,CaC6的临界转变温度最高,达到11.5K。加压后转变温度还可进一步提高(15.1 K在8 GPa时)。[2]
性质
[编辑]LiC6因锂离子较小半径是已知体积膨胀率最小的1阶GIC之一,被广泛应用为商用锂离子电池的负极材料。充电过程中锂离子由电解液嵌入负极,放电时脱嵌,从石墨生成LiC6的理论容量为372mAh/g。
KC8是已知最强的还原剂之一。一般在惰性气体氛围的保护下以熔融态的金属钾还原石墨粉制得,[5][6]或是在真空双泡管中以加热扩散的金属钾蒸气还原石墨粉制得,[7]还可以通过电化学法在含钾离子的电解液中还原石墨电极制备。[8]钾离子进入石墨层间,颜色由黑色逐渐变蓝,最终变为金色的KC8。从结构上来说,相邻钾离子的距离是碳骨架六边形距离的两倍。碳与钾之间形成了离子键,使得此化合物为良导体。[9] KC8也是超导体,其超导转变温度为0.14K。[2]
参考
[编辑]- ^ M.S. Dresselhaus and G. Dresselhaus Review:. Intercalation compounds of graphite. Advances in Physics. 1981, 30 (2): 139–326. Bibcode:1981AdPhy..30..139D. doi:10.1080/00018738100101367. (187 pages), also reprinted as Dresselhaus, M. S.; Dresselhaus, G. Intercalation compounds of graphite. Advances in Physics. 2002, 51: 1–186. Bibcode:2002AdPhy..51....1D. doi:10.1080/00018730110113644.
- ^ 2.0 2.1 2.2 2.3 N. Emery; et al. Review: Synthesis and superconducting properties of CaC6. Sci. Technol. Adv. Mater. (free download pdf). 2008, 9: 044102. doi:10.1088/1468-6996/9/4/044102.
- ^ H-P Boehm; et al. Nomenclature and terminology of graphite intercalation compounds (PDF). Pure & Appl. Chem. 1994, 66: 1893. (原始内容 (free download pdf)存档于2012-04-06).
- ^ D. Savoia; et al. Applications of potassium-graphite and metals dispersed on graphite in organic synthesis (free download pdf). Pure & Appl. Chem. 1985, 57: 1887 [2009-10-15]. (原始内容存档 (PDF)于2009-09-29).
- ^ Ottmers, D.M.; Rase, H.F. Potassium graphites prepared by mixed-reaction technique. Carbon. 1966-05, 4 (1): 125–127. doi:10.1016/0008-6223(66)90017-0.
- ^ D. E. Bergbreiter; et al. Reactions of potassium-graphite. J. Am. Chem. Soc. 1978, 100: 2126. doi:10.1021/ja00475a025.
- ^ D. E. Nixon; et al. Formation and structure of the potassium graphites. J. Phys. D Appl. Phys. 291, 1: 2126. doi:10.1088/0022-3727/1/3/303.
- ^ Z. Jian; et al. Carbon electrodes for K-ion batteries. J. Am. Chem. Soc. 2015, 137: 11566. doi:10.1021/jacs.5b06809.
- ^ NIST Ionizing Radiation Division 2001 - Technical Highlights. [2009-10-15]. (原始内容存档于2014-11-29).
延伸阅读
[编辑]- M. Endo and M. Suzuki. Graphite intercalation compounds and applications. Oxford University Press. 2003. ISBN 0195128273.
