塔菲尔方程
外观
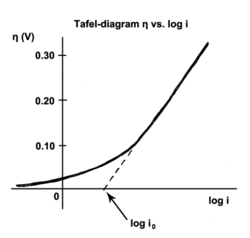
塔菲尔方程给出了电极反应的反应速率和过电位的关系[1]。塔菲尔方程最早是由瑞士化学家尤利乌斯·塔菲尔根据实验数据归纳得出。
单电极的塔菲尔方程可以写作:
式中
概述
[编辑]交换电流密度指的是氧化剂或还原剂和电极之间达到电子转移平衡时的电流密度,代表着两者平衡时的电化学反应速率。塔菲尔斜率可以通过实验求出,也可以通过理论推导。
定义为
式中
另一形式
[编辑]塔菲尔方程还可以写作
式中
应用
[编辑]塔菲尔方程可以应用于极化率高的区域,对于低极化率区域,电流和极化率常呈线性关系:
参见
[编辑]参考文献
[编辑]- ^ Bard, A. J.; Faulkner, L. R. “Electrochemical Methods. Fundamentals and Applications” 2nd Ed. Wiley, New York. 2001. ISBN 0-471-04372-9
- G.T. Burstein. A Century of Tafel’s Equation: 1905–2005 A Commemorative Issue of Corrosion Science. Corrosion Science. 2005, 47 (12): 2858–2870. doi:10.1016/j.corsci.2005.07.002.



















