磷的同素异形体

磷的同素异形体有许多种,其中白磷和红磷最为常见。另外还存在紫磷和黑磷。气态磷单质中有P2分子与磷原子。

| 形态 | 白磷(α) | 白磷(β) | 紫磷 | 黑磷 | 红磷 |
|---|---|---|---|---|---|
| 晶系 | 体心立方 | 三斜 | 单斜 | 正交、三方、面心立方、无定形 | 无定形 |
| 皮尔逊符号 | aP24 | mP84 | oS8 | - | |
| 空间群 | I43m | P1 No.2 | P2/c No.13 | Cmca No.64 | - |
| 密度(g/cm3) | 1.828 | 1.88 | 2.36 | 2.69 | 2.0 ~ 2.4 |
| 能隙(eV) | 2.1 | 1.5 | 0.34 | ||
| 折射率 | 1.8244 | 2.6 | 2.4 |
白磷
[编辑]

白磷(因商品白磷常带黄色,故又稱為黄磷[3]:180),分子式P4,为白色固体,质软。白磷有剧毒,致死量为50mg[4]:422。不溶于水,溶于大多数有机溶剂[4]:422。常温下为立方晶系的α-型,具体结构仍未知,熔点为44.1℃。-77℃一以下转化为六方晶系的β-型,密度1.88g/cm3。[4]:422可用於製造磷酸及肥料。实验室置于冷水中保存。常用于化学武器。34°C时可在空气中自燃,生成白色烟雾,主要成分为五氧化二磷(烟)以及五氧化二磷于空气中水结合生成的磷酸(雾)。
白磷弹是利用了白磷在空气中自燃特性的化学武器,曾被当作燃烧弹使用,但后来由于對交战国士兵造成的巨大身体及心理创伤而逐渐被各国弃用,转而作为目标指示弹及烟雾弹使用。
安全
[编辑]过去,不慎误服白磷后常用硫酸铜溶液洗胃,原因是白磷和硫酸銅溶液會發生如下反應:
但是,硫酸铜有毒,会损害肾脏和大脑。目前,在美国等国家已经不再使用。在一本美国海军编制的手册中則推荐使用碳酸氢盐溶液来中和磷酸。[5]
红磷
[编辑]

“红磷”一词可以指代所有带红色的磷,故其具有多种晶型,它们的密度介于2.0-2.4g/cm3 之间,熔点介于585-610℃之间。红磷在许多溶剂中都很难溶解,不能自燃,也基本没有毒性。[4]:424
将白磷加熱至400℃以下或用紫外光照射白磷即可獲得紅磷,在硫、碘或钨丝的催化下加热可以加快转化速率[3]:183-184。紅磷的結構屬多分子不規則排列。
用途
[编辑]可當火柴摩擦面。
在俄羅斯和前蘇聯地區,紅磷是一種監控物質,因為紅磷可用作非法生產安非他命類的興奮劑。
黑磷
[编辑]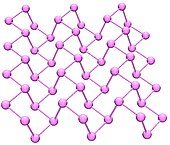

黑磷是一种有金属光泽的晶体,是磷的同素异形体中密度最大、热力学最稳定以及性质最不活泼的一种。它是高聚的不溶性固体。[4]:422它是用白磷在很高压强(12,000大氣壓)和较高温度(200℃)下转化而形成的。
种类
[编辑]目前已知的黑磷有四种晶系:正交、三方、面心立方和无定形[4]:422。三方黑磷是由许多层聚合的六元环组成,类似石墨。正交黑磷的结构类似于有“褶皱”的六元环所组成。面心立方黑磷中每个磷原子都处于6个其他磷原子组成的八面体中心。高压下,正交黑磷会可逆地转变为三方和面心立方黑磷。[4]:423无定形的黑磷在125°C时开始向红磷转变。
结构
[编辑]黑磷具有像石墨的片状结构和導電性,黑磷晶体有一些本质特征:如晶体内不仅有共价键,还有离子键和范德华力。
紫磷
[编辑]

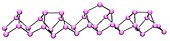
紫磷为单斜晶系,又名希托夫磷。此分子的结构较为复杂,每个磷原子的三条键呈三角锥,互相堆积成为管状结构,并排列为双层。每两层又垂直地堆积形成三维结构。[4]:423 紫磷加熱至300°C才能在空氣中被點燃,不溶於所有的溶劑,具有金屬光澤,因此雖非金屬卻稱作金屬磷。
紫磷可透過把白磷以500°C溶解在盛有熔融的鉛的密封管中18小時製得。此外,透過在一密封管中以530°C加熱紅磷,密封管的上半部維持在444°C,亦可製得紫磷結晶。
若紫磷在一充滿不活潑氣體中(如氮氣或二氧化碳)被加熱則會昇華,得出的氣體會凝華為白磷。[來源請求]
环状磷
[编辑]环状的磷在 2007年被预测。[6] 环状的磷是使用蒸汽封装法在疏散的多壁碳纳米管内自行组装的,内径为5-8纳米。在原子尺度为5.90纳米的多壁碳纳米管内观察到一个直径为5.30纳米的环,由23个P8和23个P2单元组成,共230个磷原子,邻近的两个磷环的距离为 6.4 Å。[7]
P6 环状分子不稳定,不能分离。
蓝磷
[编辑]于2016年,通过分子束外延的方法用黑磷作为前体,开始生产一层的蓝磷。 [8]
二磷分子
[编辑]

二磷分子 (P2) 可以在极端条件下产生 (例如1100开氏度下的 P4) 。 2006年,在正常条件下,人们发现使用某些过渡金属的配合物(例如,钨和铌的配合物)就可以在均质溶液中产生二磷分子。 [9]
二磷是磷的气态形式,在 1200 °C 至 2000 °C 下热稳定。 白磷分子(P
4) 在低温就开始分解成二磷并形成平衡。 P
2 分子在 800 °C 下的浓度是 ≈ 1%。 到了 2000 °C以上,二磷分子会分解成自由磷原子。
参考资料
[编辑]- ^ A. Holleman, N. Wiberg. XV 2.1.3. Lehrbuch der Anorganischen Chemie 33. de Gruyter. 1985. ISBN 3-11-012641-9.
- ^ Berger, L. I. Semiconductor materials. CRC Press. 1996: 84. ISBN 0-8493-8912-7.
- ^ 3.0 3.1 张青莲. 无机化学丛书 第四卷. 1995-01-01. ISBN 9787030305480.
- ^ 4.0 4.1 4.2 4.3 4.4 4.5 4.6 4.7 麦松威.周公度.李伟基. 高等无机结构化学. 2001-07. ISBN 9787301047934.
- ^ US Navy's Treatment of Chemical Agent Casualties and Conventional Military Chemical Injuries: FM8-285: Part 2 Conventional Military Chemical Injuries. [2009-05-05]. (原始内容存档于2005-11-22).
- ^ Karttunen, Antti J.; Linnolahti, Mikko; Pakkanen, Tapani A. Icosahedral and Ring-Shaped Allotropes of Phosphorus. Chemistry - A European Journal. 15 June 2007, 13 (18): 5232–5237. PMID 17373003. doi:10.1002/chem.200601572.
- ^ Zhang, Jinying; Zhao, Dan; Xiao, Dingbin; Ma, Chuansheng; Du, Hongchu; Li, Xin; Zhang, Lihui; Huang, Jialiang; Huang, Hongyang; Jia, Chun-Lin; Tománek, David; Niu, Chunming. Assembly of Ring-Shaped Phosphorus within Carbon Nanotube Nanoreactors. Angewandte Chemie International Edition. 6 February 2017, 56 (7): 1850–1854. PMID 28074606. doi:10.1002/anie.201611740.
- ^ Zhang, Jia Lin; Zhao, Songtao and 10 others. Epitaxial Growth of Single Layer Blue Phosphorus: A New Phase of Two-Dimensional Phosphorus. Nano Letters. 30 June 2016, 16 (8): 4903–4908. Bibcode:2016NanoL..16.4903Z. PMID 27359041. doi:10.1021/acs.nanolett.6b01459.
- ^ Piro, Na; Figueroa, Js; Mckellar, Jt; Cummins, Cc. Triple-bond reactivity of diphosphorus molecules. Science. 2006, 313 (5791): 1276–9. Bibcode:2006Sci...313.1276P. PMID 16946068. doi:10.1126/science.1129630.

