貝里斯-希爾曼反應
外觀
(重新導向自Baylis-Hillman反应)
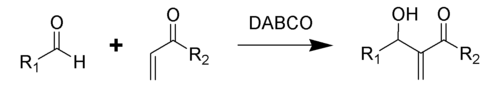
貝里斯-希爾曼反應(Baylis–Hillman reaction),是α,β-不飽和化合物與親電試劑(醛、酮)在合適的催化劑作用下,生成烯烴α-位加成產物的反應。催化劑一般採用DABCO(1,4-二氮雜雙環[2,2,2]辛烷的縮寫形式,俗稱:三亞乙基二胺),生成物為烯丙基醇[1]。這一反應又被稱為森田-貝里斯-希爾曼反應(Morita–Baylis–Hillman reaction),或者簡稱為MBH反應(MBH reaction)[2],這一反應名稱得名自日本化學家森田健一(Ken-ichi Morita)、英國化學家安東尼·貝里斯(Anthony B. Baylis)和德國化學家梅維爾·希爾曼(Melville E. D. Hillman)。
後來,親電試劑擴展到亞胺類sp2型碳的親電試劑,稱為氮雜-貝里斯-希爾曼反應[3]。
反應底物中的親電試劑可以是醛、亞胺、亞胺鹽以及活化的酮。α,β-不飽和化合物(活化烯烴)可以是丙烯酸酯、丙烯醛、乙烯基酮、丙烯腈、α,β-不飽和碸、亞碸、亞胺以及α,β-不飽和環烯酮等缺電子烯烴。
除DABCO可作為催化劑外,其他的叔胺和叔膦乃至硒酚鋰等弱親核試劑也可以用於催化這個反應[4][5]。
反應機理
[編輯]貝里斯-希爾曼反應經歷叔胺與活化烯烴的Michael加成反應啟動的加成-消除反應歷程[6]。

反應特點
[編輯]- 反應原料廉價,比較易得。
- 反應具有原子經濟性。
- 反應產物具有多個可以進一步反應,進行繼續轉化的官能團。
- 環境友好,反應用到的催化劑主要是有機小分子催化劑,從而可以避免通常情況下,不對稱催化反應中可能用到的金屬離子。
- 反應條件溫和,多數反應在室溫條件下就可以進行。
應用
[編輯]參見
[編輯]參考資料
[編輯]- ^ Baylis, A. B.; Hillman, M. E. D. German Patent. 1972. 缺少或
|title=為空 (幫助) 2,155,113. - ^ Morita, K.; Z. Suzuki, H. Hirose. Bull. Chem. Soc. Jpn. 1968, 41 (2815). 缺少或
|title=為空 (幫助) - ^ Perlmutter, P.; Teo, C. C. Tetrahedron Lett. 1984, 25 (5951). 缺少或
|title=為空 (幫助) - ^ Basavaiah, D.; Rao, P. D.; Hyma, R. S. Tetrahedron. 1996, 52: 8001. 缺少或
|title=為空 (幫助)(綜述) - ^ Ciganek, E. Org. React. 1997, 51 (201). 缺少或
|title=為空 (幫助)(綜述) - ^ Hill, J. S.; Isaacs, N. S. J. Phys. Org. Chem. 1990, 3 (285). 缺少或
|title=為空 (幫助) - ^ Iwabuchi, Y.; Nakatani, M.; Yokoyama, N.; Hatakeyama, S. J. Am. Chem. Soc. 1999, 121 (10219). 缺少或
|title=為空 (幫助) - ^ Iura, Y.; Sugahara, T.; Ogasawara, K. Org. Lett. 2001, 3 (291). 缺少或
|title=為空 (幫助) - ^ Shi, M.; Xu, Y.-M. Angew. Chem. Int. Ed. 2002, 41 (4507). 缺少或
|title=為空 (幫助)
