弗賴斯重排反應
弗賴斯重排反應是酚酯在路易斯酸或布朗斯特酸催化下重排為鄰位或對位酰基酚的反應。[1][2][3]
反應由德國化學家 Karl Theophil Fries 首先報道。
反應常用的路易斯酸催化劑有三氯化鋁、三氟化硼、氯化鋅、氯化鐵、四氯化鈦、四氯化錫和三氟甲磺酸鹽。也可以用氟化氫或甲磺酸等質子酸催化。鄰、對位產物的比例取決於原料酚酯的結構、反應條件和催化劑的種類等。一般來說,對位產物是動力學控制產物,鄰位產物是熱力學控制產物。反應在低溫(100°C 以下)下進行時主要生成對位產物,而在較高溫度時一般得到鄰位產物。可利用鄰、對位性質上的差異來分離這兩者。一般鄰位異構體可以生成分子內氫鍵,可隨水蒸氣蒸出。
脂肪或芳香羧酸的酚酯都可以發生重排。因取代基影響反應,底物不能含有位阻大的基團。當酚組分的芳香環上有間位定位基存在時,重排一般不能發生。
這個方法是在酚的芳環上引入酰基的重要方法。
反應機理
[編輯]弗賴斯重排的機理至今仍未完全清楚,可能有時為分子內的反應,而從交叉實驗結果來看可能有時又為分子間的反應。一個接受較廣的機理是下圖所示涉及碳正離子的機理。

該機理中,首先是酚酯的羰基氧與路易斯酸性的鋁原子進行配位。然後鋁基重排到酚氧上,C-O 鍵斷裂,產生酚基鋁化物和酰基正離子。酰基正離子接下來在苯環上酚基的鄰位或對位對其發生親電芳香取代,再經水解得到產物羥基芳酮。
光弗賴斯重排
[編輯]弗賴斯重排也可以在沒有催化劑的情況下進行,但需要有紫外光的存在。產物仍然是鄰或對羥基芳酮。這種類型的弗賴斯重排稱為「光弗賴斯重排」。[4]
光弗賴斯重排產率很低,很少用於合成。不過苯環上連有間位定位基時仍然可以進行光弗賴斯重排。
光弗賴斯重排反應為自由基機理,首先是酚酯分子被光激發,激發態的酚酯在溶劑籠中均裂為一對酚基和酰基自由基,然後酰基自由基再從鄰位或對位與酚基自由基偶聯,並經互變異構得到產物羥基芳酮。
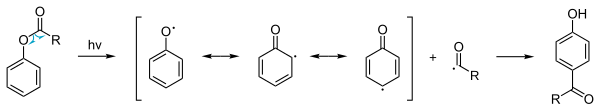
酚是光弗賴斯重排的常見產物,它是由酚基自由基從溶劑籠中脫離,並從其他分子中奪取氫原子生成的。
研究顯示光弗賴斯重排是以聚對苯二甲酸乙二酯(PET)製成的塑料瓶,在~40°C 和波長為 310nm 的紫外光照射下發生降解的機理之一。(這個條件類似於天氣炎熱時塑料瓶的降解條件)[5]
光弗賴斯重排的一個有趣的應用是乙醇中的碳酸雙(對叔丁基苯)酯在光照射下的雙重排,產生雙(5-叔丁基-2-羥基苯基)甲酮。[6]
陰離子弗賴斯重排
[編輯]陰離子弗賴斯重排指的是通過 α-鹵代芳酯金屬化引發的弗賴斯重排。
參見
[編輯]參考資料
[編輯]- ^ Fries, K. ; Finck, G. Über Homologe des Cumaranons und ihre Abkömmlinge. Chemische Berichte. 1908, 41 (3): 4271–4284. doi:10.1002/cber.190804103146.
- ^ Fries, K.; Pfaffendorf, W. Über ein Kondensationsprodukt des Cumaranons und seine Umwandlung in Oxindirubin. Chemische Berichte. 1910, 43 (1): 212–219. doi:10.1002/cber.19100430131.
- ^ March, J. Advanced Organic Chemistry, 3rd Ed.; John Wiley & Sons: Chichester, 1985; S. 499ff.
- ^ Bellus, D. Advances in Photochemistry; John Wiley & Sons: Chichester, 1971; Vol. 8, 109–159.
- ^ Norma Searle, "Environmental effects on polymeric materials," pp. 313-358, in Plastics and the Environment, edited by Anthony Andrade, Wiley, 2003.
- ^ W. M. Horspool and P. L. Pauson. The photochemical decomposition of some aryl esters. J. Chem. Soc. 1965: 5162–5166. doi:10.1039/JR9650005162.
