苯三羰基鉻
外觀
| (Benzene)chromium(0) tricarbonyl | |||
|---|---|---|---|
| |||
| IUPAC名 (benzene)tricarbonylchromium | |||
| 別名 | 三羰基(苯)鉻 | ||
| 識別 | |||
| CAS號 | 12082-08-5 | ||
| PubChem | 10954891 | ||
| ChemSpider | 9130108 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | WVSBQYMJNMJHIM-UHFFFAOYAR | ||
| 性質 | |||
| 化學式 | Cr(C6H6)(CO)3 | ||
| 摩爾質量 | 214.14 g/mol g·mol⁻¹ | ||
| 外觀 | 黃色晶體 | ||
| 熔點 | 163 - 166 °C | ||
| 溶解性(水) | 難溶 | ||
| 溶解性 | THF, 乙醚, 苯 | ||
| 結構 | |||
| 配位幾何 | tetrahedral, "piano stool" | ||
| 危險性 | |||
GHS危險性符號
| |||
| GHS提示詞 | Warning | ||
| H-術語 | H302, H312, H332 | ||
| P-術語 | P261, P264, P270, P271, P280, P301+312, P302+352, P304+312, P304+340, P312, P322, P330, P363, P501 | ||
| 主要危害 | Harmful through inhalation, contact with skin, or swallowed | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
苯三羰基鉻是一種金屬有機化合物,化學式為Cr(C6H6)(CO)3,它是黃色晶體,可溶於常見的非極性有機溶劑。它最初於1957年由Fischer和Öfele報道,他們通過二苯鉻的羰基化反應製備。[1]
- Cr(CO)6 + C6H6 → Cr(C6H6)(CO)3 + 3 CO
它的苯環比苯本身更親電,可以發生親核加成反應:[2]
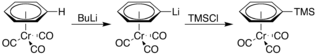
其酸性也更強,鋰化後可以進行一系列反應:
參考文獻
[編輯]- ^ Fischer, Ernst Otto; Őfele, Karl. (1957). 「Über Aromatenkomplexe von Metallen, XIII Benzol-Chrom-Tricarbonyl,」 Chemische Berichte, 90, 2532-5. doi:10.1002/cber.19570901117.
- ^ Herndon, James W; Laurent, Stéphane E. (2008). 「(η6-Benzene)tricarbonylchromium,」 in Encyclopedia of Reagents for Organic Synthesis, John Wiley & Sons, Chichester, 2008. doi:10.1002/047084289X.rb025.pub2. Article Online Posting Date: March 15, 2009
| |||||||||||||||||||||||||||||||||||||||||