乙二醇
外观
此條目需要擴充。 (2011年5月21日) |
| 乙二醇 | |
|---|---|

| |
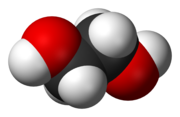
| |
| IUPAC名 Ethane-1,2-diol | |
| 别名 | 乙撑亚胺 MEG 1,2-乙二醇 |
| 识别 | |
| CAS号 | 107-21-1 |
| SMILES |
|
| 性质 | |
| 化学式 | C2H4(OH)2 |
| 摩尔质量 | 62.068 g·mol⁻¹ |
| 密度 | 1.1132 |
| 熔点 | −12.9 °C (8.8 °F) |
| 沸点 | 197.3 °C (387 °F) |
| 溶解性(水) | 与水以任意比互溶 |
| 危险性 | |
| 闪点 | 111 °C (closed cup) |
| 自燃温度 | 410 °C |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
乙二醇,又名甘醇。化学式HOCH2—CH2OH。一种简单的二元醇。无色无臭、有甜味液体,能与水以任意比例混合。用作溶剂、防冻剂以及PET等的原料。
乙二醇對動物有毒性,人類致死劑量估計為1.6 g/kg,[1]不過成人服食30毫升已有可能引致死亡。[2]
制备
乙二醇可由乙烯透過反应中间体环氧乙烷產生。環氧乙烷與水的反應產生乙二醇的化學反應式如下:
- C2H4O + H2O → HO–CH2CH2–OH
此反應可由酸或鹼的催化下加速反應,或在中性pH值條件下提高的溫度也可以加速反應。乙二醇最高的產率發生在酸性或中性pH下與大量過量的水,在這條件下,乙二醇的產量可達90%。主要的副產物是屬於乙二醇低聚物的 二甘醇、三甘醇、四甘醇。每年生產約六十七億公斤。 有一個選擇性較高的方式是使用OMEGA process。反應式為:
- C2H4O + CO2 → C3H4O3
- C3H4O3 + H2O → HOC2H4OH + CO2
在OMEGA process中,第一步驟:環氧乙烷先與二氧化碳轉變成碳酸乙烯酯(Ethylene carbonate)第二步驟:碳酸乙烯酯(Ethylene carbonate)與水反應,選擇性地產生乙二醇單體。在第二步驟被釋放的二氧化碳,可以回饋到第一步驟再使用。[3]
毒性
乙二醇的毒性不高,目前已知對人類的最低致死劑量LDLO為786毫克/公斤。[4]乙二醇最大的危險性在於它的甜味。因此相較於其他有毒物質,孩童和動物比較容易因攝取大量的乙二醇而中毒。經過消化系統作用,乙二醇會先被氧化成乙醇酸,再被氧化成草酸。草酸及其副產物會先影響中樞神經系統,接著是心臟,而後影響腎臟。如無適當治療,攝取過量乙二醇會導致死亡。[5]
根據美國毒物管制中心2007年的資料,當年有大約1000起乙二醇中毒事件且其中有16人死亡。2008年則有7人死於乙二醇中毒。(Toxicity, Ethylene Glycol)
生活環境中的乙二醇
- 生活環境中的乙二醇主要來自於機場的用來除冰的除冰劑或其他含有乙二醇的產品。
- 乙二醇在大氣中自然分解的時間大約為10天。
- 水中或土壤中的乙二醇則需大約幾個星期才會分解。[6]
參考資料
- ^ http://mtcc.vghtc.gov.tw/intrChemicalAidCont.asp?CasNo=107-21-1
- ^ Field D. Acute ethylene glycol poisoning. Crit Care Med. 1985, 13 (10): 872–3. PMID 4028762.
- ^ Siegfried Rebsdat; Dieter Mayer (2005), "Ethylene Glycol", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi: 10.1002/14356007.a10_101
- ^ Safety Officer in Physical Chemistry. Safety (MSDS) data for ethylene glycol. Oxford University. November 23, 2009 [December 30, 2009].
- ^ Ethylene glycol. National Institute for Occupational Safety and Health. Emergency Response Database. August 22, 2008. Retrieved December 31, 2008.
- ^ (CDC ToxFAQs)
