草酸亚铁
外观
| 草酸亚铁 | |
|---|---|

| |
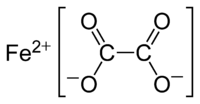
| |
| 英文名 | Ferrous oxalate Iron(II) oxalate |
| 别名 | 草酸铁(II) |
| 识别 | |
| CAS号 | 516-03-0 6047-25-2((dihydrate)) |
| PubChem | 10589 |
| SMILES |
|
| EINECS | 208-217-4 |
| 性质 | |
| 化学式 | FeC2O4 |
| 摩尔质量 | 143.86 g/mol(无水) 179.89 g/mol(二水) g·mol⁻¹ |
| 外观 | 黄色晶体(二水)[1] |
| 氣味 | 无味 |
| 密度 | 2.28 g·cm-3 |
| 熔点 | 200-275℃(无水,分解) 120-170℃(二水,失水) |
| 溶解性(水) | 0.097 g/100ml(二水,25℃) |
| 危险性 | |
| 警示术语 | R:R21/22 |
| 安全术语 | S:S24/25 |
| 欧盟分类 | |
GHS危险性符号 [2] [2]
| |
| GHS提示词 | Warning |
| H-术语 | H302, H312[2] |
| P-术语 | P280[2] |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
草酸亚铁(化学式:FeC2O4)是铁(II)的草酸盐,黄色晶体,难溶于水,缓慢溶于浓盐酸。[3]
制备
[编辑]草酸亚铁可由Fe2+与C2O42-在溶液中的反应制得:[4]
- Fe2+ + C2O42- → FeC2O4↓
如将硫酸酸化的硫酸亚铁铵和草酸溶液混合,加热并搅拌,静置后倒出上层清液,分别用蒸馏水和丙酮洗涤沉淀,干燥,得到草酸亚铁二水合物晶体。[5]
化学性质
[编辑]草酸亚铁可溶于碱金属草酸盐溶液中,形成[Fe(C2O4)2]2-。[4]
加热草酸亚铁固体,可以得到纳米铁粉。该粉末可以在空气中自燃。[6]
- FeC2O4 → Fe + 2 CO2↑
加热草酸亚铁二水合物,其分解反应分为三步,首先是结晶水的脱除:[1]
- FeC2O4·2H2O → FeC2O4 + 2 H2O
第二步是脱去CO:
- FeC2O4 → FeCO3 + CO↑
第三步是FeCO3的分解:
- FeCO3 → FeO + CO2↑
此外,当H2O来不及扩散时,存在以下副反应:
- 3 FeO + H2O → Fe3O4 + H2
用途
[编辑]参考文献
[编辑]- ^ 1.0 1.1 方正东, 汪敦佳. 二水草酸亚铁热分解行为及脱水反应动力学研究 (页面存档备份,存于互联网档案馆). 无机化学学报, 2005, 21(11):1682-1686
- ^ 2.0 2.1 2.2 来源:Sigma-Aldrich Co., Iron(II) oxalate dihydrate (2014-05-03查阅).
- ^ 朱文祥. 无机化合物制备手册. 化学工业出版社, 2006. pp 516
- ^ 4.0 4.1 谢高阳 等. 无机化学丛书 第九卷 锰分族 铁系 铂系. 科学出版社, 2011. pp 173 羧酸铁(II)
- ^ 5.0 5.1 孙悦, 乔庆东. 合成草酸亚铁的反应时间对组成的影响. 辽宁石油化工大学学报, 2005, 25(4):1-4
- ^ 赵维元. 纳米铁粉的制备及应用研究. 高中数理化, 2015(16): 61-62
- ^ Andre AngermannJörg Töpfer. Synthesis of magnetite nanoparticles by thermal decomposition of ferrous oxalate dihydrate. J. J Mater Sci (2008) 43: 5123. doi:10.1007/s10853-008-2738-3
- ^ Xiangqian Fan, et al. α-Ferrous oxalate dihydrate: a simple coordination polymer featuring photocatalytic and photo-initiated Fenton oxidations. Sci China Mater 2016, 59(7): 574–580
