信号转导

信号转导(英语:signal transduction)又称讯息传导、讯息传递,是化学或物理信号(讯息)通过一系列分子转变及传递至细胞的过程,最常见的是蛋白激酶催化的蛋白质磷酸化,最终导致细胞反应。
负责检测刺激的蛋白质通常称为“受体”,但依语境有时称“传感器”。[1]受体与配体结合(或信号传感)引起的变化产生信号级联(signaling cascade),其为沿信号传导途径的生物化学事件链。当信号通路彼此相互作用时,它们形成网络,通常通过组合信号传导事件来协调细胞反应。[2]在分子水平上,此类反应包括基因转录或翻译的变化,蛋白质的翻译后和构象变化,以及它们的位置变化。这些分子事件是控制细胞生长,增殖,代谢和许多其他过程的基本机制。[3]在多细胞生物中,信号转导途径已经进化到以多种方式调节细胞通讯。
信号通路的每个组件(或节点)根据其相对于初始刺激所起的作用进行分类。配体被称为第一信使,而受体是信号传感器,然后激活初级效应器。这种效应器通常与第二信使相关联,第二信使可以激活次级效应器,等等。根据节点的效率,可以放大信号(称为信号增益的概念),这样一个信号分子就可以产生涉及数百个到数百万个分子的响应[4]。与其他信号一样,生物信号的转导的特征是延迟,噪声,信号反馈和前馈和干扰,其范围可以从可忽略到病态[5]。随着计算生物学的出现,信号通路和网络的分析已经成为理解细胞功能和疾病的重要工具,包括发信号通知对获得性耐药性反应的重新布线机制。[6]

刺激
[编辑]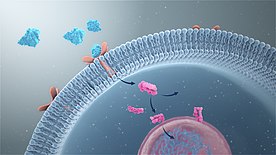
信号转导的基础是将某种刺激转化为生化信号。 这种刺激的性质可以有很大的不同,例如细胞外的信号(例如EGF的存在)以及细胞内的事件(例如复制性端粒磨损导致的DNA损伤)都属于刺激[7]。 传统上,到达中枢神经系统的信号被归类为感官感觉。 这些在称为突触传递的过程中从一个神经元传递到另一个神经元。 许多其他细胞间信号传递机制存在于多细胞生物中,例如控制胚胎发育的那些[8]。
受体
[编辑]受体大致可分为两大类:细胞内受体和细胞外受体。
第二信使
[编辑]第一信使是从细胞外液到达细胞并与其特定受体结合的信号分子(激素、神经递质和旁分泌/自分泌剂)。 第二信使是进入细胞质并在细胞内起作用以触发反应的物质。 实质上,第二信使充当从质膜到细胞质的化学中继器,从而进行细胞内信号转导。
参阅
[编辑]参考资料
[编辑]- ^ Bradshaw, Ralph A.; Dennis, Edward A., eds. (2010). Handbook of Cell Signaling (2nd ed.). Amsterdam, Netherlands: Academic Press. ISBN 9780123741455.
- ^ Papin, Jason A.; Hunter, Tony; Palsson, Bernhard O.; Subramaniam, Shankar (14 January 2005). "Reconstruction of cellular signalling networks and analysis of their properties". Nature Reviews Molecular Cell Biology. 6 (2): 99–111. doi:10.1038/nrm1570. PMID 15654321.
- ^ Krauss, Gerhard (2008). Biochemistry of Signal Transduction and Regulation. Wiley-VCH. p. 15. ISBN 978-3527313976.
- ^ Reece, Jane; Campbell, Neil (2002). Biology. San Francisco: Benjamin Cummings. ISBN 0-8053-6624-5.
- ^ Kolch, Walter; Halasz, Melinda; Granovskaya, Marina; Kholodenko, Boris N. (20 August 2015). "The dynamic control of signal transduction networks in cancer cells". Nature Reviews Cancer. 15 (9): 515–527. doi:10.1038/nrc3983. PMID 26289315.
- ^ Bago R, Sommer E, Castel P, Crafter C, Bailey FP, Shpiro N, Baselga J, Cross D, Eyers PA, Alessi DR (2016) The hVps34-SGK3 pathway alleviates sustained PI3K/Akt inhibition by stimulating mTORC1 and tumour growth. EMBO Journal 35:1902-22
- ^ Smogorzewska A, de Lange T. Different telomere damage signaling pathways in human and mouse cells. The EMBO Journal. August 2002, 21 (16): 4338–48. PMC 126171
 . PMID 12169636. doi:10.1093/emboj/cdf433.
. PMID 12169636. doi:10.1093/emboj/cdf433.
- ^ Lawrence PA, Levine M. Mosaic and regulative development: two faces of one coin. Current Biology. April 2006, 16 (7): R236–9. PMID 16581495. doi:10.1016/j.cub.2006.03.016
 .
.
