叔丁基亞磺酰胺
外觀
| 叔丁基亞磺酰胺 左:R型體,右:S型體 | |||
|---|---|---|---|
| |||

| |||
| IUPAC名 2-甲基丙烷-2-亞磺酰胺 2-Methylpropane-2-sulfinamide | |||
| 別名 | 特丁基亞磺酰、2-甲基-2-丙烷亞磺酰胺、埃爾曼亞磺酰胺 | ||
| 識別 | |||
| CAS號 | 146374-27-8((R/S)) 196929-78-9((R)-(+)) 343338-28-3((S)-(-)) | ||
| PubChem | 3382465((R/S)) 10964479((R)-(+)) 11355477((S)-(-)) | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | CESUXLKAADQNTB-UHFFFAOYSA-N | ||
| 性質 | |||
| 化學式 | C4H11NOS | ||
| 摩爾質量 | 121.2 g·mol−1 | ||
| 外觀 | 白色或淡黃色固態 | ||
| 熔點 | 102 -105 °C(270 K) | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
叔丁基亞磺酰胺(英語:tert-Butanesulfinamide),學名2-甲基-2-丙烷亞磺酰胺,俗稱埃爾曼亞磺酰胺(英語:Ellman's sulfinamide),是一種含硫有機化合物,屬亞磺酸酰胺類化合物。兩種對應異構體均有市售,並常用作不對稱合成的手性助劑,特別是用於合成手性銨鹽或胺[1][2][3]。叔丁基亞磺酰胺以及相關的合成方法由喬納森·A·埃爾曼(Jonathan A. Ellman)等人在1997年提出[4],因此該化合物又稱為埃爾曼亞磺酰胺。
對映純合成
[編輯]對映純級的叔丁基亞磺酰胺可以由廉價的叔丁基二硫經過立體選擇性氧化成硫代亞磺酸酯,再利用氨基鋰使二硫鍵斷裂得到。其第一步立體選擇性氧化過程用到了乙酰丙酮氧釩(IV)和有機手性配體,該有機手性配體由3,5-二叔丁基水楊醛與光譜純的手性氨基茚滿醇縮合得到。
 |
| 叔丁基亞磺酰胺合成路線 |
|---|
手性胺合成
[編輯]叔丁基亞磺酰胺與酮和醛縮合生成對應的N-叔丁基亞磺酰酮亞胺和N-叔丁基亞磺酰醛亞胺。這類亞胺比一般亞胺更耐水解,但更容易與親核試劑反應。當親核試劑(Nu-)與這類亞胺雙鍵發生非對應選擇性加成,叔丁基亞磺酰基起到手性助劑的作用。叔丁基亞磺酰基同時也起到的保護基的作用。與鹽酸反應即可去掉叔丁基亞磺酰基,形成對應的手性銨鹽、手性胺(採用醛為起始原料)或手性仲胺(採用酮為起始原料)
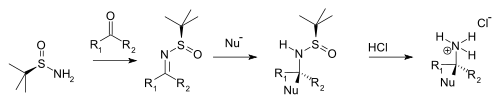 |
| 叔丁基亞磺酰胺的手性胺合成 |
|---|
富蘭克林·A·戴維斯在此基礎上還開發出以亞磺酰亞胺為中間體的不對稱合成胺類化合物的方法[5]。
運用
[編輯]在抗過敏藥西替利嗪的不對稱合成中(手性體比外消旋體藥效更強),就用到了叔丁基亞磺酰胺作為手性助劑。採用4-氯苯甲醛與叔丁基亞磺酰胺縮合得到對應的N-叔丁基亞磺酰醛亞胺,然後與苯基溴化鎂加成得到關鍵的手性中心[6]。
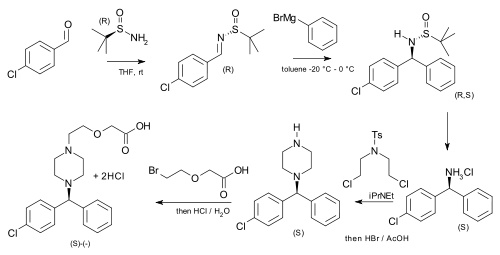 |
| 西替利嗪的不對稱合成 |
|---|
參考文獻
[編輯]- ^ Ellman, J. A. Applications of tert-butanesulfinamide in the asymmetric synthesis of amines. Pure and Applied Chemistry. 2003, 75: 39–46. S2CID 97201636. doi:10.1351/pac200375010039
 .
.
- ^ Robak, Maryann T.; Herbage, Melissa A.; Ellman, Jonathan A. Synthesis and Applications oftert-Butanesulfinamide. Chemical Reviews. 2010, 110 (6): 3600–740. PMID 20420386. doi:10.1021/cr900382t.
- ^ Organic Syntheses, Vol. 82, p.157 (2005). Link
- ^ Liu, Guangcheng; Cogan, Derek A.; Ellman, Jonathan A. Catalytic Asymmetric Synthesis of tert-Butanesulfinamide. Application to the Asymmetric Synthesis of Amines. Journal of the American Chemical Society. 1997, 119 (41): 9913. doi:10.1021/ja972012z.
- ^ Davis, Franklin A.; Reddy, Rajarathnam E.; Szewczyk, Joanna M.; Reddy, G. Venkat; Portonovo, Padma S.; Zhang, Huiming; Fanelli, Dean; Zhou, Ping; et al. Asymmetric Synthesis and Properties of Sulfinimines (ThiooximeS-Oxides). The Journal of Organic Chemistry. 1997, 62 (8): 2555–2563. PMID 11671597. doi:10.1021/jo970077e.
- ^ Pflum, D; Krishnamurthy, D; Han, Z; Wald, S; Senanayake, C. Asymmetric synthesis of cetirizine dihydrochloride. Tetrahedron Letters. 2002, 43 (6): 923. doi:10.1016/S0040-4039(01)02294-8.


