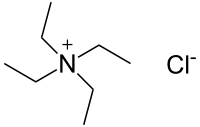
四乙基氯化銨
外觀
| 四乙基氯化銨 | |
|---|---|
| |
| IUPAC名 N,N,N-Triethylethanaminium chloride | |
| 別名 | 氯化四乙基銨 |
| 識別 | |
| CAS號 | 56-34-8 |
| PubChem | 5946 |
| ChemSpider | 5733 |
| SMILES |
|
| InChI |
|
| InChIKey | YMBCJWGVCUEGHA-REWHXWOFAF |
| ChEBI | 78161 |
| 性質 | |
| 化學式 | C8H20ClN |
| 摩爾質量 | 165.7 g·mol−1 |
| 外觀 | 無色潮解固體 |
| 密度 | 1.08 g/cm3[1] |
| 熔點 | 360 °C(633 K)(四水[1]) |
| 溶解性(水) | 極易溶 |
| 危險性 | |
| 致死量或濃度: | |
LD50(中位劑量)
|
65 mg/kg(小鼠,腹膜注射) 900 mg/kg(小鼠,口服) |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
四乙基氯化銨,簡稱TEAC,是一種季銨鹽,化學式 (C2H5)4N+Cl−,有時寫作Et4N+Cl−。它是吸濕性的無色晶體。在藥理學和生理學研究中,它已被用作四乙基銨陽離子的來源,也用於有機化學合成。
製備和結構
[編輯]TEAC可以由三乙胺和氯乙烷反應而成。[2]
TEAC有兩種穩定的水合物,分別是一水合物和四水合物。[3]一水合物TEAC.H2O 的晶體結構已確定,[4] 四水合物TEAC.4H2O也是如此。[5]
Harmon和Gabriele提供了製備大量TEAC.H2O晶體的詳細信息,他們對該化合物和相關化合物進行了紅外光譜學研究。[6]研究人員也指出,儘管剛提純的 TEAC.H2O 不含三乙胺鹽酸鹽,但加熱TEAC時會通過霍夫曼消除反應產生少量的三乙胺鹽酸鹽。
- Cl− + H-CH2-CH2-N+Et3 → Cl-H + H2C=CH2 + Et3N
合成應用
[編輯]在很大程度上,TEAC的合成應用類似於四乙基溴化銨(TEAB)和四乙基碘化銨(TEAI),儘管其中一種鹽在特定反應中可能比另一種更有效。舉個例子,TEAC在從芳胺、硝基芳烴和一氧化碳製備二芳基脲的反應中作為助催化劑的產率比TEAB和TEAI高。[7]
在其他示例中,例如以下示例,TEAC不如TEAB或TEAI有效:
- 通過羧酸的碳酸乙烯酯和某些帶有酸性N-H的雜環化合物進行2-羥乙基化(-CH2-CH2-OH基團的連接)。[8]
- 相轉移催化劑在芴的偕二烷基化中,以及氫氧化鈉和鹵代烷烴水溶液進行苯胺的N,N-二烷基化和咔唑的N-烷基化。[9]
生物學
[編輯]與四乙基溴化銨和四乙基碘化銨一樣,TEAC已被用作許多臨床和藥理學研究的四乙基銨離子來源,在四乙基銨鹽條目下有更詳細的介紹。簡而言之,TEAC的神經節阻滯特性已在臨床上進行了探索。[10]雖然它現在作為藥物基本上已經過時,但它仍然用於生理研究,因為它能夠阻斷各種組織中的 K+ 通道。[11][12]
毒性
[編輯]TEAC的毒性是由四乙基銨陽離子導致的,這已被廣泛研究。TEAC的急性毒性可以和四乙基溴化銨和四乙基碘化銨比較。這些數據[13]是用於比較目的,詳細信息可在四乙基銨鹽條目中找到。
參見
[編輯]參考資料
[編輯]- ^ 1.0 1.1 The Merck Index, 10th Ed., p.1316, Rahway: Merck & Co.
- ^ Roose, Peter; Eller, Karsten; Henkes, Erhard; Rossbacher, Roland; Höke, Hartmut, Amines, Aliphatic, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, 2005, doi:10.1002/14356007.a02_001.pub2
- ^ K. M. Harmon, J. M. Gabriele and J. Harmon (1990). "Hydrogen bonding Part 30. New IR spectra-structure correlations for tetraethylammonium, tetramethylammonium, and N,N-dimethyl-pyrrolidinium fluoride monohydrates, tetraethylammonium chloride monohydrate, and tetramethylammonium hydroxide dihydrate; evidence for a planar (H2O.F−)2 cluster". J. Mol. Struct. 216 53-62.
- ^ J. H. Loehlin and A. Kvick (1978). "Tetraethylammonium chloride monohydrate". Acta Crystallographica Section B 34 3488–3490.
- ^ Y.-S. Lam and T. C. W. Mak (1978). "Crystal data for some tetraethylammonium salt hydrates". 11 193.
- ^ Harmon, Kenneth M.; Gabriele, Julie M. Hydrogen bonding. 11. Infrared study of the water-chloride ion cluster in tetraethylammonium chloride hydrate. Inorganic Chemistry. 1981, 20 (11): 4013–4015. doi:10.1021/ic50225a087.
- ^ H. A. Dieck, R. M. Laine and R. F. Heck (1975). "Low-pressure, palladium-catalyzed N,N'-diarylurea synthesis from nitro compounds, amines, and carbon monoxide". J. Org. Chem. 40 2819–2822.
- ^ T.Yoshino et al. (1977). "Synthetic studies with carbonates. Part 6. Syntheses of 2-hydroxyethyl derivatives by reactions of ethylene carbonate with carboxylic acids or heterocycles in the presence of tetraethylammonium halides or under autocatalytic conditions". J. Chem. Soc., Perkin 1 1266–1272.
- ^ G. Saikia and P. K. Iyer (2010). "Facile C-H alkylation in water: enabling defect-free materials for optoelectronic devices". J. Org. Chem. 75 2714–2717.
- ^ G. K. Moe and W. A. Freyburger (1950). "Ganglionic blocking agents". Pharmacol. Rev. 2 61–95.
- ^ B. Hille (1967). "The selective inhibition of delayed potassium currents in nerve by tetraethylammonium ions". J. Gen. Physiol. 50 1287–1302.
- ^ C. M. Armstrong and B. Hille (1972). "The inner quaternary ammonium receptor in potassium channels of the node of Ranvier". J. Gen. Physiol. 59 388–400.
- ^ O. M. Gruhzit, R. A. Fisken and B. J. Cooper (1948). "Tetraethylammonium chloride [(C2H5)4NCl]. Acute and chronic toxicity in experimental animals". J. Pharmacol. Exp. Ther. 92 103–107.
