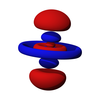
d2sp2混成
外觀
| d2sp2雜化 | |
|---|---|
| d2sp2雜化後的電子軌道排布 (以鎢元素為例) | |
| 參與d2sp2雜化的原子軌道 | |
| s軌道 | 1個 |
| p軌道 | 2個 |
| d軌道 | 2個 |
| 含有採用d2sp2雜化原子的分子或離子 | |
| 其他 | VO(acac)2[1]、W(CO)5[2] |
d2sp2雜化(英語:d2sp2 hybridization)是指一個原子內的兩個n-1d軌道、一個ns軌道和兩個np軌道發生雜化的過程。原子發生d2sp2雜化後,上述n-1d軌道、ns軌道和np軌道便會轉化成為五個雜化軌道,稱為「d2sp2雜化軌道」。五個d2sp2雜化軌道分別存在於兩個平面上,其中,位於水平面的四個雜化兩兩之間的夾角皆為90°,另有一個雜化軌道位於軸向平面、垂直於其餘四個雜化軌道。一般認為d2sp2雜化的水平雜化軌道是由dx²-z²、s、px和py軌道組成的,而軸向雜化軌道則由dz²和pz組成。d2sp2雜化一般發生在分子形成過程中。雜化過程中,能量相近的d軌道、s軌道和p軌道發生疊加,不同類型的原子軌道重新分配能量並調整方向。
參考文獻
[編輯]- ^ 配合物的化学键理论:杂化轨道与空间构型的关系 (PDF). 配位化學. [2012-01-30]. (原始內容 (PDF)存檔於2016-03-04) (中文).
- ^ Gerard Daniël Rieck. Properties of Compounds. Tungsten and its compounds. Pergamon Press. 1967: 85 (英語).

![{\displaystyle W^{*}\,[Xe]5d^{6}{\frac {\color {White}/}{(d^{2}sp^{2})^{5}}}{\frac {\color {White}/}{6p}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/bde7eb98355583b5958199844ef86a0c18e5c6af)