普林斯反應
普林斯反應(Prins reaction)是一種將醛或酮與烯烴或炔烴在酸催化下進行的縮合反應[1][2][3]。
此反應可用於製取二噁烷(與過量甲醛、低溫)、1,3-二醇(與甲醛、水和質子酸)、烯丙醇(無水情況下失水)、氯代醇(與氯離子)和酯(與乙酸)等化合物。其中關鍵性的中間體是質子化的羰基化合物對烯烴的親電加成所生成的碳正離子中間體。

歷史
[編輯]1919年,荷蘭化學家 Hendrik Jacobus Prins 發表了以苯乙烯(下圖)、蒎烯、莰烯、丁香酚、異黃樟素和茴香腦為原料的 Prins 反應。

1937年,有人研究了利用甲醛與異丁烯的 Prins 反應並失水以製取異戊二烯(作為合成橡膠原料)的反應。

反應機理
[編輯]質子化的羰基化合物——氧鎓離子作為親電試劑與烯烴發生親電加成,生成關鍵性的碳正離子中間體 (4),它受到分子內羥基氧的鄰基參與作用而得到穩定。

該碳正離子接下來有多種轉化方式,而這也是反應產物多樣性的來源。
- 藍色:碳正離子被水或其他親核試劑捕獲,最終生成1,3-加成物(6)。
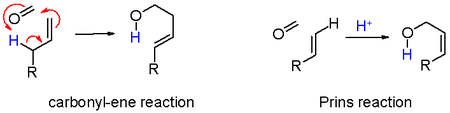
- 黑色:碳正離子的鄰位碳質子被奪取,從而發生消除,生成不飽和化合物(7)。當原料烯烴有未取代烯碳時,其與羰基化合物的加成以及其後的消除步驟可以協同進行,烯丙位的氫經羰基-ene反應而轉變為產物中的羥基氫。
- 綠色:碳正離子被另一分子羰基化合物所捕獲,經正離子中間體(8)(其中正電荷分散在氧和碳原子上),再關環,去質子化,得到最終產物二氧六環(10)。此路線的一個例子是從苯乙烯合成4-苯基-1,3-二氧六環。[4]
- 灰色:特定條件下,非常穩定的碳正離子中間體可以發生分子內環化產生噁丁環衍生物(12),類似於Paterno-Büchi 光化學反應。
變體
[編輯]1、鹵代 Prins 反應:用路易斯酸(如四氯化錫或三溴化硼)代替質子酸和水,以鹵離子作為親核試劑捕獲反應中的碳正離子中間體,得到鹵代醇。
例如,某些烯丙基胡薄荷酮在路易斯酸催化下在二氯甲烷中發生環化,可用於構建十氫萘環系。以四氯化鈦催化在−78°C環化,可生成三氯化鈦-烷氧負離子中間體並發生氯離子與碳正離子的同面捕獲,從而以高非對映選擇性(91% cis)得到順式產物。相反,以四氯化錫催化於室溫下環化,則主要(98% trans)生成反式產物。[5]

2、串聯 Prins-嚬哪醇重排:二甲縮醛(掩蔽的羰基化合物)與三異丙基矽基醚(掩蔽的醇)在四氯化錫催化之下產生的 Prins 產物再發生 pinacol 重排,用於構建五元環化合物(以及螺環化合物)。[6]

應用
[編輯]1、用於 Exiguolide 的全合成:[7]

參考資料
[編輯]- ^ Condensation of formaldehyde with some unsaturated compounds H. J. Prins, Chemisch Weekblad, 16, 64, 1072, 1510 1919
- ^ Chemical Abstracts 13, 3155 1919
- ^ The Olefin-Aldehyde Condensation. The Prins Reaction. E. Arundale, L. A. Mikeska Chem. Rev.; 1952; 51(3); 505-555. Link (頁面存檔備份,存於互聯網檔案館)
- ^ 4-Phenyl-m-dioxane R. L. Shriner and Philip R. Ruby Organic Syntheses, Coll. Vol. 4, p.786 (1963); Vol. 33, p.72 (1953). Article (頁面存檔備份,存於互聯網檔案館)
- ^ R. Brandon Miles, Chad E. Davis, and Robert M. Coates. Syn- and Anti-Selective Prins Cyclizations of ,-Unsaturated Ketones to 1,3-Halohydrins with Lewis Acids. J. Org. Chem. 2006, 71 (4): 1493–1501. doi:10.1021/jo052142n.
- ^ Larry E. Overman and Emile J. Velthuisen. Scope and Facial Selectivity of the Prins-Pinacol Synthesis of Attached Rings. J. Org. Chem. 2006, 71 (4): 1581–1587. doi:10.1021/jo0522862.
- ^ Min Sang Kwon, Sang Kook Woo, Seong Wook Na, and Eun Lee. Total Synthesis of (+)-Exiguolide. Angew. Chem. Int. Ed. 2008, 47: 1733–1735. doi:10.1002/anie.200705018.
外部連結
[編輯]- Prins reaction in Alkaloid total synthesis Link[失效連結]
- Prins reaction @ organic-chemistry.org (頁面存檔備份,存於互聯網檔案館)
