溶劑效應
溶劑效應是指溶劑所產生的一連串化學反應,會影響主要化學反應的反應速率、反應平衡、溶解度、穩定性甚至是反應機理;換而言之,化學反應中的熱力學和動力學可藉由選擇適當溶劑來控制。
溶質在溶劑中溶解時會與溶劑產生相互作用,其過程稱為「溶劑化(solvation)」,取決於雙方(指溶質和溶劑)的自由能 (free energy)變化,而自由能在反應中受多個因素影響。
進行溶劑效應的靜態模擬時,我們將焦點放在溶劑效應的兩個主要作用上:一是短程作用,是指溶劑和溶質分子的反應中心所產生的相互作用(如:配位鍵、氫鍵的形成等);另一個是遠程作用,極性溶劑、溶質分子兩個偶極距間的靜電相互作用。
在進行靜態模擬可使用的三種溶解模型[1]:
- 微觀溶解模型(Micro solvation Model):模擬在反應過程裏短程作用較重要的反應,直接模擬溶液中溶劑分子和溶質反應中心的作用。
- 內隱溶劑模型(Implicit solvent model):某些化學反應無短程作用,此時我們可利用此模型模擬其遠程作用;將溶劑效應視為分佈在連續介質中的溶質分子。
- 將溶劑的短程作用和遠程作用皆列為考慮條件,並結合微觀溶解模型(micro solvation model)和內隱溶劑模型(Implicit solvent model)的模擬方法提升靜態模擬的準確度,近年來漸漸爲人們所青睞。
短程作用的模擬,大多採用QM法(QM methods),研究溶劑分子的活性中心,考慮鍵的生成對反應區域和反應過渡態結構和能量的影響。
遠程作用需要考慮較多變因,故需要藉助物理模型來做近似處理;連續介質(Continuum)模型有很多,其中常用的是極化連續介質模型(Polarized Continuum Model, PCM)。PCM最早於1981年由Tomasi教授(意大利比薩大學)提出 [2]。
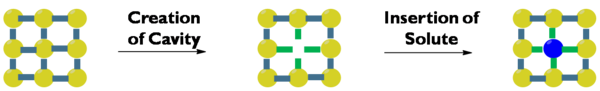
溶劑效應涉及到三個概念溶劑空腔形成(cavity formation)、分散排斥(dispersion-repulsion)和靜電交互作用(electrostatic interaction)[3]
- 溶劑空腔形成(cavity formation):在連續的介質中騰出空腔(cavity)以容納溶質,藉以提升整個系統能量,所提升的能量稱爲空腔能量(cavity formation energy)。
- 分散排斥(dispersion-repulsion):溶質和溶劑在空腔裏所產生的相互作用,會使整個系統能量下降,故一般為負值;其主作用力為凡得瓦力(van der Waals' force),並且不包括靜電作用力。
- 靜電交互運用(electrostatic interaction):溶質分子的電荷分佈會因為靜電的相互作用(electrostatic energy)使連續介質(溶劑)産生極化現象,而溶劑極化則反過來影響溶質分子的電荷分佈,相互作用的過程會使系統能量下降。[4]。
以上三大概念所提到的能量增減總和即為溶劑化自由能(free energy of solvation)[5]。
對穩定性的影響
[編輯]不同的溶劑可能會因為反應物及產物的穩定性差異而影響反應的平衡常數,反應會朝向產物較穩定的方向平衡。反應物或產物可利用任何與溶劑所產生的非共價相互作用(如氫鍵、偶極-偶極相互作用、凡得瓦力等作用)來提升穩定性。
酸鹼平衡
[編輯]酸或鹼的電解平衡會受溶劑變化影響。但溶劑不僅僅是受其酸性或鹼性影響,同時也受到其介電常數(dielectric constant)和其優先溶劑化(preferentially solvate)影響,而使特定反應的酸鹼平衡較穩定;換而言之,即溶解能力及介電常數的變化皆可以影響的溶液的酸鹼值。
| 溶劑 | 介電常數[6] |
|---|---|
| 乙腈(氰化甲烷)(Acetonitrile, ACN) | 37 |
| 二甲基亞碸(Dimethylsulfoxide, DMSO) | 47 |
| 水(Water) | 78 |
在上表中可以看出水是極性最大的溶劑,第二為DMSO,最後為氰化甲烷。
再思考下面的酸離解公式:
- HA ⇌ A− + H+,
水是上表中極性最大的溶劑,相較於二甲基亞碸或氰化甲烷,水使得離子化的物質能產生更高的穩定度;由此可知,水中的酸性會比二甲基亞碸或氰化甲烷來得低,如下表中可看出,pKa值在25℃時之值為氰化甲烷(ACN)[7][8][9]>二甲基亞碸(DMSO)[10]>水。
| HA ⇌ A− + H+ | ACN | DMSO | water |
|---|---|---|---|
| 對-甲苯磺酸(p-Toluenesulfonic acid) | 8.5 | 0.9 | 強 |
| 2,4-二硝基酚(2,4-Dinitrophenol) | 16.66 | 5.1 | 3.9 |
| 苯甲酸(Benzoic acid) | 21.51 | 11.1 | 4.2 |
| 醋酸(Acetic acid) | 23.51 | 12.6 | 4.756 |
| 酚(Phenol) | 29.14 | 18.0 | 9.99 |
酮烯醇的平衡(Keto enol equilibria)
[編輯]各種1,3 - 二羰基化合物(1,3-dicarbonyl compounds)可以透過互變異構物(tautomeric forms)的形式存在,如圖所示。

1,3 - 二羰基化合物最常在環烯醇(cyclic enol)(為順式異構體)和二酮(diketo)這兩種結構間互相轉換。
互變異構作用的平衡常數如下:
溶劑對乙酰丙酮(Acetylacetone)互變異構的平衡常數之影響如下:
| 溶劑 | KT |
|---|---|
| 氣態(Gas phase) | 11.7 |
| 環己烷(Cyclohexane) | 42 |
| 四氫呋喃(Tetrahydrofuran, THF) | 7.2 |
| 苯環(Benzene) | 14.7 |
| 乙醇(Ethanol) | 5.8 |
| 二氯甲烷(Dichloromethane) | 4.2 |
| 水(Water) | 0.23 |
參考資料
[編輯]- ^ Reichardt C: Solvents and solvent effects in organic chemistry. 2nd edition. VCH, New York, USA; 1991.
- ^ Mennucci, R. Cammi, J. Tomasi. "Medium Effects on the Properties of Chemical Systems: Electric and magnetic Response of Donor-Acceptor Systems within the Polarizable Continuum Model." Int. J. Quantum Chem., 75 (1999) 783
- ^ Bevilaqua T, Goncalves TF, Venturini CG, Machado VG: Solute-solvent and solvent-solvent interactions in the preferential solvation of 4-[4-(dimethylamino)styryl]-1-methylpyridinium iodide in 24 binary solvent mixtures.
- ^ Eric V. Anslyn; Dennis A. Dougherty. Modern Physical Organic Chemistry. University Science Books. 2006. ISBN 978-1-891389-31-3.
- ^ J. Chem. Phys. 134, 041105 (2011)
- ^ Template:Loudon p. 317–318
- ^ Kütt, A.; Movchun, V.; Rodima, T,; Dansauer, T.; Rusanov, E.B. ; Leito, I.; Kaljurand, I.; Koppel, J.; Pihl, V.; Koppel, I.; Ovsjannikov, G.; Toom, L.; Mishima, M.; Medebielle, M.; Lork, E.; Röschenthaler, G-V.; Koppel, I.A.; Kolomeitsev, A.A. Pentakis(trifluoromethyl)phenyl, a Sterically Crowded and Electron-withdrawing Group: Synthesis and Acidity of Pentakis(trifluoromethyl)benzene, -toluene, -phenol, and -aniline. J. Org. Chem. 2008, 73 (7): 2607–2620. PMID 18324831. doi:10.1021/jo702513w.
- ^ Kütt, A.; Leito, I.; Kaljurand, I.; Sooväli, L.; Vlasov, V.M.; Yagupolskii, L.M.; Koppel, I.A. A Comprehensive Self-Consistent Spectrophotometric Acidity Scale of Neutral Brønsted Acids in Acetonitrile. J. Org. Chem. 2006, 71 (7): 2829–2838. PMID 16555839. doi:10.1021/jo060031y.
- ^ Kaljurand, I.; Kütt, A.; Sooväli, L.; Rodima, T.; Mäemets, V. Leito, I; Koppel, I.A. Extension of the Self-Consistent Spectrophotometric Basicity Scale in Acetonitrile to a Full Span of 28 pKa Units: Unification of Different Basicity Scales. J. Org. Chem. 2005, 70 (3): 1019–1028. PMID 15675863. doi:10.1021/jo048252w.
- ^ Bordwell pKa Table (Acidity in DMSO). [2008-11-02]. (原始內容存檔於2008-10-09).

![{\displaystyle {\mathbf {K} }_{\mathrm {T} }={\frac {[cis-enol]}{[diketo]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e9921ac02a5c977cb96d9a14a8fd9ffe9794422f)