氢化钛
外观
| 氢化钛[1] | |
|---|---|
| |

| |
| 别名 | 氢化钛(II),二氢化钛 |
| 识别 | |
| CAS号 | 7704-98-5 ? |
| PubChem | 197094 |
| RTECS | XR2130000 |
| 性质 | |
| 化学式 | TiH2 |
| 摩尔质量 | 49.883 g·mol⁻¹ |
| 外观 | 深灰色粉末 |
| 密度 | 3.75 g/cm3 |
| 熔点 | 450°C时分解 |
| 溶解性(水) | 不溶于水 |
| 结构 | |
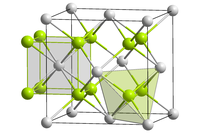
| 晶体结构 | 萤石型(立方),cF12 |
| 空间群 | Fm3m, No. 225 |
| 危险性 | |
| 欧盟分类 | 未提及 |
| NFPA 704 | |
| 自燃温度 | 342 °C |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
氢化钛(TiH2)是一种钛元素和氢元素形成的金属氢化物。它化学性质比较活泼,需保存在远离高温和强氧化剂处。
因为在空气中较稳定,它也可以被用于制备氢气和氢氧化钛。它可以由氢气与金属钛直接反应获得。300℃以上时,金属钛能可逆地吸收氢,最终形成化学式为TiH2的化合物。如果加热到1000℃以上,氢化钛将完全分解为钛和氢气。在足够高的温度下,钛氢合金与氢气处于平衡状态,此时氢气的分压是金属中氢含量和温度的函数。氢化钛还存在成分可变、Ti-H间距不同的结构很复杂的缺氢相,这些缺氢相近年来得到广泛的研究,因为它们可用于制作缓冲器、反射器或高温防护装备,还有可能用于移动式的核反应堆。[2]
氢化钛与高氯酸钾一起用作烟花爆竹的点火剂和闪光粉。它还在生产发泡金属的工艺中用作发泡剂。
钛的其他含氢化合物有TiHCl3。人们认为这是齐格勒-纳塔催化剂催化烯烃加聚反应的中间体。据报道这是一种不稳定的液体,Ti-H键的伸缩振动频率约为1600cm-1。但它至今还未被分离出来。[3]
参考资料
[编辑]- ^ Lide, David R., Handbook of Chemistry and Physics 87, Boca Raton, FL: CRC Press: 4–91, 1998, ISBN 0-8493-0594-2
- ^ Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements, 2nd Edition, Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- ^ 张青莲. 《无机化学丛书》第八卷:钛分族、钒分族、铬分族. 北京: 科学出版社. : P21. ISBN 7-03-002238-6.

