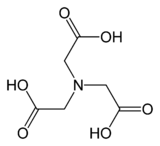
氮[基]三醋酸
| 氮[基]三醋酸 | |
|---|---|
| |
| IUPAC名 2,2′,2′′-Nitrilotriacetic acid[1] | |
| 英文名 | N,N-Bis(carboxymethyl)glycine[2] 2- [Bis(carboxymethyl)amino]acetic acid[2] Triglycine[3] |
| 識別 | |
| CAS號 | 139-13-9 |
| PubChem | 8758 |
| ChemSpider | 8428 |
| SMILES |
|
| Beilstein | 1710776 |
| Gmelin | 3726 |
| UN編號 | 2811 |
| EINECS | 205-355-7 |
| ChEBI | 44557 |
| RTECS | AJ0175000 |
| DrugBank | DB03040 |
| KEGG | C14695 |
| MeSH | Nitrilotriacetic+Acid |
| 性質 | |
| 化學式 | C6H9NO6 |
| 摩爾質量 | 191.14 g·mol−1 |
| 外觀 | 白色結晶 |
| 熔點 | 242 °C(515 K)(分解)[4] |
| 溶解性(水) | 3.8 g(25 °C)[5] |
| 熱力學 | |
| ΔfHm⦵298K | −1.3130–−1.3108 MJ mol−1 |
| 危險性 | |
GHS危險性符號 
| |
| GHS提示詞 | 警告 |
| H-術語 | H302, H319, H351 |
| P-術語 | P281, P305+351+338 |
| 致死量或濃度: | |
LD50(中位劑量)
|
1.1 g kg−1 (口服,大鼠) |
| 相關物質 | |
| 相關羧酸 | |
| 相關化學品 | |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氮[基]三醋酸(NTA)[6]是一種胺基多羧酸,示性式為N(CH2CO2H)3。它在常溫常壓下是一種無色固體,可做為螯合劑與Ca2+(鈣離子)、Co2+(亞鈷離子)、Cu2+(銅離子)和Fe3+(鐵離子)等金屬離子形成配位化合物(螯合物)。 [7]
製備
[編輯]氮[基]三醋酸及其鈉鹽可商購獲得。它由氨、甲醛和氰化鈉或氰化氫為原料所制備。每年全球產能估計為10萬噸。NTA 也作為EDTA合成中的雜質,由氨副產物的反應產生。 [8]
配位化學及應用
[編輯]NTA 的用途類似於 EDTA,兩者都是螯合劑。NTA的加入用於替代聚磷酸鈉和聚磷酸鉀作為水軟化劑、洗滌劑和清潔劑的功能。
在一項應用中,NTA可用於將鉻化砷酸銅處理過的木材中作為螯合劑去除其中的鉻、銅和砷。 [11]
實驗室中應用
[編輯]在實驗室中,該化合物用於錯合滴定。 NTA 的一種變體用於在組氨酸標籤方法中進行蛋白質分離和純化。 [12]修飾後的 NTA 可用於將鎳固定在固體支持物上。這允許純化有任一末端含六個組氨酸殘基組成標記的蛋白質。 [13]
組氨酸標籤結合金屬螯合劑複合物的金屬。以前,亞胺二乙酸用於此目的。現在,更常用的是氮[基]三醋酸。 [14]
Ernst Hochuli等人在1987年於實驗室將 NTA 配體和鎳離子用於耦合到瓊脂糖珠上。 [15]這種Ni-NTA 瓊脂糖 (頁面存檔備份,存於網際網路檔案館)是通過親和層析純化其標記蛋白的最常用工具。
- NTA複合體
-
[Ni(NTA)(H2O) 2 ]-結構的三個視圖。
-
鈣陽離子與氮[基]三醋酸根陰離子生七配位錯合物[Ca(NTA)(H2 O)3 ]-的結構式 。
-
氮[基]三醋酸鉺銨晶體,其中鉺的化合價為+3。
毒性與環境作用
[編輯]氮[基]三醋酸可引起眼睛、皮膚和呼吸道刺激;並可能導致腎臟和膀胱損傷。預計該化合物有可能導致人類癌症。 [2]
與 EDTA 相比,NTA 易於生物降解,並且在廢水處理過程中可幾乎被完全去除。 NTA 對環境的影響很小。儘管廣泛用於清潔產品,但供水中的濃度太低,不會對人類健康或環境質量產生相當大的影響。 [16]
參考資料
[編輯]- ^ Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014: 21, 679. ISBN 978-0-85404-182-4. doi:10.1039/9781849733069.
- ^ 2.0 2.1 2.2 Nitrilotriacetic Acid - Compound Summary. PubChem Compound. USA: National Center for Biotechnology Information. Identification. 26 March 2005 [2012-07-13]. (原始內容存檔於2023-04-04).
- ^ Nitrilotriacetic acid. [2021-07-11]. (原始內容存檔於2014-01-02).
- ^ "PhysProp" data were obtained from Syracuse Research Corporation of Syracuse, New York (US). Retrieved from SciFinder. [2021-07-12].
- ^ Calculated using Advanced Chemistry Development (ACD/Labs) Software V11.02 (© 1994-2021 ACD/Labs). Retrieved from SciFinder. [2021-07-12].
- ^ 樂詞網--氮[基]三醋酸. 國家教育研究院. [2023-08-11]. (原始內容存檔於2023-08-11) (中文(臺灣)).
- ^ Nitrilotriacetic Acid and Its Salts (頁面存檔備份,存於網際網路檔案館), International Agency for Research on Cancer
- ^ Hart, J. Roger (2005) "Ethylenediaminetetraacetic Acid and Related Chelating Agents" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim. doi:10.1002/14356007.a10_095
- ^ Yuan, Yongkun; Jiang, Yugui. Preparation process of N-(2-amino-2-oxoethyl)-N-(carboxymethyl)-glycine. 2020 CN 111909047 A.
- ^ B. L. Barnett, V. A. Uchtman "Structural investigations of calcium-binding molecules. 4.
- ^ Fang-Chih, C.; Ya-Nang, W.; Pin-Jui, C.; Chun-Han, K. Factors affecting chelating extraction of Cr, Cu, and As from CCA-treated wood.
- ^ Liu, Weijing. Layer-by-Layer Deposition with Polymers Containing Nitrilotriacetate, A Convenient Route to Fabricate Metal- and Protein-Binding Films. ACS Applied Materials & Interfaces. 2016, 8 (16): 10164–73. PMID 27042860. doi:10.1021/acsami.6b00896.
- ^ qiaexpressionist (PDF). [2021-07-11]. (原始內容存檔 (PDF)於2007-02-22).
- ^ Lauer, Sabine A.; Nolan, John P. Development and characterization of Ni-NTA-bearing microspheres. Cytometry. 2002, 48 (3): 136–145. ISSN 1097-0320. PMID 12116359. doi:10.1002/cyto.10124.
- ^ Hochuli, E.; Döbeli, H.; Schacher, A. New metal chelate adsorbent selective for proteins and peptides containing neighbouring histidine residues. Journal of Chromatography A. January 1987, 411: 177–184. ISSN 0021-9673. PMID 3443622. doi:10.1016/s0021-9673(00)93969-4.
- ^ Brouwer, N.; Terpstra, P. Ecological and Toxicological Properties of Nitrilotriacetic Acid (NTA) as a Detergent Builder.

![[Ni(NTA)(H2O) 2 ]-結構的三個視圖。](http://upload.wikimedia.org/wikipedia/commons/thumb/1/14/Ni%28NTA%29%28aq%2923views.png/500px-Ni%28NTA%29%28aq%2923views.png)
![鈣陽離子與氮[基]三醋酸根陰離子生七配位錯合物[Ca(NTA)(H2 O)3 ]-的結構式 。](http://upload.wikimedia.org/wikipedia/commons/thumb/0/06/Calcium_complex_of_NTA_trianion.svg/210px-Calcium_complex_of_NTA_trianion.svg.png)