 米氏方程
米氏方程
米-門二氏動力學(英語:Michaelis-Menten kinetics),又稱米氏動力學,以德國生物化學家萊昂諾爾·米夏埃利斯和加拿大醫師莫德·門滕的名字命名,是酶動力學中一個極為重要的方程,可以描述多種非變異構酶動力學現象,其表示式為[1]:
![{\displaystyle V_{0}=V_{max}{\frac {[S]}{K_{M}+[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aea91db71093c3e3765f9735e885876853c774bd)
以下米氏方程的推導是由喬治·愛德華·布里格斯和約翰·伯頓·桑德森·霍爾丹在1925年提出的[2]:
假設有下圖所示的酶促反應

假設此酶促反應不可逆,反應產物不和酶結合;k2<k-1, E+S⇌ES 之間的平衡迅速建立達到平衡態(Steady-state),也就是受質和酶的化合物(ES)的濃度不變;建立平衡態所消耗的受質的量很小,可以忽略。這樣有以下關係:
![{\displaystyle {\frac {d[ES]}{dt}}=k_{1}[E][S]-k_{-1}[ES]-k_{2}[ES]=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2bb19158ff794158ceac860552fbfa1eacdf3558)
![{\displaystyle [ES]={\frac {k_{1}[E][S]}{k_{-1}+k_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/041c97c8ca3aa792f4fe79f75ec6b88ba19098aa)
米氏常數Km的定義為:

原式可簡化為:
![{\displaystyle [ES]={\frac {[E][S]}{K_{M}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/426c5653fdc41c7abfc4c6476a0a1382218a6b18) (1)
(1)
總的酶的濃度[E0]等於自由酶[E]與酶-受質化合物[ES]的和,則有以下關係:
![{\displaystyle [E_{0}]=[E]+[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/98b6b65c6ec79a6eb4bdb476e877e3acfb8c6503)
![{\displaystyle [E]=[E_{0}]-[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ba5fa93cfdb8b7ffec08ac9d5892a6df7b7c1694) (2)
(2)
將(2)式代入(1):
![{\displaystyle [ES]={\frac {([E_{0}]-[ES])[S]}{K_{M}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6860b0e8111740790c87ad122a1a178d5fe0250f)
整理得:
![{\displaystyle [ES]{\frac {K_{M}}{[S]}}=[E_{0}]-[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f3dd9883ccb42a38f3da032b9d36546eb5abd251)
=[E_{0}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c94beb1eac2e33f33b3d17ce7fe076bfc19db071)
![{\displaystyle [ES]=[E_{0}]{\frac {1}{1+{\frac {K_{M}}{[S]}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a00fd6436acc76be3c4d255ecaef581be2c3697e) (3)
(3)
下式可以描述該酶促反應的速率:
![{\displaystyle {\frac {d[P]}{dt}}=k_{2}[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0fc45725f2f145f603fcf61641d533d1bbcdb70d) (4)
(4)
將 (3) 代入 (4),分號上下同時乘以[S]得:
![{\displaystyle {\frac {d[P]}{dt}}=k_{2}[E_{0}]{\frac {[S]}{K_{M}+[S]}}=V_{max}{\frac {[S]}{K_{M}+[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4b54929f1125ebd25b46665b8fe7aec861f8bf33)
或
![{\displaystyle V_{0}=V_{max}{\frac {[S]}{K_{M}+[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aea91db71093c3e3765f9735e885876853c774bd)
該式可通過非線性作圖或Lineweaver-Burk(雙倒數作圖),Eadie-Hofstee等作圖法變換為線性圖進行分析。
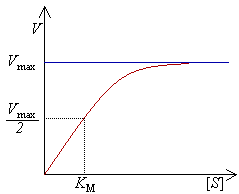
 用Vmax=100,KM=10繪製的米氏方程的圖像。
用Vmax=100,KM=10繪製的米氏方程的圖像。
在推導過程中幾點需要注意:
- [E0]是總的酶的量。反應中酶-底物配合物的量[ES]是極不好測量的,所以式子必須寫成[E0]表示的形式,因為試驗中所用的酶的量是已知的。
- d[P]/dt(V0, 反應初速度),是試驗中測得的產物生成的初速度,一般是酶促反應在反應開始的幾秒鐘到幾分鐘之內的速度,在這段時間內底物的真實濃度幾乎和底物最初的濃度相同([S]≈[S0])。
- k2[E0](Vmax) 是酶促反應在給定的酶的量下的最大速度(當所有的酶都在酶-底物配合物的狀態下)。k2有時也寫為kcat。
- 米氏常數是酶的特徵性物理常數。
- 從KM可判斷酶的專一性和天然底物。
- 進行酶活力測定時通常選10KM。
- 底物濃度較低時,KM可判斷底物走哪一條代謝途徑。
要測得方程中的KM和Vmax,需要在酶的量[E0]恆定並已知的情況下,在不同的底物濃度[S]下測得反應的初速度V0,用非線性作圖或線性作圖的方法求得KM和Vmax。
KM反映了底物和酶結合的緊密程度,Vmax反映了酶催化反應的速度。
- ^ Leonor Michaelis, Maud Menten (1913). Die Kinetik der Invertinwirkung, Biochem. Z. 49:333-369.
- ^ G. E. Briggs and J. B. S. Haldane (1925) A note on the kinetics of enzyme action, Biochem. J., 19, 339-339.



![{\displaystyle V_{0}=V_{max}{\frac {[S]}{K_{M}+[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aea91db71093c3e3765f9735e885876853c774bd)

![{\displaystyle {\frac {d[ES]}{dt}}=k_{1}[E][S]-k_{-1}[ES]-k_{2}[ES]=0}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2bb19158ff794158ceac860552fbfa1eacdf3558)
![{\displaystyle [ES]={\frac {k_{1}[E][S]}{k_{-1}+k_{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/041c97c8ca3aa792f4fe79f75ec6b88ba19098aa)

![{\displaystyle [ES]={\frac {[E][S]}{K_{M}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/426c5653fdc41c7abfc4c6476a0a1382218a6b18)
![{\displaystyle [E_{0}]=[E]+[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/98b6b65c6ec79a6eb4bdb476e877e3acfb8c6503)
![{\displaystyle [E]=[E_{0}]-[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ba5fa93cfdb8b7ffec08ac9d5892a6df7b7c1694)
![{\displaystyle [ES]={\frac {([E_{0}]-[ES])[S]}{K_{M}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6860b0e8111740790c87ad122a1a178d5fe0250f)
![{\displaystyle [ES]{\frac {K_{M}}{[S]}}=[E_{0}]-[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f3dd9883ccb42a38f3da032b9d36546eb5abd251)
=[E_{0}]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c94beb1eac2e33f33b3d17ce7fe076bfc19db071)
![{\displaystyle [ES]=[E_{0}]{\frac {1}{1+{\frac {K_{M}}{[S]}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a00fd6436acc76be3c4d255ecaef581be2c3697e)
![{\displaystyle {\frac {d[P]}{dt}}=k_{2}[ES]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/0fc45725f2f145f603fcf61641d533d1bbcdb70d)
![{\displaystyle {\frac {d[P]}{dt}}=k_{2}[E_{0}]{\frac {[S]}{K_{M}+[S]}}=V_{max}{\frac {[S]}{K_{M}+[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4b54929f1125ebd25b46665b8fe7aec861f8bf33)