薗頭耦合反應
薗頭耦合反應(英語:Sonogashira coupling,日語:薗頭カップリング Sonogashira Kappuringu,「薗」普通話音「園」),又稱Sonogashira偶聯反應、薗頭反應或薗頭-萩原耦合反應,是一種有機合成中用到的形成碳 - 碳鍵的交叉偶聯反應[1][2]。
它使用鈀催化劑在末端炔和芳基或乙烯基鹵化物之間形成碳 - 碳鍵。由於其有用的形成碳 - 碳鍵的性質,薗頭耦合反應被廣泛應用在各種領域。該反應可以在溫和的條件下進行,例如室溫、水相以及在弱鹼的存在之下,這使得薗頭耦合反應可以被應用在複雜分子的合成中。在製藥、天然產物合成等之中都有所應用[1]。其在合成中的應用包括tazarotene[3],一種治療銀屑病和粉刺的藥物,以及 altinicline[4],一種潛在的可以治療帕金森病、阿茲海默病、圖雷特氏綜合症、精神分裂症和注意缺陷障礙的物質。
歷史[編輯]
薗頭耦合反應最早於1975年由三位在大阪大學的日本化學家薗頭健吉、任田康夫和萩原信衛所發表[2]。它是 Cassar 偶聯和可得到同樣產物,但需要高溫等較劇烈條件的赫克反應的擴充。薗頭耦合反應和赫克反應都用到了鈀催化劑促進偶聯,其中薗頭耦合反應同時使用了鈀催化劑和銅催化劑,提升了反應活性,使得反應可以在室溫進行,讓薗頭耦合反應十分有用,尤其是芳基和烯基鹵化物的炔化上[5] 。其出色的應用價值從現在仍在進行的對其反應條件的進一步優化和理解的研究中就可見一斑。經常有在鈀(0)催化劑催化下末端炔和 sp2,甚至 sp3 - 鹵化物或三氟甲磺酸酯的偶聯反應,不論有沒有同時使用銅催化劑,都被稱作「薗頭耦合反應」,儘管它們實際上不是在薗頭耦合反應的條件下進行的[5]。
機理[編輯]
該反應的機理尚不明確,但有的研究認為它涉及到鈀循環和銅循環[6]。

鈀循環[編輯]
- 不活潑的鈀(II) 催化劑在鹼性條件下被還原為鈀(0) 化合物。
- 活化的鈀催化劑為 14 電子化合物 ,Pd0L2,它可以和芳基或烯基鹵化物發生氧化加成反應,生成鈀(II) 錯合物中間體。這一步被認為是此反應中的速率決定步驟。
- 鈀(II) 錯合物中間體和銅催化循環中生成的炔銅錯合物發生金屬置換反應,重新生成鹵化亞銅並回到銅催化循環中。
- 氧化加成後的錯合物為反式構型,在順反異構化後之後才能在之後生成最後產物。
- 在最後一步中,順反異構化後的鈀(II) 錯合物中間體發生還原消除反應,生成偶聯化產物,鈀催化劑重新生成。
銅循環[編輯]
- 反應過程中被認為在鹼的存在下,形成了π-炔錯合物,增加了末端炔質子的酸性,促進了炔銅化合物的形成。
- 炔銅化合物繼續和鈀(II) 錯合物中間體反應,同時得到恢復的鹵化亞銅。
對該反應機理的研究表明反應中存在以上的催化循環,但對於有些依反應條件不同而發生變化的中間體的準確結構仍存在爭論。例如,有證據表明在和體積較大的膦反應時,單錯合的 Pd0(PR3) 錯合物會成為可能的催化中間體[7]。與之相反的是,有一些結果指出,實際上催化劑並不是配位飽和的 Pd0L2 錯合物,而是形成的鈀陰離子物種。在有陰離子和鹵化物存在時常見的 Pd0(PPh3)2 在有鹵素陰離子存在時並不能在溶液里形成,因為它會飽和配位 Pd0,形成陰離子物種 [L2Pd0Cl]-,參與交叉偶聯反應[8]。
催化劑[編輯]
一般情況下,該反應需要兩種催化劑:一種鈀(0) 錯合物和一種銅(I) 鹵化物。鈀催化劑的例子有鈀 - 膦錯合物,例如 Pd(PPh3)4,其衍生物 Pd(PPh3)2Cl2 也較常用。也有使用雙齒配體錯合物 Pd(dppe)Cl2、Pd(dppp)Cl2 和 Pd(dppf)Cl2 的情況[6]。使用這些催化劑的缺點是需要較大量的鈀(可達 5% 化學當量)和更大量的銅催化劑[6]。鈀(II) 經常作為被用作預催化劑,因為它比鈀(0) 更加穩定,而且可以在實驗室條件下穩定保存數月之久[9]。若使用鈀(II) 催化劑時,鈀(II)在反應中會被胺、膦配體或反應物還原至鈀(0),使反應繼續進行[10]。當使用類似 Pd(PPh3)2Cl2 的催化劑時,三苯基膦被氧化生成三苯基氧化膦也可以促進鈀(0)的形成。
銅(I) 鹽,例如碘化亞銅,會和末端炔反應形成銅(I) 炔化物,作為偶聯反應中的活性物質。銅(I) 鹽作為反應的副催化劑,可以提高反應速率[5]。
反應條件[編輯]
薗頭耦合反應通常在較溫和的條件下進行[11]。交叉偶聯在鹼,通常為同時作為溶劑的胺的存在下進行[2]。反應介質必須為鹼性,以中和反應中產生的鹵化氫,所以三乙胺、二乙胺等胺類物質通常被作為溶劑使用,二甲基甲酰胺和乙醚也可作為溶劑。偶爾也會使用碳酸鉀、碳酸銫等其他鹼。此反應必須在隔絕空氣的條件下進行,因為鈀(0) 錯合物在空氣中不穩定,且氧氣的存在會促進炔二聚體的產生。 根據 sp2 鹵化物或三氟甲磺酸酯底物的不同,在這些反應條件下會得到不同的結果。
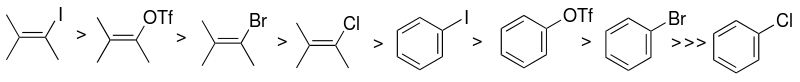
應用[編輯]
同大多數鈀介導的偶合反應一樣,該反應一般只適用於不飽和碳原子之間的偶合。在傳統有機合成中,乙烯基鹵素都是惰性化合物,很難發生取代反應,但在現代有機合成中這種觀念發生了徹底的變化。在鈀催化下乙烯基鹵素化合物變得相當活潑,能發生一系列取代反應。而薗頭反應就是其中一個反應代表。烯炔結構是天然產物中常見的結構,特別是菊科植物的次生代謝產物富含這種結構。在全合成研究中薗頭反應無疑是一種有力的合成手段。
另見[編輯]
參考文獻[編輯]
- ^ 1.0 1.1 Sonogashira, K., Development of Pd-Cu catalyzed cross-coupling of terminal acetylenes with sp2-carbon halides, J. Organomet. Chem., 2002, 653: 46–49, doi:10.1016/s0022-328x(02)01158-0
- ^ 2.0 2.1 2.2 Sonogashira, K., Tohda, Y., Hagihara, N., A convenient synthesis of acetylenes: catalytic substitutions of acetylenic hydrogen with bromoalkenes, iodoarenes and bromopyridines, Tetrahedron Lett., 1975, 16: 4467–4470, doi:10.1016/s0040-4039(00)91094-3
- ^ Frigoli, S., Fuganti, C., Malpezzi, L., Serra, S., Palladium-Catalyzed Cross-Coupling Reactions in the Synthesis of Pharmaceuticals, Org. Process Res. Dev., 2004, 6: 205–245, doi:10.1007/b94551
- ^ King, A. O., Yasuda, N., A Practical and Efficient Process for the Preparation of Tazarotene, Top. Organomet. Chem., 2005, 9: 646–650, doi:10.1021/op050080x
- ^ 5.0 5.1 5.2 Chinchilla, R.: Najera, C., Recent advances in Sonogashira reactions, Chem. Soc. Rev., 2011, 40: 5084–5121, doi:10.1039/c1cs15071e
- ^ 6.0 6.1 6.2 6.3 Chinchilla, R.; Najera, C., The Sonogashira Reaction: A Booming Methodology in Synthetic Organic Chemistry, Chem. Rev., 2007, 107: 874–922, PMID 17305399, doi:10.1021/cr050992x
- ^ Stambuli, J. P.; Buhl, M.; Hartwig, J. F., Synthesis, Characterization, and Reactivity of Monomeric, Arylpalladium Halide Complexes with a Hindered Phosphine as the Only Dative Ligand, J. Am. Chem. Soc., 2002, 124: 9346–9347, doi:10.1021/ja0264394
- ^ Amatore, C.; Jutand, A., Anionic Pd(0) and Pd(II) Intermediates in Palladium-Catalyzed Heck and Cross-Coupling Reactions, Acc. Chem. Res., 2000, 33: 314–321, doi:10.1021/ar980063a
- ^ Bohm, V. P. W.; Herrmann, W. A., A Copper-Free Procedure for the Palladium-Catalyzed Sonogashira Reaction of Aryl Bromides with Terminal Alkynes at Room Temperature, Eur. J. Org. Chem., 2000, 200: 3679–3681, doi:10.1002/1099-0690(200011)2000:22<3679::aid-ejoc3679>3.0.co;2-x
- ^ Yin, L.; Liebscher, J., Carbon-Carbon Coupling Reactions Catalyzed by Heterogeneous Palladium Catalysts, Chem. Rev., 2006, 107: 133–173, doi:10.1021/cr0505674
- ^ Kohnen, A. L; Danheiser, R. L., Synthesis of Terminal 1,3-Diynes Via Sonogashira Coupling of Vinylidene Chloride Followed by Elimination. Preparation of 1,3-Decadiyne, Org. Synth., 2007, 84: 77, doi:10.15227/orgsyn.084.0077
| |||||||||||||||||

![{\displaystyle {\begin{matrix}{}\\{\mathsf {{\ce {R-\!{\equiv }\!-H}}+\underbrace {\color {Red}{\ce {R'}}} _{{\text{Aryl,}} \atop {Vinyl}}\!-\!\underbrace {X} _{{\text{I, Br,}} \atop {\text{Cl, OTf}}}{\ce {->[{\text{Pd cat., Cu cat.}}][{\text{base, rt}}]R-\!{\equiv }\!}}{\color {Red}{-}}{\color {Red}{\ce {R'}}}}}\end{matrix}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/2bda132325979b005ba667d85a7ccb64c6151228)