讨论:N-溴代丁二酰亚胺
|
本条目页依照页面评级标准评为乙级。 本条目页属于下列维基专题范畴: |
|||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|||||||||||||||||
| N-溴代丁二酰亚胺曾于2015年7月9日通过新条目推荐投票,登上维基百科首页的“你知道吗?”栏位。 |
 | 此条目为第十三次动员令多于15种外语版本的条目类的作品之一,是一篇达标条目。 |
从英文版翻译
[编辑]| N-溴代丁二酰亚胺 | |
|---|---|

| |

| |
| IUPAC名 1-Bromo-2,5-pyrolidinedione | |
| 别名 | N-bromosuccinimide; NBS |
| 识别 | |
| CAS号 | 128-08-5 |
| SMILES |
|
| 性质 | |
| 化学式 | C4H4BrNO2 |
| 摩尔质量 | 177.98 g·mol⁻¹ |
| 外观 | White solid |
| 密度 | 2.098 g/cm3 (solid) |
| 熔点 | 175 - 178 °C |
| 溶解性(水) | 1.47 g / 100 mL (25 °C) |
| 危险性 | |
| 主要危害 | Irritant |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
N-Bromosuccinimide or NBS is a chemical reagent which is used in radical substitution and electrophilic addition reactions in organic chemistry. NBS can be considered a convenient source of bromine.
Chemistry
[编辑]Addition to alkenes
[编辑]NBS will react with alkenes 1 in aqueous solvents to give bromohydrins 2. The preferred conditions are the portionwise addition of NBS to a solution of the alkene in 50% aqueous DMSO, DME, THF, or tert-butanol at 0°C.[1] Formation of a bromonium ion and immediate attack by water gives strong Markovnikov addition and anti stereochemical selectivities.[2]
Side reactions include the formation of α-bromo-ketones and dibromo compounds. These can be minimized by the use of freshly recrystallized NBS.
With the addition of nucleophiles, instead of water, various bifunctional alkanes can be synthesized.[3]
Allylic and benzylic bromination
[编辑]Standard conditions for using NBS in allylic and/or benzylic bromination involves refluxing a solution of NBS in anhydrous CCl4 with a radical initiator, usually azo-bis-isobutyronitrile (AIBN), benzoyl peroxide, irradiation, or both to effect radical initiation.[4][5] This is also called the Wohl-Ziegler reaction.[6][7]
The carbon tetrachloride must be maintained anhydrous throughout the reaction, as the presence of water may likely hydrolyze the desired product.[8] Barium carbonate is often added to maintain anhydrous and acid-free conditions.
Bromination of carbonyl derivatives
[编辑]NBS can α-brominate carbonyl derivatives via either a radical pathway (as above) or via acid-catalysis. For example, hexanoyl chloride 1 can be brominated in the alpha-position by NBS using acid catalysis.[9]
The reaction of enolates, enol ethers, or enol acetates with NBS is the preferred method of α-bromination as it is high-yielding with few side-products.[10][11]
Bromination of aromatic derivatives
[编辑]Electron-rich aromatic compounds, such as phenols, anilines, and various aromatic heterocycles[12], can be brominated using NBS.[13][14] Using DMF as the solvent gives high levels of para-selectivity.[15]
Hofmann rearrangement
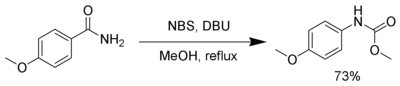
[编辑]NBS, in the presence of a strong base, such as DBU, reacts with primary amides to produce a carbamate via the Hofmann rearrangement.[16]
Selective oxidation of alcohols
[编辑]It is uncommon, but possible for NBS to oxidize alcohols. E. J. Corey et al. found that one can selectively oxidize secondary alcohols in the presence of primary alcohols using NBS in aqueous DME.[17]
Preparation
[编辑]NBS is commercially available. It can also be synthesized in the laboratory. To do so, sodium hydroxide and bromine are added to an ice-water solution of succinimide. The NBS product precipitates out and can be collected by filtration.
Crude NBS gives better yield in the Wohl-Ziegler reaction. In other cases, impure NBS (slightly yellow-colored) may give unreliable results. It can be purified by recrystallization from 90-95 °C water.
Precautions
[编辑]Although NBS is easier and safer to handle than bromine, precautions should be taken to avoid inhalation. NBS should be stored in a refrigerator. NBS will decompose over time giving off bromine. Pure NBS is white, but it is often found to be off-white or brown colored by bromine.
In general, reactions involving NBS are exothermic. Therefore, extra precautions should be taken when used on a large scale.
See also
[编辑]References
[编辑]- ^ Hanzlik, R. P. Organic Syntheses, Coll. Vol. 6, p.560 (1988); Vol. 56, p.112 (1977). (Article)
- ^ Beger, J. J. Prakt. Chem. 1991, 333(5), 677-698.
- ^ Haufe, G.; Alvernhe, G.; Laurent, A.; Ernet, T.; Goj, O.; Kröger, S.; Sattler, A. Organic Syntheses, Coll. Vol. 10, p.128 (2004); Vol. 76, p.159 (1999). (Article)
- ^ Djerassi, C.; Chem. Rev. 1948, 43, 271.
- ^ Greenwood, F. L.; Kellert, M. D.; Sedlak, J. Organic Syntheses, Coll. Vol. 4, p.108 (1963); Vol. 38, p.8 (1958). (Article)
- ^ Wohl, A. Ber. 1919, 52, 51.
- ^ Ziegler, K.; et al. Ann. 1942, 551, 30.
- ^ Binkley, R. W.; Goewey, G. S.; Johnston, J; J. Org. Chem. 1984, 49, 992.
- ^ Harpp, D. N.; Bao, L. Q.; Coyle, C.; Gleason, J. G.; Horovitch, S. Organic Syntheses, Coll. Vol. 6, p.190 (1988); Vol. 55, p.27 (1976). (Article)
- ^ Stotter, P. L.; Hill, K. A.; J. Org. Chem. 1973, 38, 2576.
- ^ Lichtenthaler, F. W.; et al. Synthesis 1992, 179.
- ^ Amat, M.; Hadida, S.; Sathyanarayana, S.; Bosch, J. Organic Syntheses, Coll. Vol. 9, p.417 (1998); Vol. 74, p.248 (1997). (Article)
- ^ Gilow, H. W.; Burton, D. E.; J. Org. Chem. 1981, 46, 2221.
- ^ Brown. W. D.; Gouliaev, A. H. Organic Syntheses, Vol. 81, p.98 (2005). (Article)
- ^ Mitchell, R. H.; Lai, Y.-H.; Williams, R. V.; J. Org. Chem. 1979, 44, 4733.
- ^ Keillor, J. W.; Huang, X. Organic Syntheses, Coll. Vol. 10, p.549 (2004); Vol. 78, p.234 (2002). (Article)
- ^ Corey, E. J.; Ishiguro, M. Tetrahedron Lett. 1979, 20, 2745-2748.
External links
[编辑]{{DEFAULTSORT:Bromosuccinimide, N-}} [[:Category:Organobromides]] [[:Category:Reagents for organic chemistry]] [[:de:N-Bromsuccinimid]] [[:ja:N-ブロモスクシンイミド]] [[:pl:NBS]]
-Zhuhui 2007年8月1日 (三) 19:43 (UTC)
挂disputed维护模板
[编辑]各位可参考WP:DYKC候选区的意见进行改善。--食人魔国王Talk 2015年7月9日 (四) 02:39 (UTC)
- 第一点所述内容已删除,第三点及之后各点已经改善。第二点留待原作者处理。--William915(与我讨论) 2015年7月9日 (四) 13:27 (UTC)
- @William915:不好意思这么晚才回复您,感谢您再次为我的不专业翻译抓出错误
- 1.这部分我太粗心了,写的时候竟然把整段文字给遗漏了,已补上。
- 2.的确文献上没有注明温度,经过搜寻之后也没有找到相关资料,所以删除。
- 3.我来试试看能不能直接改图
- 谢谢您帮我改正第4条之后的问题。原来在有文献支持的状况下还有这么多不准确!之后做翻译的时候我会多多注意的,还请多多指教了。
- (PS. 根据使用者:和平奋斗救地球/自然科学条目提升计划的统计,虽然化学类的条目在维基的自然科条目中相对算是不缺乏的,但许多最基本的条目内容还是相当不足,还请您有空的话多多关注他们,最近发现我这种非化学本科专业的学生写起条目来还是有极限的,许多条目好像看得懂却都不敢碰><″)--Yrr933!(留言) 2015年7月10日 (五) 07:42 (UTC)
- @William915:不好意思这么晚才回复您,感谢您再次为我的不专业翻译抓出错误
新条目推荐讨论

- 在有机合成上,哪种试剂被广泛应用于自由基取代反应和亲电加成反应中,并可当作溴的替代物?。
 说明:条目翻译自英文维基,扩充约8400字节--Yrr933!(留言) 2015年7月5日 (日) 08:33 (UTC)
说明:条目翻译自英文维基,扩充约8400字节--Yrr933!(留言) 2015年7月5日 (日) 08:33 (UTC)- (+)支持:符合标准,部分错字与N的斜体显示问题已作修改。--William915(与我讨论) 2015年7月5日 (日) 08:56 (UTC)
- (+)支持:符合标准。--V (1984) 2015年7月5日 (日) 08:48 (UTC)
- (+)支持:符合标准。--Walter Grassroot (♬) 2015年7月6日 (一) 13:01 (UTC)
- (+)支持:符合标准。4Li 2015年7月7日 (二) 01:42 (UTC)
- (+)支持,符合标准。--Iflwlou [ M { 2015年7月7日 (二) 07:14 (UTC)
- @Yrr933!:
- 你告诉我,“将0.16莫耳(约16 g)的丁二酰亚胺溶于至于冰浴中的氢氧化钠溶液中(6.4 g溶入40 mL水中并加入30 g碎冰),持续搅拌约5分钟后,过滤并以清水清洗产物”的过程中有没有发生核反应?溴从哪里来?--Antigng(留言) 2015年7月7日 (二) 08:05 (UTC)
- 来源4中何处提到“进行此反应的最佳条件是在0 °C下,将NBS分批加入烯烃的DMSO或DME或THF或叔丁醇其中之一的50 %水溶液中。”--Antigng(留言) 2015年7月7日 (二) 08:17 (UTC)
- 右图有错,反应产物应当是消旋的。

- “进行烯丙基类与苯甲基类化合物的溴化反应的基本条件是在回流装置中将NBS溶入无水四氯化碳。”溶吗?9号、10号注释失效,无法查证。--Antigng(留言) 2015年7月7日 (二) 08:22 (UTC)
- “然而为了使此反应有较高的产率和较少其他副产物产生,通常会使用NBS加上烯醇或烯醇醚,这样也能产生α-溴化反应。”脚注13明明是烯醇锂盐的溴化反应,怎么在条目里写成了烯醇与NBS德反应?有多少烯醇可以稳定存在?--Antigng(留言) 2015年7月7日 (二) 08:30 (UTC)
- “拥有高电子密度的芳香类化合物像是酚、苯胺或杂环化合物……”杂环化合物都具有高电子密度?你可以试试用NBS给吡啶溴化。--Antigng(留言) 2015年7月7日 (二) 08:33 (UTC)
- “霍夫曼重排反应则是以一级酰胺和NBS与强碱(如DBU)反应产生胺基甲酸酯。”哪个来源这么说的?原文标题"METHYL CARBAMATE FORMATION VIA MODIFIED HOFMANN REARRANGEMENT REACTIONS",英文MODIFIED是什么意思?--Antigng(留言) 2015年7月7日 (二) 08:35 (UTC)
- (-)反对:内容欠准确,请主编回应并改善上述问题。--食人魔国王Talk 2015年7月9日 (四) 02:35 (UTC)