全氟丁磺醯氟
| 全氟丁磺醯氟 | |
|---|---|

| |
| IUPAC名 1,1,2,2,3,3,4,4,4-九氟丁-1-磺醯氟 1,1,2,2,3,3,4,4,4-Nonafluorobutane-1-sulfonyl fluoride | |
| 別名 | 全氟丁基磺醯氟 九氟丁磺醯氟 九氟丁基磺醯氟 |
| 識別 | |
| 縮寫 | NfF |
| CAS號 | 375-72-4 |
| PubChem | 67814 |
| ChemSpider | 61131 |
| SMILES |
|
| InChI |
|
| InChIKey | LUYQYZLEHLTPBH-UHFFFAOYAE |
| EINECS | 206-792-6 |
| 性質 | |
| 化學式 | C4F10O2S |
| 莫耳質量 | 302.09 g·mol⁻¹ |
| 密度 | 1.682 g/mL[1] |
| 熔點 | -120 °C(153 K) |
| 沸點 | 65 - 66 °C(272 K) |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
全氟丁磺醯氟(英語:Perfluorobutanesulfonyl fluoride),又稱九氟丁磺醯氟(英語:nonafluorobutanesulfonyl fluoride),縮寫NfF,是一種有機化合物,屬磺醯鹵的全氟衍生物。為無色易揮發液體,不溶於水但溶於常見的有機溶劑。其通過環丁碸電化學氟化得到,並用於製備全氟丁磺酸鹽或全氟丁磺酸酯,因為這類化合物可充當鈀催化的偶聯反應的親電試劑,在有機合成中有重要運用。全氟丁磺醯氟作為一種全氟烷基磺醯化試劑,與常用的三氟甲磺酸酐相比更穩定且成本更低。其結構中可離去的醯氟原子可以被胺、酚鹽以及烯醇鹽等親核試劑取代,分別得到對應的磺醯胺、磺酸芳香醇酯和磺酸烯醇酯。然而全氟丁磺醯氟不能被水這種弱親核試劑進攻,因此在pH < 12的水溶液中很穩定。全氟丁磺醯氟與氫氧化鋇反應會水解產生全氟丁磺酸鋇Ba(ONf)2,Ba(ONf)2與硫酸反應會進一步得到全氟丁磺酸和硫酸鋇沉澱。
提純
[編輯]
市售的全氟丁磺醯氟常含有6-10%的全氟環丁碸雜質,全氟環丁碸是在全氟丁磺醯氟生產過程中產生。將其與K3PO4和K2HPO4的1:1 摩爾比的高濃度水溶液進行強力攪拌96小時,靜置分層除去水相後加入P2O5進行蒸餾就可得到純度>99%的全氟丁磺醯氟,而且該方法幾乎沒有全氟丁磺醯氟損耗[2]。
對應的磺酸芳香醇酯和磺酸烯醇酯合成
[編輯]全氟丁磺酸的芳香醇酯和烯醇酯常作為鈀催化交叉偶聯反應中的親電試劑。其反應性和常用的三氟甲磺酸類親電試劑相似,但全氟丁磺酸酯更不易於水解產生對應的酮(烯醇互變異構產物)或酚。其耐水解特性使得其在布赫瓦爾德-哈特維希偶聯反應成為一種很好的親電試劑,以次減少水解副反應帶來的反應產率下降[3]。
β-酮酯的烯醇鈉鹽與1.15當量的全氟丁磺醯氟反應可高產得到相應的全氟丁磺酸烯醇酯。2-甲氧基乙醯乙酸乙酯(即R=R'=-CH3)利用該方法可以得到極高純度(幾何級)的E異構體[4]。
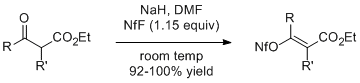
一些簡單的醛或酮與全氟丁磺醯氟在諸如DBU、磷腈等鹼存在下反應可以得到高產率的全氟丁磺酸烯醇酯,而不生成單獨的烯醇鹽。採用不對稱酮與全氟丁磺醯氟在P2-磷腈鹼作用下置於-30至-20°C間反應可以得到少取代的全氟丁磺酸烯醇酯[2]。若採用三氟甲磺酸酐進行類似的反應則需用到昂貴的2,6-二叔丁基吡啶才能得到較高的產率。
全氟丁磺醯氟與烯醇鹽反應結果很大程度上取決於烯醇鹽中烯醇陰離子和金屬陽離子的結構。例如,與甲基酮的烯醇鋰鹽反應時,全氟丁磺醯氟會親電進攻烯醇中的O原子(預期反應位點)和C原子(非預期反應位點),從而得到混合產物。這種效應在頻哪酮的烯醇鋰鹽中尤為明顯,它會產生有利於進攻C原子的2:1混合產物。取代程度更高的烯醇鋰鹽僅產生O-磺醯化產物,產率各不相同[5]。
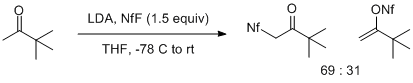
三甲基矽基烯醇基醚與全氟丁磺醯氟在亞化學計量的氟離子存在下,以0°C至室溫間反應可以得到產率適中的全氟丁磺酸烯醇酯。有研究表明採用乾燥的四丁基氟化銨作為氟離子源效果最好[5],但採用CsF能適應複雜和困難的情況[6]。

全氟丁磺酸芳香醇酯可由全氟丁磺醯氟與酚在碳酸鉀[7]和三乙胺[3]等鹼作用下直接反應得到,並且近乎完全反應。氫化鈉和丁基鋰等強鹼也可以用,但有時產率會較低[8]。
與醇反應
[編輯]全氟丁磺醯氟與醇的反應凸顯了全氟丁磺酸烷基醇酯的不穩定性,大多數情況下,與醇反應要麼得到的是氟代烷(由F-進攻全氟丁磺酸烷基醇酯中間產物得到);要麼是烯烴(酯中間體發生全氟丁磺酸消去反應)。
合成二全氟丁磺酸醯亞胺(Nf2NH)
[編輯]在乙腈中,全氟丁磺醯氟在三乙胺存在下與氯化銨發生反應得到二全氟丁磺酸醯亞胺三乙銨鹽,產率為97%。類似地,在三乙銨-KOH的甲醇溶液中反應可得到相應的鉀鹽[9]。利用Amberlite IR-100陽離子交換樹脂作為固定相,甲醇作為洗脫劑進行離子交換色譜分離可得到超強酸二全氟丁磺酸醯亞胺,這一過程中可能還產生了MeOH2+ Nf2N−鹽[10]。
參考文獻
[編輯]- ^ Perfluoro-1-butanesulfonyl fluoride. [22 July 2012].
- ^ 2.0 2.1 Vogel, Michael A. K.; Christian B. W. Stark; Ilya M. Lyapkalo. A Straightforward Synthesis of Alkenyl Nonaflates from Carbonyl Compounds Using Nonafluorobutane-1-sulfonyl Fluoride in Combination with Phosphazene Bases. Synlett. 2007, 2007 (EFirst): 2907–2911. ISSN 0936-5214. doi:10.1055/s-2007-991084.
- ^ 3.0 3.1 Meadows, Rebecca E.; Simon Woodward. Steric effects in palladium-catalysed amination of aryl triflates and nonaflates with the primary amines PhCH(R)NH2 (R=H, Me). Tetrahedron. 2008-02-11, 64 (7): 1218–1224. ISSN 0040-4020. doi:10.1016/j.tet.2007.11.074.
- ^ Bellina, Fabio; Donatella Ciucci; Renzo Rossi; Piergiorgio Vergamini. Synthesis of vinyl nonaflates derived from β-ketoesters, β-diketones or α-diketones and their palladium-catalyzed cross-coupling reactions with organozinc halides. Tetrahedron. 1999-02-12, 55 (7): 2103–2112. ISSN 0040-4020. doi:10.1016/S0040-4020(98)01221-6.
- ^ 5.0 5.1 Lyapkalo, Ilya M.; Matthias Webel; Hans-Ulrich Reißig. An Expedient and Stereoselective Synthesis of Alkenyl Nonaflates from Silyl Enol Ethers: Optimization, Scope and Limitations. European Journal of Organic Chemistry. 2002, 2002 (6): 1015–1025. ISSN 1099-0690. doi:10.1002/1099-0690(200203)2002:6<1015::AID-EJOC1015>3.0.CO;2-K.
- ^ Bräse, Stefan. Synthesis of Bis(enolnonaflates) and their 4-exo-trig-Cyclizations by Intramolecular Heck Reactions. Synlett. 1999, 1999 (10): 1654–1656. ISSN 0936-5214. doi:10.1055/s-1999-2892.
- ^ Shekhar, Shashank; Travis B. Dunn; Brian J. Kotecki; Donna K. Montavon; Steven C. Cullen. A General Method for Palladium-Catalyzed Reactions of Primary Sulfonamides with Aryl Nonaflates. J. Org. Chem. 2011, 76 (11): 4552–4563. ISSN 0022-3263. PMID 21510695. doi:10.1021/jo200443u.
- ^ Uemura, Minoru; Hideki Yorimitsu; Koichiro Oshima. Cp∗Li as a base: application to palladium-catalyzed cross-coupling reaction of aryl-X or alkenyl-X (X=I, Br, OTf, ONf) with terminal acetylenes. Tetrahedron. 2008-02-18, 64 (8): 1829–1833. ISSN 0040-4020. doi:10.1016/j.tet.2007.11.095. hdl:2433/88969
 .
.
- ^ Quek, Ser Kiang; Ilya M. Lyapkalo; Han Vinh Huynh. Synthesis and properties of N,N′-dialkylimidazolium bis(nonafluorobutane-1-sulfonyl)imides: a new subfamily of ionic liquids. Tetrahedron. 2006-03-27, 62 (13): 3137–3145. ISSN 0040-4020. doi:10.1016/j.tet.2006.01.015.
- ^ Hashmi, A. Stephen K.; Tobias Hengst; Christian Lothschütz; Frank Rominger. New and Easily Accessible Nitrogen Acyclic Gold(I) Carbenes: Structure and Application in the Gold-Catalyzed Phenol Synthesis as well as the Hydration of Alkynes. Advanced Synthesis & Catalysis. 2010, 352 (8): 1315–1337. ISSN 1615-4169. doi:10.1002/adsc.201000126.
