三磷酸鸟苷
| 三磷酸鸟苷 | |
|---|---|

| |

| |
| IUPAC名 ((2R,3S,4R,5R)-5-(2-amino-6-oxo-1,6-dihydro-9H-purin-9-yl)-3,4-dihydroxytetrahydrofuran-2-yl)methyl tetrahydrogen triphosphate | |
| 别名 | guanosine triphosphate, 9-β-D-ribofuranosylguanine-5'-triphosphate, 9-β-D-ribofuranosyl-2-amino-6-oxo-purine-5'-triphosphate |
| 识别 | |
| CAS号 | 86-01-1 |
| PubChem | 6830 |
| ChemSpider | 6569 |
| SMILES |
|
| InChI |
|
| InChIKey | XKMLYUALXHKNFT-UUOKFMHZBF |
| ChEBI | 15996 |
| KEGG | C00044 |
| MeSH | Guanosine+triphosphate |
| IUPHAR配体 | 1742 |
| 性质 | |
| 化学式 | C10H16N5O14P3 |
| 摩尔质量 | 523.18 g·mol−1 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
鳥苷-5'-三磷酸,簡稱鳥苷三磷酸或三磷酸鳥苷(英語:Guanosine triphosphate,縮寫:GTP),係一類嘌呤類核苷三磷酸。它可以在DNA複製期間的DNA轉錄過程中作爲RNA生物合成的底物。它的結構與含氮鹼基鳥嘌呤相似,唯一的不同是GTP連有一個核糖基團以及三個磷酸基團,其中,鳥嘌呤與核糖基團的1位碳相連,磷酸基團與核糖基團的5位碳相連。
另外,GTP還能在生物體代謝過程中作能量源或底物活化劑,這一點和ATP(三磷酸腺苷)相似,不過,它的專一性較強。GTP在蛋白質生物合成以及糖質新生過程中作能量源。
GTP在信號轉導過程中起不可或缺的作用,特別是和G蛋白作用時以及在第二信使機制中,在GTP酶的催化作用下,GTP會轉化爲GDP(二磷酸鳥苷)。
用途[编辑]
能量轉化[编辑]
GTP參與細胞中的能量轉化過程。比如,在三羧酸循環中,一種酶能產出GTP分子。這也相當於產生了一分子的ATP,因爲GTP能被核苷二磷酸激酶(NDK)轉化爲ATP分子[1]。
基因轉譯[编辑]
在轉譯過程中,GTP作爲氨酰tRNA與核糖體A位點結合、核糖體在mRNA上自5'端向3'端轉位等過程的能量源[2]。
微管動力學不穩定性[编辑]
在微管聚合過程中,每一個異質二聚體都由攜帶兩分子GTP的一個α和一個β微管蛋白分子生成。這些分子攜帶的GTP會在二聚體加到延伸中的微管正端時水解。上述GTP水解對微管生成並不是必须的,但似乎只有與GDP結合的微管蛋白可以解聚。因此,不難推測,一個GTP結合微管蛋白在微管尖端作爲一個「帽」來防止解聚。一旦這個GTP分子水解,微管就會開始解聚,並迅速縮短[3]。
線粒體功能[编辑]
蛋白質轉位進入線粒體基質的過程需要與GTP和ATP的相互作用。這些蛋白質的進入對線粒體內幾個調節通路來說至關重要[4]。
生物合成[编辑]
在細胞中,GTP能通過多種途徑合成:
- 作爲由琥珀酰輔酶A合成酶催化的琥珀酰輔酶A轉化爲琥珀酸過程(該過程是三羧酸循環的一部分)的副產物[1]。
- 通過ATP分子的磷酸基團轉換作用合成。該過程由核苷二磷酸激酶催化,該酶起到平衡不同的核苷三磷酸濃度的作用[1]。
cGTP[编辑]
在嗅覺系統中,cGTP(環鳥苷三磷酸)起到幫助cAMP(環腺苷酸)活化環核苷酸門控離子通道的作用[5]。
參見[编辑]
核糖核苷酸[编辑]
 單磷酸腺苷 AMP |
 二磷酸腺苷 ADP |
 三磷酸腺苷 ATP |
 單磷酸鳥苷 GMP |
 二磷酸鳥苷 GDP |
 三磷酸鳥苷 GTP |
 單磷酸胸苷 TMP |
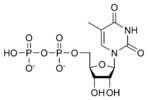 二磷酸胸苷 TDP |
 三磷酸胸苷 TTP |
 单磷酸尿苷 UMP |
 二磷酸尿苷 UDP |
 三磷酸尿苷 UTP |
 單磷酸胞苷 CMP |
 二磷酸胞苷 CDP |
 三磷酸胞苷 CTP |
脫氧核糖核苷酸[编辑]
 單磷酸脫氧腺苷 dAMP |
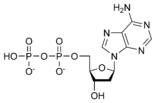 二磷酸脫氧腺苷 dADP |
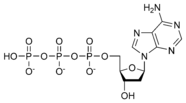 三磷酸脫氧腺苷 dATP |
 單磷酸脫氧鳥苷 dGMP |
 二磷酸脫氧鳥苷 dGDP |
 三磷酸脫氧鳥苷 dGTP |
 單磷酸脱氧胸苷 dTMP |
 二磷酸脱氧胸苷 dTDP |
 三磷酸脱氧胸苷 dTTP |
 單磷酸脫氧尿苷 dUMP |
 二磷酸脫氧尿苷 dUDP |
 三磷酸脫氧尿苷 dUTP |
 單磷酸脫氧胞苷 dCMP |
 二磷酸脫氧胞苷 dCDP |
 三磷酸脫氧胞苷 dCTP |
參考[编辑]
- ^ 1.0 1.1 1.2 Berg, JM; JL Tymoczko; L Stryer. Biochemistry 5th. WH Freeman and Company. 2002: 476. ISBN 0-7167-4684-0.
- ^ Solomon, EP; LR Berg; DW Martin. Biology 7th. 2005: 244–245.
- ^ Gwen V. Childs. Microtubule structure. cytochemistry.net. [2016-07-18]. (原始内容存档于2010-02-15).
- ^ Sepuri, Naresh Babu V.; Norbert Schülke; Debkumar Pain. GTP Hydrolysis Is Essential for Protein Import into the Mitochondrial Matrix. Journal of Biological Chemistry. 16 January 1998, (273): 1420–1424. doi:10.1074/jbc.273.3.1420.
- ^ Boron & Boulpaep. Medical Physiology Updated. Elsevier Saunders. 2005: 90. ISBN 1-4160-2328-3.
外部連結[编辑]
| 维基共享资源上的相关多媒体资源:三磷酸鸟苷 |
- GTP bound to proteins[失效連結] in the PDB
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
