高碘酸盐
| 高碘酸盐 | |
|---|---|

| |

| |
| 系统名 tetraoxoiodate(1−) hexaoxoiodate(5−) | |
| 识别 | |
| CAS号 | 15056-35-6(偏高碘酸盐) |
| PubChem | 167232(偏高碘酸盐) 6857432(原高碘酸盐) |
| ChemSpider | 146311 (偏高碘酸盐), 5256770 (原高碘酸盐) |
| SMILES |
|
| InChI |
|
| InChIKey | KHIWWQKSHDUIBK-UHFFFAOYSA-M(偏高碘酸盐) TWLXDPFBEPBAQB-UHFFFAOYSA-I(原高碘酸盐) |
| 性质 | |
| 化学式 | IO4−或IO65- |
| 相关物质 | |
| 其他阴离子 | 高氯酸盐 高溴酸盐 高锰酸盐 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
高碘酸根由碘和氧组成,是碘达到最高氧化态+7时形成含氧阴离子。不像高氯酸根等其它高卤酸根,高碘酸根有两种形态:偏高碘酸根(IO−
4)和 原高碘酸根(IO5−
6),这点与碲酸盐类似。高碘酸根可以和阳离子结合,形成高碘酸盐,也就是高碘酸的盐。
高碘酸盐是被海因里希·马格努斯和C. F. Ammermüller发现的。他们也在1833年发现了高碘酸。[1]
制备
[编辑]传统上,高碘酸盐最常以高碘酸氢钠(Na3H2IO6)的形式产生。[2]这是可商购的,但是也可以通过用氯和氢氧化钠来氧化碘酸盐来生产。[3]用溴代替氯来氧化碘化物也是可行的。
- NaIO3 + Cl2 + 4 NaOH → Na3H2IO6 + 2 NaCl + H2O
- NaI + 4 Br2 + 10 NaOH → Na3H2IO6 + 8 NaBr + 4 H2O
现代工业规模生产涉及在PbO2阳极上碘酸盐的电化学氧化,并具有以下标准电极电位:
偏高碘酸盐一般由硝酸来对高碘酸氢钠进行脱水而成的。[2]在 100 °C 的真空下,高碘酸氢钠也可以脱水成高碘酸盐。
- Na3H2IO6 + 2 HNO3 → NaIO4 + 2 NaNO3 + 2 H2O
- H5IO6 → HIO4 + 2 H2O
它们也可以由碘酸盐和次氯酸盐等强氧化剂反应而成:
形态和变化
[编辑]高碘酸盐可以以多种形式存在于水性介质中,其中pH是控制因素。原高碘酸盐具有许多酸解离常数。[5][6]
H5IO6 ⇌ H
4IO−
6+ H+ pKa = 3.29 H
4IO−
6⇌ H
3IO2−
6+ H+ pKa = 8.31 H
3IO2−
6⇌ H
2IO3−
6+ H+ pKa = 11.60
原高碘酸四氢根和偏高碘酸根存在平衡。
- H
4IO−
6 ⇌ IO−
4 + 2 H2O, K = 29
由于这个原因,原高碘酸盐经常被认为是偏高碘酸盐的二水合物,[来源请求]写作IO−
4·2H2O。但是,由于H5IO6的X射线晶体学结果显示它有5个一样的I-OH基团,因此该描述并不准确。[7]
在极端的pH值下,高碘酸盐可能会形成其他物质。在碱性条件下,高碘酸三氢盐会脱水形成二碘酸盐。
- 2 H
3IO2−
6 ⇌ H
2I
2O4−
10 + 2 H2O, K = 820
在超强酸下,高碘酸也会被质子化,形成六氢氧化碘阳离子。[8]
- H
6IO+
6 ⇌ H5IO6 + H+, pKa = −0.8
结构和成键
[编辑]不管是偏高碘酸根还是原高碘酸根,碘原子都处于超价状态,也就是可以形成超过符合八隅体规则所需要的键的数量的键。这可以用配位键进行了解释,也证实了这些分子中不存在双键。[9]
高碘酸根的真正结构就看阳离子是什么,但是平均而言,原高碘酸盐采用略有变形的八面体结构,X射线衍射显示I–O键长为1.89 Å。[10][7]偏高碘酸根的结构则是变形四面体, I–O 键长为 1.78 Å。[11][12]
反应
[编辑]热分解
[编辑]高碘酸盐在水热条件下进行热分解,可以用于制备碘酸盐:[13]
- 2 La(H2O)3{IO4(OH)2} + 4 H5IO6 → 2 La(IO3)3·1⁄2H2O + 3 O2 + 17 H2O
裂解反应
[编辑]高碘酸盐可以在各种1,2-双官能化烷烃上裂解碳-碳键。[14][15]最常见的例子是二醇裂解,它也是第一个被发现的(Malaprade反应)。[16] 除二醇外,高碘酸盐还可裂解1,2-羟酮,1,2-二酮,α-酮酸,α-羟酸,氨基酸,[17]1,2-胺醇,[18]1,2-二胺和[19]环氧化物[20]并形成醛,酮和羧酸。

烯烃也可以在Lemieux–Johnson氧化反应中被氧化和裂解。 这利用了四氧化锇的催化负载,该负载由高碘酸盐原位再生。 整个过程等同于臭氧化反应。
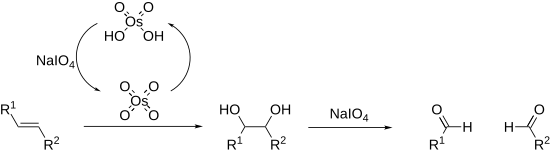
裂解反应涉及称为高碘酸酯的环状中间体。其形成可能受pH和温度的影响[21]但是底物的几何形状影响最大,顺式二醇的反应明显快于反式二醇。[22]反应是放热的,并且通常在0℃下进行。由于高碘酸盐仅易溶于水,因此反应通常在水性介质中进行。 在溶解度很重要的情况下,可以使用高碘酸,因为它可溶于醇。 相转移催化剂在多相液体混合物中反应也有效。 在极端情况下,高碘酸盐可能会交换四乙酸铅,后者以相似的方式反应并溶于有机溶剂(Criegee反应)。

高碘酸盐裂解通常在分子生物化学中用于修饰糖类环的目的,因为许多五元和六元糖具有邻位二醇。 从历史上看,它也被用来确定单糖的结构。[23][24]
高碘酸盐的裂解可以以工业规模进行,以形成在造纸中使用的二醛淀粉。[25]
氧化反应
[编辑]高碘酸盐都是强氧化剂。 它们可以氧化邻苯二酚成1,2-苯醌,把对苯二酚氧化成1,4-苯醌。[26]硫化物也会被它们氧化成亚砜。[27]高碘酸盐的氧化性很强,可以制备其它强氧化剂如:高锰酸盐,[28]四氧化锇[29] 和四氧化钌。
利基用途
[编辑]显微镜学中使用的几种染色剂基于高碘酸盐(例如PAS染色法和琼斯氏染色)。
高碘酸盐也已经用作烟火制造术中的氧化剂。[31]2013年,美国陆军宣布将用高碘酸钠替代对环境有害的化学物硝酸钡和高氯酸钾,用于示踪弹药。[32]
其它含氧阴离子
[编辑]高碘酸盐是碘的含氧阴离子之一。碘可以形成氧化态为−1(其实不是)、+1、+3、+5、+7的含氧阴离子。一系列中性的碘的氧化物也是已知的。
| 碘的氧化态 | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| 名字 | 碘化物 | 次碘酸盐 | 亚碘酸盐 | 碘酸盐 | 高碘酸盐 |
| 化学式 | I− | IO− | IO− 2 |
IO− 3 |
IO− 4 或 IO5− 6 |
| 结构 | 
|
参见
[编辑]参考资料
[编辑]- ^ Ammermüller, F.; Magnus, G. Ueber eine neue Verbindung des Jods mit Sauerstoff, die Ueberjodsäure. Annalen der Physik und Chemie. 1833, 104 (7): 514–525. Bibcode:1833AnP...104..514A. doi:10.1002/andp.18331040709 (德语).
- ^ 2.0 2.1 Riley, edited by Georg Brauer; translated by Scripta Technica, Inc. Translation editor Reed F. Handbook of preparative inorganic chemistry. Volume 1 2nd. New York, N.Y.: Academic Press. 1963: 323–324. ISBN 012126601X.
- ^ Hill, Arthur E. Ternary Systems. VII. The Periodates of the Alkali Metals. Journal of the American Chemical Society. October 1928, 50 (10): 2678–2692. doi:10.1021/ja01397a013.
- ^ Parsons, Roger. Handbook of electrochemical constants. Butterworths Scientific Publications Ltd. 1959: 71.
- ^ Aylett, founded by A.F. Holleman; continued by Egon Wiberg; translated by Mary Eagleson, William Brewer; revised by Bernhard J. Inorganic chemistry 1st English ed., [edited] by Nils Wiberg. San Diego, Calif.: Berlin: Academic Press, W. de Gruyter. 2001: 454. ISBN 0123526515.
- ^ Burgot, Jean-Louis. Ionic equilibria in analytical chemistry. New York: Springer. : 358. ISBN 1441983821.
- ^ 7.0 7.1 Feikema, Y. D. The crystal structures of two oxy-acids of iodine. I. A study of orthoperiodic acid, H5IO6, by neutron diffraction. Acta Crystallographica. 1966, 20 (6): 765–769. doi:10.1107/S0365110X66001828.
- ^ Greenwood, N.N.; Earnshaw, A. Chemistry of the elements
 2nd. Oxford: Butterworth-Heinemann. 2006: 874. ISBN 0750633654.
2nd. Oxford: Butterworth-Heinemann. 2006: 874. ISBN 0750633654.
- ^ Ivanov, A.; Popov, A.; Boldyrev, A.; Zhdankin, V. The I=X (X = O,N,C) Double Bond in Hypervalent Iodine Compounds: Is it Real?. Angew. Chem. Int. Ed. 2014, 53: 9617–9621. doi:10.1002/anie.201405142.
- ^ Tichý, K.; Rüegg, A.; Beneš, J. Neutron diffraction study of diammonium trihydrogen periodate, (NH4)2H3IO6, and its deuterium analogue, (ND4)2D3IO6. Acta Crystallographica Section B. 1980, 36 (5): 1028–1032. doi:10.1107/S0567740880005225.
- ^ Levason, W.; Webster, M. Ammonium tetraoxoiodate(VII). Acta Crystallographica Section C. 15 June 1999, 55 (6): IUC9900052. doi:10.1107/S0108270199099394
 .
.
- ^ Kálmán, A.; Cruickshank, D. W. J. Refinement of the structure of NaIO4. Acta Crystallographica Section B. 1970, 26 (11): 1782–1785. doi:10.1107/S0567740870004880.
- ^ Hector, Andrew L.; Henderson, Stuart J.; Levason, William; Webster, Michael. Hydrothermal Synthesis of Rare Earth Iodates from the Corresponding Periodates: Structures of Sc(IO3)3, Y(IO3)3 · 2 H2O, La(IO3)3 · 1/2 H2O and Lu(IO3)3 · 2 H2O. Zeitschrift für anorganische und allgemeine Chemie. 2002, 628 (1): 198–202. ISSN 0044-2313. doi:10.1002/1521-3749(200201)628:1<198::AID-ZAAC198>3.0.CO;2-L (德语).
- ^ Sklarz, B. Organic chemistry of periodates. Quarterly Reviews, Chemical Society. 1967, 21 (1): 3. doi:10.1039/QR9672100003.
- ^ Bamford, edited by C.H.; Tipper, C.F.H. Reactions of non-metallic inorganic compounds. Amsterdam: Elsevier Pub. Co. 1972: 435. ISBN 9780080868011.
- ^ L. Malaprade, Bull. Soc. Chim. Fr. 3, 1, 833 (1934)
- ^ Clamp, J.R.; Hough, L. The Periodate Oxidation of Amino Acids with Reference to Studies on Glycoproteins.. The Biochemical Journal. Jan 1965, 94: 17–24. PMC 1206400
 . PMID 14342227. doi:10.1042/bj0940017.
. PMID 14342227. doi:10.1042/bj0940017.
- ^ Nicolet, Ben H.; Shinn, Leo A. THE ACTION OF PERIODIC ACID ON α-AMINO ALCOHOLS. Journal of the American Chemical Society. June 1939, 61 (6): 1615–1615. doi:10.1021/ja01875a521.
- ^ Maros, László; Molnár-Perl, Ibolya; Schissel, Enikó; Szerdahelyi, Vilmos. Mechanism of the periodate oxidation of ethane-1,2-diamine, N,N′-dimethylethane-1,2-diamine, and 2-aminoethanol. Journal of the Chemical Society, Perkin Transactions 2. 1980, (1): 39. doi:10.1039/P29800000039.
- ^ Telvekar, Vikas N.; Patel, Dharmeshkumar J.; Mishra, Sanket J. Oxidative Cleavage of Epoxides Using Aqueous Sodium Paraperiodate. Synthetic Communications: 311–315. doi:10.1080/00397910802372574.
- ^ Buist, G. J.; Bunton, C. A.; Hipperson, W. C. P. The mechanism of oxidation of α-glycols by periodic acid. Part X. The oxidation of pinacol, and a general discussion of the stability of periodate esters and their role in the mechanism of oxidation. Journal of the Chemical Society B: Physical Organic. 1971: 2128. doi:10.1039/J29710002128.
- ^ McMurry, John. Organic chemistry
 8th ed., [international ed.] Singapore: Brooks/Cole Cengage Learning. 2012: 312. ISBN 084005453X.
8th ed., [international ed.] Singapore: Brooks/Cole Cengage Learning. 2012: 312. ISBN 084005453X.
- ^ Jackson, Ernest L.; Hudson, C. S. Studies on the Cleavage of the Carbon Chain of Glycosides by Oxidation. A New Method for Determining Ring Structures and Alpha and Beta Configurations of Glycosides. Journal of the American Chemical Society. June 1937, 59 (6): 994–1003. doi:10.1021/ja01285a010.
- ^ Robyt, John F. Essentials of carbohydrate chemistry. New York: Springer. 1998. ISBN 0387949518.
- ^ Yu, Jiugao; Chang, Peter R.; Ma, Xiaofei. The preparation and properties of dialdehyde starch and thermoplastic dialdehyde starch. Carbohydrate Polymers. January 2010, 79 (2): 296–300. doi:10.1016/j.carbpol.2009.08.005.
- ^ Weidman, S. W.; Kaiser, E. T. The Mechanism of the Periodate Oxidation of Aromatic Systems. III. A Kinetic Study of the Periodate Oxidation of Catechol. Journal of the American Chemical Society. December 1966, 88 (24): 5820–5827. doi:10.1021/ja00976a024.
- ^ Leonard, Nelson J.; Johnson, Carl R. Periodate Oxidation of Sulfides to Sulfoxides. Scope of the Reaction. The Journal of Organic Chemistry. January 1962, 27 (1): 282–284. doi:10.1021/jo01048a504.
- ^ Lemieux, R. U.; Rudloff, E. Von. Periodate–Permanganate Oxidations: I. Oxidation of Olefins. Canadian Journal of Chemistry. November 1955, 33 (11): 1701–1709. doi:10.1139/v55-208.
- ^ Pappo, R.; Allen, Jr., D. S.; Lemieux, R. U.; Johnson, W. S. Notes - Osmium Tetroxide-Catalyzed Periodate Oxidation of Olefinic Bonds. The Journal of Organic Chemistry. 1956, 21 (4): 478–479. ISSN 0022-3263. doi:10.1021/jo01110a606.
- ^ Weber, Dieter; Vőfély, Róza; Chen, Yuehua; Mourzina, Yulia; Poppe, Ulrich. Variable resistor made by repeated steps of epitaxial deposition and lithographic structuring of oxide layers by using wet chemical etchants. Thin Solid Films. 2013, 533: 43–47. doi:10.1016/j.tsf.2012.11.118
 .
.
- ^ Moretti, Jared D.; Sabatini, Jesse J.; Chen, Gary. Periodate Salts as Pyrotechnic Oxidizers: Development of Barium- and Perchlorate-Free Incendiary Formulations. Angewandte Chemie International Edition. 9 July 2012, 51 (28): 6981–6983. PMID 22639415. doi:10.1002/anie.201202589.
- ^ Picatinny to remove tons of toxins from lethal rounds. U.S. Army. [31 October 2013]. (原始内容存档于2016-10-09).
