层粘连蛋白



层粘连蛋白(英语:laminin)是细胞外基质的高分子量(~400至~900kDa)糖蛋白。它们是基底层(基底膜的一层)的主要成分,是大多数细胞和器官的一个蛋白质网络基础。层粘连蛋白是基底层的重要和生物活性部分,影响细胞分化,迁移和黏附[1][2]。
层粘连蛋白是由三条不同的肽链(α-链,β-链,γ-链)组成异源三聚体,外形似不对称十字架,呈一条长臂(三链螺旋)和三条短臂(单链),末端均为球状。其α-链,β-链和γ-链分别有五种,四种和三种遗传变体。层粘连蛋白分子根据其链组成命名。例如层粘连蛋白-511含有α5,β1和γ1链[3]。
三聚体蛋白相交形成十字形结构,可以与其他细胞膜和细胞外基质分子结合[4]。三个较短的臂特别擅长与其他层粘连蛋白分子结合,这允许它们形成片。长臂能够与细胞结合,这有助于将有组织的组织细胞锚定到膜上。
层粘连蛋白家族的糖蛋白是生物体几乎每个组织中结构支架的组成部分。 它们被分泌并掺入细胞相关的细胞外基质中。 层粘连蛋白对组织的维持和存活至关重要。 有缺陷的层粘连蛋白可导致肌肉形成不当,导致肌肉营养不良,致命的皮肤水疱病(交界性大疱性表皮松解症)和肾脏过滤器(肾病症候群)的缺陷[5]。
类型
[编辑]分子生物学家已经鉴定了15种层粘连蛋白三聚体。层粘连蛋白是不同的α-,β-和γ-链的组合[6]。
- 五种形式的α-链是:LAMA1,LAMA2,LAMA3(具有三种剪接形式),LAMA4,LAMA5
- β-链包括:LAMB1,LAMB2,LAMB3,LAMB4(注意,没有已知的层粘连蛋白三聚体包含LAMB4,其功能仍然知之甚少)
- γ链是:LAMC1,LAMC2,LAMC3
层粘连蛋白先前已经被发现,即层粘连蛋白-1,层粘连蛋白-2,层粘连蛋白-3等,但是命名法被改变以描述每种同种型中存在哪些链(层粘连蛋白-111,层粘连蛋白-211等)[3]。 此外,许多层粘连蛋白在层粘连蛋白命名法到位之前具有俗名(common names)[7][8]。
| 旧的命名法 | 旧同义词 | 链组成 | 新的命名法 |
|---|---|---|---|
| Laminin-1 | EHS laminin | α1β1γ1 | Laminin-111 |
| Laminin-2 | Merosin | α2β1γ1 | Laminin-211 |
| Laminin-3 | S-laminin | α1β2γ1 | Laminin-121 |
| Laminin-4 | S-merosin | α2β2γ1 | Laminin-221 |
| Laminin-5 / Laminin-5A | Kalinin, epiligrin, nicein, ladsin | α3Aβ3γ2 | Laminin-332 / Laminin-3A32 |
| Laminin-5B | α3Bβ3γ2 | Laminin-3B32 | |
| Laminin-6 / Laminin-6A | K-laminin | α3Aβ1γ1 | Laminin-311 / Laminin-3A11 |
| Laminin-7 / Laminin-7A | KS-laminin | α3Aβ2γ1 | Laminin-321 / Laminin-3A21 |
| Laminin-8 | α4β1γ1 | Laminin-411 | |
| Laminin-9 | α4β2γ1 | Laminin-421 | |
| Laminin-10 | Drosophila-like laminin | α5β1γ1 | Laminin-511 |
| Laminin-11 | α5β2γ1 | Laminin-521 | |
| Laminin-12 | α2β1γ3 | Laminin-213 | |
| Laminin-14 | α4β2γ3 | Laminin-423 | |
| α5β2γ2 | Laminin-522 | ||
| Laminin-15 | α5β2γ3 | Laminin-523 |
功能
[编辑]层粘连蛋白形成独立的网络,并通过entactin的IV型胶原蛋白网络[9],纤连蛋白[10],和perlecan相关。 它们还通过整合素受体和其他质膜分子与细胞膜结合,如dystroglycan糖蛋白复合物和Lutheran血型糖蛋白[4]。 通过这些相互作用,层粘连蛋白有助于细胞附着和分化,细胞形状和运动,维持组织表型,促进组织存活[4][6]。 层粘连蛋白的这些生物学功能中的一些与特定的氨基酸序列或层粘连蛋白的片段有关[4]。 例如,位于层粘连蛋白α链上的肽序列[GTFALRGDNGDNGQ]促进内皮细胞的黏附[11]。
层粘连蛋白α4分布在多种组织中,包括周围神经系统,背根神经节,骨骼肌和毛细血管; 在神经肌肉接点处,它是突触专业化所必需的[12]。 层粘连蛋白-G结构域的结构已经被预测类似于五聚蛋白[13]。
在神经发育中的作用
[编辑]层粘连蛋白-111是神经轴突将在体内和体外生长的主要底物。 例如,它奠定了发展视网膜神经节细胞从视网膜到顶盖的途径。 它也经常用作细胞培养实验中的底物。
在周围神经修复中的作用
[编辑]层粘连蛋白在周围神经损伤后在损伤部位富集并由施旺细胞分泌。 周围神经系统的神经元表达整合素受体,其附着于层粘连蛋白并在损伤后促进神经再生[14]。
病理
[编辑]一种特定层粘连蛋白,层粘连蛋白-211的功能失调结构是一种形式的先天性肌营养不良的原因[15]。 层粘连蛋白-211由α2,β1和γ1链组成。 这种层粘连蛋白的分布包括大脑和肌肉纤维。 在肌肉中,它通过G结构域与α-dystroglycan和整合素α7-β1结合,并且通过另一端与细胞外基质结合。
上皮细胞黏附到基底膜所必需的层粘连蛋白-332异常,导致称为交界性大疱性表皮松解症的病症,其特征在于全身性水疱,皮肤和粘膜的旺盛肉芽组织,以及凹陷的牙齿。
肾脏过滤器中的功能性层粘连蛋白-521导致蛋白质渗漏到尿液中和肾病症候群[5]。
层粘连蛋白质结构域
[编辑]| Laminin Domain I | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 鉴定 | |||||||||
| 标志 | Laminin_I | ||||||||
| Pfam | PF06008(旧版) | ||||||||
| InterPro | IPR009254 | ||||||||
| |||||||||
| Laminin Domain II | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 鉴定 | |||||||||
| 标志 | Laminin_II | ||||||||
| Pfam | PF06009(旧版) | ||||||||
| InterPro | IPR010307 | ||||||||
| |||||||||
| Laminin B (Domain IV) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 鉴定 | |||||||||
| 标志 | Laminin_B | ||||||||
| Pfam | PF00052(旧版) | ||||||||
| InterPro | IPR000034 | ||||||||
| |||||||||
| Laminin EGF-like (Domains III and V) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 crystal structure of three consecutive laminin-type epidermal growth factor-like (le) modules of laminin gamma1 chain harboring the nidogen binding site | |||||||||
| 鉴定 | |||||||||
| 标志 | Laminin_EGF | ||||||||
| Pfam | PF00053(旧版) | ||||||||
| Pfam宗系 | CL0001(旧版) | ||||||||
| InterPro | IPR002049 | ||||||||
| PROSITE | PDOC00021 | ||||||||
| SCOP | 1tle / SUPFAM | ||||||||
| |||||||||
| Laminin G domain | |||||||||
|---|---|---|---|---|---|---|---|---|---|
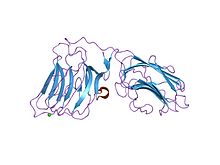 laminin alpha 2 chain lg4-5 domain pair, ca1 site mutant | |||||||||
| 鉴定 | |||||||||
| 标志 | Laminin_G_1 | ||||||||
| Pfam | PF00054(旧版) | ||||||||
| Pfam宗系 | CL0004(旧版) | ||||||||
| InterPro | IPR012679 | ||||||||
| SCOP | 1qu0 / SUPFAM | ||||||||
| |||||||||
| Laminin G domain | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 the structure of the ligand-binding domain of neurexin 1beta: regulation of lns domain function by alternative splicing | |||||||||
| 鉴定 | |||||||||
| 标志 | Laminin_G_2 | ||||||||
| Pfam | PF02210(旧版) | ||||||||
| Pfam宗系 | CL0004(旧版) | ||||||||
| InterPro | IPR012680 | ||||||||
| SMART | TSPN | ||||||||
| |||||||||
| Laminin N-terminal (Domain VI) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 鉴定 | |||||||||
| 标志 | Laminin_N | ||||||||
| Pfam | PF00055(旧版) | ||||||||
| Pfam宗系 | CL0202(旧版) | ||||||||
| InterPro | IPR008211 | ||||||||
| SMART | LamNT | ||||||||
| SCOP | 1klo / SUPFAM | ||||||||
| |||||||||
结构域I和结构域II
[编辑]层粘连蛋白是三聚体分子; 层粘连蛋白-1是α1β1γ1三聚体(Protein trimer)。 已经提出,来自层粘连蛋白A,B1和B2的结构域I和II可以聚集在一起形成三卷曲螺旋的螺旋结构[16]。
层粘连蛋白B结构域
[编辑]层粘连蛋白B结构域(也称为结构域IV)是功能未知的胞外(extracellular)模块。 它存在于许多不同的蛋白质中,包括来自基底膜的硫酸乙酰肝素蛋白聚糖,来自秀丽隐杆线虫的层粘连蛋白样蛋白质和层粘连蛋白。 在短层粘连蛋白链(α4或β3)中未发现层粘连蛋白IV结构域。
EGF样结构域
[编辑]除了不同类型的球状结构域外,每个层粘连蛋白亚基在其前半部分含有长度约为60个氨基酸的连续重复序列,其中包括8个保守的半胱氨酸[17]。该结构域的三级结构在N端与EGF样结构域模块的三级结构相似[18][19]。 它也被称为'LE'或'层粘连蛋白型EGF样'结构域。 不同形式的层粘连蛋白中层粘连蛋白EGF样结构域的拷贝数量是高度可变的; 从3份至22份拷贝数量已被发现。在小家鼠的层粘连蛋白γ-1链中,第七个LE结构域已被证明是唯一一个与巢蛋白具有高亲和力结合的结构域[20]。 结合位点位于环C1-C3和C5-C6内的表面上[18][19]。 层粘连蛋白中长的连续层粘连蛋白EGF样结构域形成有限柔韧性的棒状元件,这决定了基底膜层粘连蛋白网络形成的空间间隔[21][22]。
含有层粘连蛋白结构域的人类蛋白
[编辑]层粘连蛋白结构域I
[编辑]LAMA1; LAMA2; LAMA3; LAMA4; LAMA5;
层粘连蛋白结构域II
[编辑]LAMA1; LAMA2; LAMA3; LAMA4; LAMA5;
层粘连蛋白EGF样结构域(结构域III和V)
[编辑]AGRIN; ATRN; ATRNL1; CELSR1; CELSR2; CELSR3; CRELD1; HSPG2; LAMA1; LAMA2; LAMA3; LAMA4; LAMA5; LAMB1; LAMB2; LAMB3; LAMB4; LAMC1; LAMC2; LAMC3; MEGF10; MEGF12; MEGF6; MEGF8; MEGF9; NSR1; NTN1; NTN2L; NTN4; NTNG1; NTNG2; RESDA1; SCARF1; SCARF2; SREC; STAB1; USH2A;
层粘连蛋白G结构域(结构域IV)
[编辑]AGRIN; CELSR1; CELSR2; CELSR3; CNTNAP1; CNTNAP2; CNTNAP3; CNTNAP3B; CNTNAP4; CNTNAP5; COL11A1; COL11A2; COL12A1; COL14A1; COL15A1; COL16A1; COL18A1; COL19A1; COL20A1; COL21A1; COL22A1; COL24A1; COL27A1; COL5A1; COL5A3; COL9A1; CRB1; CRB2; CSPG4; EGFLAM; EYS; FAT; FAT2; FAT3; FAT4; GAS6; HSPG2; LAMA1; LAMA2; LAMA3; LAMA4; LAMA5; NELL1; NELL2; NRXN1; NRXN2; NRXN3; PROS1; SLIT1; SLIT2; SLIT3; SPEAR; THBS1; THBS2; THBS3; THBS4; USH2A;
层粘连蛋白N端(结构域VI)
[编辑]LAMA1; LAMA2; LAMA3; LAMA5; LAMB1; LAMB2; LAMB3; LAMB4; LAMC1; LAMC3; NTN1; NTN2L; NTN4; NTNG1; NTNG2; USH2A;
参阅
[编辑]参考资料
[编辑]- ^ Timpl R, Rohde H, Robey PG, Rennard SI, Foidart JM, Martin GR. Laminin--a glycoprotein from basement membranes. The Journal of Biological Chemistry. October 1979, 254 (19): 9933–7. PMID 114518.
- ^ DOI 10.1007/s00441-009-0838-2
- ^ 3.0 3.1 Aumailley M, Bruckner-Tuderman L, Carter WG, Deutzmann R, Edgar D, Ekblom P, Engel J, Engvall E, Hohenester E, Jones JC, Kleinman HK, Marinkovich MP, Martin GR, Mayer U, Meneguzzi G, Miner JH, Miyazaki K, Patarroyo M, Paulsson M, Quaranta V, Sanes JR, Sasaki T, Sekiguchi K, Sorokin LM, Talts JF, Tryggvason K, Uitto J, Virtanen I, von der Mark K, Wewer UM, Yamada Y, Yurchenco PD. A simplified laminin nomenclature. Matrix Biology. August 2005, 24 (5): 326–32. PMID 15979864. doi:10.1016/j.matbio.2005.05.006.
- ^ 4.0 4.1 4.2 4.3 M. A. Haralson; John R. Hassell. Extracellular matrix: a practical approach. Ithaca, N.Y: IRL Press. 1995. ISBN 0-19-963220-0.
- ^ 5.0 5.1 Yurchenco PD, Patton BL. Developmental and pathogenic mechanisms of basement membrane assembly. Current Pharmaceutical Design. 2009, 15 (12): 1277–94. PMC 2978668
 . PMID 19355968. doi:10.2174/138161209787846766.
. PMID 19355968. doi:10.2174/138161209787846766.
- ^ 6.0 6.1 Colognato H, Yurchenco PD. Form and function: the laminin family of heterotrimers. Developmental Dynamics. June 2000, 218 (2): 213–34. PMID 10842354. doi:10.1002/(SICI)1097-0177(200006)218:2<213::AID-DVDY1>3.0.CO;2-R.
- ^ Royce, Peter M. (编). Connective tissue and its heritable disorders: molecular, genetic, and medical aspects 2nd. New York: Wiley-Liss. 2002: 306 [2018-11-06]. ISBN 9780471251859. (原始内容存档于2018-11-06).
- ^ Kühn, Klaus. Extracellular matrix constituents as integrin ligands. Elbe, Johannes A. (编). Integrin-ligand interaction. New York: Chapman & Hall. 1997: 50 [2018-11-06]. ISBN 9780412138614. (原始内容存档于2018-11-06).
- ^ Smith J, Ockleford CD. Laser scanning confocal examination and comparison of nidogen (entactin) with laminin in term human amniochorion. Placenta. January 1994, 15 (1): 95–106. PMID 8208674. doi:10.1016/S0143-4004(05)80240-1.
- ^ Ockleford C, Bright N, Hubbard A, D'Lacey C, Smith J, Gardiner L, Sheikh T, Albentosa M, Turtle K. Micro-trabeculae, macro-plaques or mini-basement membranes in human term fetal membranes?. Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. October 1993, 342 (1300): 121–36 [2018-11-06]. doi:10.1098/rstb.1993.0142. (原始内容存档于2018-11-07).
- ^ Beck et al., 1999.[需要明确引用]
- ^ Ichikawa N, Kasai S, Suzuki N, Nishi N, Oishi S, Fujii N, Kadoya Y, Hatori K, Mizuno Y, Nomizu M, Arikawa-Hirasawa E. Identification of neurite outgrowth active sites on the laminin alpha4 chain G domain. Biochemistry. April 2005, 44 (15): 5755–62. PMID 15823034. doi:10.1021/bi0476228.
- ^ Beckmann G, Hanke J, Bork P, Reich JG. Merging extracellular domains: fold prediction for laminin G-like and amino-terminal thrombospondin-like modules based on homology to pentraxins. Journal of Molecular Biology. February 1998, 275 (5): 725–30. PMID 9480764. doi:10.1006/jmbi.1997.1510.
- ^ Nieuwenhuis, B.; Haenzi, B.; Andrews, M. R.; Verhaagen, J.; Fawcett, J. W. Integrins promote axonal regeneration after injury of the nervous system. Biological Reviews. 2018. doi:10.1111/brv.12398.
- ^ Hall TE, Bryson-Richardson RJ, Berger S, Jacoby AS, Cole NJ, Hollway GE, Berger J, Currie PD. The zebrafish candyfloss mutant implicates extracellular matrix adhesion failure in laminin alpha2-deficient congenital muscular dystrophy. Proceedings of the National Academy of Sciences of the United States of America. April 2007, 104 (17): 7092–7. PMC 1855385
 . PMID 17438294. doi:10.1073/pnas.0700942104.
. PMID 17438294. doi:10.1073/pnas.0700942104.
- ^ Sasaki M, Kleinman HK, Huber H, Deutzmann R, Yamada Y. Laminin, a multidomain protein. The A chain has a unique globular domain and homology with the basement membrane proteoglycan and the laminin B chains. The Journal of Biological Chemistry. November 1988, 263 (32): 16536–44. PMID 3182802.
- ^ Engel J. EGF-like domains in extracellular matrix proteins: localized signals for growth and differentiation?. FEBS Letters. July 1989, 251 (1-2): 1–7. PMID 2666164. doi:10.1016/0014-5793(89)81417-6.
- ^ 18.0 18.1 Stetefeld J, Mayer U, Timpl R, Huber R. Crystal structure of three consecutive laminin-type epidermal growth factor-like (LE) modules of laminin gamma1 chain harboring the nidogen binding site. Journal of Molecular Biology. April 1996, 257 (3): 644–57. PMID 8648630. doi:10.1006/jmbi.1996.0191.
- ^ 19.0 19.1 Baumgartner R, Czisch M, Mayer U, Pöschl E, Huber R, Timpl R, Holak TA. Structure of the nidogen binding LE module of the laminin gamma1 chain in solution. Journal of Molecular Biology. April 1996, 257 (3): 658–68. PMID 8648631. doi:10.1006/jmbi.1996.0192.
- ^ Mayer U, Pöschl E, Gerecke DR, Wagman DW, Burgeson RE, Timpl R. Low nidogen affinity of laminin-5 can be attributed to two serine residues in EGF-like motif gamma 2III4. FEBS Letters. May 1995, 365 (2-3): 129–32. PMID 7781764. doi:10.1016/0014-5793(95)00438-F.
- ^ Beck K, Hunter I, Engel J. Structure and function of laminin: anatomy of a multidomain glycoprotein. FASEB Journal. February 1990, 4 (2): 148–60. PMID 2404817.
- ^ Yurchenco PD, Cheng YS. Self-assembly and calcium-binding sites in laminin. A three-arm interaction model. The Journal of Biological Chemistry. August 1993, 268 (23): 17286–99. PMID 8349613.
