曼尼希反應
| 曼尼希反應 | |
|---|---|
| 命名根據 | 卡爾·曼尼希 |
| 反應類型 | 偶聯反應 |
| 標識 | |
| 有機化學網站對應網頁 | mannich-reaction |
| RSC序號 | RXNO:0000032 |
曼尼希反應(Mannich反應,簡稱曼氏反應),也稱作胺甲基化反應,是含有活潑氫的化合物(通常為羰基化合物)與甲醛和二級胺或氨縮合,生成β-氨基(羰基)化合物的有機化學反應。一般醛亞胺與α-亞甲基羰基化合物的反應也被看做曼尼希反應。反應的產物β-氨基(羰基)化合物稱為「曼尼希鹼」(Mannich鹼),簡稱曼氏鹼。

反應中的胺一般為二級胺,如哌啶、二甲胺等。如果用一級胺,反應後的縮合產物在氮上還有氫,可以繼續發生反應,故有時也可根據需要使用一級胺。如果用三級胺或芳香胺,反應中無法生成亞胺離子,停留在季銨離子一步。
胺/氨的作用是活化另一個反應物醛。甲醛是最常用的醛,一般用它的水溶液、三聚甲醛或多聚甲醛。除甲醛外,也可用其他醛。反應一般在水、乙酸或醇中進行,加入少量鹽酸以保證酸性。
含α-氫的化合物一般為羰基化合物(醛、酮、羧酸、酯)、腈、脂肪硝基化合物、末端炔烴、α-烷基吡啶或亞胺等。若用不對稱的酮,則產物是混合物。呋喃、吡咯、噻吩等雜環化合物也可反應。
曼氏反應通常需在高溫下和質子溶劑中進行,反應時間長,容易生成副產物。
歷史
[編輯]早在1895年便有人發現以酚作酸組分的曼尼希鹼,並申請了專利。[1] 之後,Tollens[2]、L. Henry、Duden、Franchimont等人發現了其他類型的曼尼希反應,包括以硝基烷和伯硝胺作酸組分的反應,但都沒有意識到這些反應所具有的普遍意義。1912年,卡爾·曼尼希用沙利比林和烏洛托品反應,得到了一個難溶於水的沉澱。此產物的結構在一年內得到了解釋,[3] 促使了他對這一類含活潑氫化合物、甲醛和胺之間的反應進行了深入的研究,從而奠定了曼尼希反應的基礎。很多生物鹼都是通過曼尼希反應合成的。
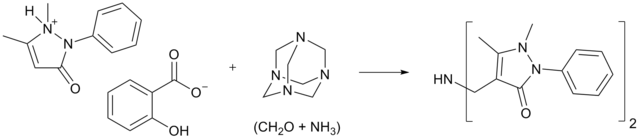
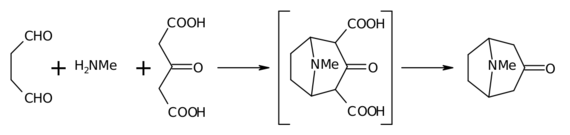
托品酮的合成是曼尼希反應的經典例子,被認為是全合成中的經典反應之一。1901年,Willstätter首先合成了這個化合物,用的是環庚酮作原料,通過14步反應,總產率僅為0.75%。1917年,羅伯特·魯賓遜以丁二醛、甲胺和3-氧代戊二酸為原料,在仿生條件下,利用了曼尼希反應,僅通過一步反應便得到了托品酮。[4] 反應的初始產率為17%,後經改進可增至90%。[5] 反應示意見下圖,機理見 [1] (頁面存檔備份,存於互聯網檔案館)。
反應機理
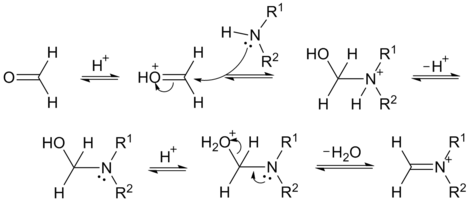
[編輯]反應的機理如下圖所示。羰基質子化,胺對羰基發生親核加成,去質子,氮上的電子轉移,水離去,可以得到一個亞胺離子中間體。以二甲胺作原料,這個中間體為N,N-二甲基-亞甲基氯化銨,在70年代由Kinact等人首先發現。它具有很強的反應性,可以使很多在通常條件下難以進行的反應得以順利進行。
亞胺離子作為親電試劑,進攻含活潑氫化合物的烯醇型結構,失去質子,便得到產物。

產物曼氏鹼比較穩定,以它作原料,經甲基化與Hofmann消除反應,或在蒸餾時和鹼作用下發生的分解反應,可以得到α,β-不飽和酮。後者可以與親核試劑發生米高加成等反應,是很有用的合成前體,但由於它一般不穩定,容易聚合,故通常採用曼氏鹼分解生成不飽和酮,並使其在原位與其它試劑發生反應。
不對稱曼尼希反應
[編輯]曼尼希反應會產生兩個原手性碳原子,因此產物是兩對對映異構體。可以經過手性誘導,使反應生成立體選擇性的產物。首個不對稱曼尼希反應於2002年報道,是以(S)-脯氨酸作手性催化劑的反應,如下圖所示。反應物醛上的取代基越大,syn型產物的比例越大。[6][2] (頁面存檔備份,存於互聯網檔案館)。

參見
[編輯]參考資料
[編輯]- ^ DRP, 89979; 90907 (1895); 90909 (1896).
- ^ Van Marle, C. M.; Tollens, B., Ber. dtsch. Chem. Ges., 36, 1351 (1903).
- ^ Mannich, C.; Krosche, W. Ueber ein Kondensationsprodukt aus Formaldehyd, Ammoniak und Antipyrin. Archiv der Pharmazie. 1912, 250: 647–667. doi:10.1002/ardp.19122500151.
- ^ Arthur J. Birch. Investigating a Scientific Legend: The Tropinone Synthesis of Sir Robert Robinson, F.R.S. Notes and Records of the Royal Society of London, 1993, 47, 277-296.
- ^ Smit, W. et al. (1998) Organic Synthesis, The Science behind the Art. Cambridge: The Royal Society of Chemistry.
- ^ Cordova, A.; Watanabe, S.; Tanaka, F.; Notz, W.; Barbas, C. F., III. A Highly Enantioselective Route to Either Enantiomer of Both α- and β-Amino Acid Derivatives. Journal of the American Chemical Society. 2002, 124 (9): 1866–1867. doi:10.1021/ja017833p.
