图书馆:氢化
{{expand|time=2011-05-22T01:18:25+00:00}}
{{Infobox industrial process
|name = 催化加氢
(Catalysed hydrogenation)
|image =
|caption =
|type = 化学
|sector = 食品工业,石油化工,制药工业,农业
|technologies = 各种过渡金属催化剂,高压反应技术
|feedstock = 未饱和底物及氢气或供氢体
|product = 饱和烃及其衍生物
|companies =
|facility =
|inventor = 保罗·萨巴捷
|year = 1897年
|developer =
}}
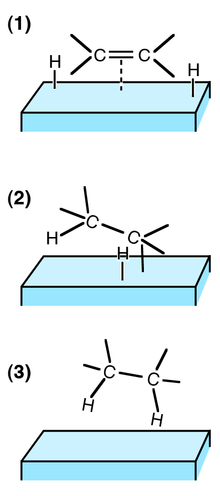
(1) 反应物吸附到催化剂表面,氢气解离
(2) 一个氢原子加成到双键的一个碳上,另一个碳原子仍附着在表面上
(3) 第二个碳原子加氢,产物分子离开催化剂表面
氢化也称为加氢,是一种用氢气和其他化合物反应的单元操作,通常发生在镍、钯、铂等催化剂表面。氢化通常用于还原未饱和的有机化合物或其他化合物。碳氢化合物的氢化可以还原掉分子中的双键和三键[1]。典型的氢化过程是烯烃加氢,有一分子的氢气加入烯烃分子中。由于氢气不活跃,通常必须有催化剂的存在才能反应,无催化剂的氢化过程只在高温下才发生。
氢化在化工生产中一般分为两种:
- 加氢——单纯增加有机化合物中氢原子的数目,使不饱和的有机物变为相对饱和的有机物,如将苯加氢生成环己烷以用于制造锦纶;将鱼油加氢制作硬化固体油以便与贮藏和运输;制造合成润滑油、肥皂、甘油的过程也是一种加氢过程。
- 氢解——同时将有机物分子进行破裂和增加氢原子。如将煤或重油经氢解,变成小分子液体状态的人造石油,经分馏可以获得人造汽油。
过程
[编辑]在氢化过程中有三种物质:作为底物的不饱和烷烃、氢气或者等价的供氢源和必要的催化剂。氢化还原反应发生的温度、压力取决于底物的种类和催化剂的活性。
相关及竞争反应
[编辑]氢化反应所需要的催化剂及反应条件也能让烯烃发生异构化反应,其构型会从顺式变为反式。这个过程在食品工业中很重要,因为加氢技术在食物里产生了大量的反式脂肪酸。
原有的化学键断裂,再加上一分子氢气的反应称为氢解。氢解可能会导致碳-碳键或碳-杂键断裂(杂原子可以是:氧、氮、硫或卤素)。氢化产物中的极性键可能是氢解产生的。
供氢源
[编辑]对于氢化过程,最直接的供氢源就是氢气,商业上氢气通常储存在加压的钢瓶中。工业上的氢化过程的压力通常是一个大气压以上,这时需要使用增压泵将钢瓶中的氢气升压到所需压力。工业上氢气的来源是碳氢化合物的蒸汽重整[2]。 许多不直接使用氢气的情况下,可以用像甲酸、异丙醇、二氢蒽这样的供氢剂作为供氢源。它们经脱氢反应生成二氧化碳、丙酮和蒽,并还原其他化合物。这样的反应称为转移加氢。
底物
[编辑]烯烃和炔烃加氢的一个重要特征是顺式加成。不论是均相催化还是非均相催化,反应都通过顺式加成机理进行,氢气从位阻最小的地方进攻[3]。加成反应可以在不同的官能团上进行:
| 底物 | 产物 | 备注 | 氢化热 (kJ/mol)[4] |
|---|---|---|---|
| R2C=CR'2 (烯烃) |
R2CHCHR'2 (烷烃) |
在人造奶油的生产中广泛应用 | −90 ~ −130 |
| RC≡CR' (炔烃) |
RCH2CH2R' (烷烃) |
部分加氢得到 cis-RHC=CHR' | −300 (加氢至饱和) |
| RCHO (醛) |
RCH2OH (伯醇) |
通常采用转移加氢 | −60 ~ −65 |
| R2CO (酮) |
R2CHOH (仲醇) |
通常采用转移加氢 | −60 ~ −65 |
| RCO2R' (酯) |
RCH2OH + R'OH (两种醇) |
常用于脂肪醇的生产 | −25 ~ −105 |
| RCO2H (羧酸) |
RCH2OH (伯醇) |
用于脂肪醇的生产 | −25 ~ −75 |
| RNO2 (硝基) |
RNH2 (胺) |
主要用于生产苯胺[5][6] | −550 |
催化剂
[编辑]除了少数情况下,在没有催化剂时,氢气不会和有机物反应。不饱和的反应底物会{{tsl|en|Chemisorption|化学吸附}}到催化剂表面,催化剂的大多数表面都被底物占据。在非均相催化反应中,氢气和催化剂表面形成键 (M-H),这样氢原子就能转移到已经吸附的底物上。铂钯铑和铷均是高活性的催化剂,可以在较低的温度压力下操作。贵金属催化剂虽然活性高,反应条件要求低,但价格太高。基于镍的非贵金属催化剂,如兰尼镍、{{tsl|en|Urushibara nickel|漆原镍}}等价格较低、更经济,但反应活性不高,需要在高温、高压下反应[7][8]。人们需要在反应活性(反应速度)与催化剂的成本以及使用高压设备的成本之间权衡,找到合适的平衡点。
催化剂通常按反应体系的相态分为两类:{{tsl|en|Homogeneous catalysis|均相催化}}和非均相催化。均相催化剂和反应物均溶解在溶剂中。而非均相催化剂是固体,悬浮在溶解有底物的溶剂中,或者与气体底物反应。
均相催化剂
[编辑]以下列出了有名的均相催化剂。这些催化剂都是配合物,可以同时活化氢气和不饱和底物。大多数情况下配合物含有铂系的金属,如铂、钌、铱等。
- 均相加氢催化剂和它们的前体
-
三(三苯基膦)二氯化钌(II)}} 是一种基于铑的预催化剂
-
Crabtree 催化剂}}是一种含依的高活性催化剂
-
Rh2Cl2(cod)2 是许多均相催化剂的前体
-
(S)-iPr-PHOX}} 是一种典型的螯合磷酸配体,用于不对称氢化反应
{{clear left}}

均相催化剂也用在不对成合成中,通过催化前手性底物加氢可以得到不对成的产物。这种方法最早的证明是铑催化的酰胺氢化反应,产物作为药物 L-DOPA 的前体[9]。为了实现不对称还原,催化剂使用手性二膦作为配体[10]。铑催化氢化也被应用于 S-metolachlor 除草剂的生产中,它使用了Josiphos 类型的配体(称为Xyliphos)[11]。从理论上讲,不对称氢化反应可以被手性非均相催化剂催化[12],但这种方法更多的是一种探索,而不是一项实用的技术。
设备
[编辑]对于氢化过程,化学工程师可以选择三大类设备:
- 常压间歇加氢
- 高温/高压间歇加氢[13]
- 流动加氢
常压加氢
[编辑]常压加氢是最原始的加氢方法。现在仍然用于教学用途。常压加氢通常在圆底烧瓶中进行,烧瓶口用橡胶圈密封,烧瓶内装有溶解的反应物和固体催化剂,并用氮气或氩气隔绝空气做保护气。氢气通过氢气球持续加入,并通过不断搅拌,以促进三相反应物反应。可以通过监视氢气球的变化或氢气的吸收来来判断氢气的消耗量,进而判断氢化反应的进行程度。通常使用盛有硫酸铜等有色液体的{{tsl|en|Sight glass|液位指示管|刻度管}}来测量氢气的吸收量,或使用带有刻度的反应器。
高温/高压加氢
[编辑]对于许多氢化反应,如去除保护基团的氢解反应和芳香体系的还原反应,常温常压下进行的十分缓慢,对于这种类型的反应一般使用高压系统。在这种情况下,催化剂添加到惰性氛围下的压力容器中,氢气直接从气瓶或实验室的供氢源加入体系中。加压的浆液体系通过机械摇动进行搅拌混合,或者使用旋转篮搅拌[13],也可以加热,让浆体自行混合,因为压力弥补了加热导致的气体溶解度的降低。
流动加氢
[编辑]流动加氢技术已经成为工业上的一种热门技术,工业应用规模也逐渐增加。该技术将氢气和稀释的溶解于溶液中的反应物连续地通过固定床催化剂。通过使用现有的高效液相色谱技术,系统允许压力从常压到加压至 {{convert|1450|psi|bar|abbr=on}},也可以提高反应温度。在实验室级的反应中,可以使用一系列预制的整装催化剂,使用时无需称重或去除失效的催化剂。
工业反应器
[编辑]工业上,催化加氢使用装有已负载催化剂的平推流反应器。操作温度、压力通常很高,具体的数值取决于催化剂的种类。相对于实验室内的催化剂,工业上催化剂在载体上的负载量很低,并且金属中添加了不同的助剂或使用混合金属来改善活性、选择性和稳定性。通常使用金属镍,因为镍相对其它贵金属是活性低、易于控制且价格便宜。
气液感应反应器(加氢器)也用于催化加氢[14]。
参考文献
[编辑]{{Reflist}}
外部链接
[编辑]{{wikiquote}}
- "The Magic of Hydro" Popular Mechanics, June 1931, pp. 107–109 {{Wayback|url=https://books.google.com/books?id=4OIDAAAAMBAJ&pg=-PA107 |date=20190608182632 }} —— 20世纪30年代,面向大众介绍石油加氢技术的早期文章。
{{Authority control}}
Category:加成反应 Category:均相催化 Category:化学工程 Category:产业制程 * Category:炼油 Category:油页岩技术 Category:合成燃料技术 Category:有机氧化还原反应
- ^ {{cite book|last=Hudlický|first=Miloš|title=Reductions in Organic Chemistry|publisher=American Chemical Society|year=1996|location=Washington, D.C.|pages=429|isbn=0-8412-3344-6}}
- ^ Paul N. Rylander, "Hydrogenation and Dehydrogenation" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. {{DOI|10.1002/14356007.a13_487}}
- ^ Advanced Organic Chemistry Jerry March 2nd Edition
- ^ Scott D. Barnicki "Synthetic Organic Chemicals" in Handbook of Industrial Chemistry and Biotechnology edited by James A. Kent, New York : Springer, 2012. 12th ed. {{ISBN|978-1-4614-4259-2}}.
- ^ {{cite journal | year = 2000 | title = Hydrogenation of nitrobenzene using polymer bound Ru(III) complexes as catalyst | url = | journal = Ind. Jr. of Chem. Tech. | volume = 7 | issue = | page = 280 }}
- ^ {{cite journal | last1 = Patel | first1 = D. R. | year = 1998 | title = Hydrogenation of nitrobenzene using polymer anchored Pd(II) complexes as catalyst | url = | journal = Journal of Molecular Catalysis | volume = 130 | issue = | page = 57 | doi=10.1016/s1381-1169(97)00197-0}}
- ^ {{OrgSynth|author=C. F. H. Allen and James VanAllan|title=m-Toylybenzylamine|collvol=3|collvolpages=827|year=1955 |prep=CV3P0827}}
- ^ {{OrgSynth|author=A. B. Mekler, S. Ramachandran, S. Swaminathan, and Melvin S. Newman|title=2-Methyl-1,3-Cyclohexanedione|collvol=5|collvolpages=743|year=1973|prep=CV5P0743}}
- ^ {{cite journal|last1=Knowles|first1=W. S.|title=Application of organometallic catalysis to the commercial production of L-DOPA|url=https://archive.org/details/sim_journal-of-chemical-education_1986-03_63_3/page/222%7Cjournal=Journal of Chemical Education|date=March 1986|volume=63|issue=3|pages=222|doi=10.1021/ed063p222|bibcode=1986JChEd..63..222K}}
- ^ {{cite book|last1=Atkins|first1=Peter W.|title=Shriver & Atkins' inorganic chemistry.|date=2010|publisher=W. H. Freeman and Co.|location=New York|isbn=978-1-4292-1820-7|page=696|edition=5th}}
- ^ {{cite journal|last1=Blaser|first1=Hans-Ulrich|last2=Pugin|first2=Benoît|last3=Spindler|first3=Felix|last4=Thommen|first4=Marc|title=From a Chiral Switch to a Ligand Portfolio for Asymmetric Catalysis|journal=Accounts of Chemical Research|date=December 2007|volume=40|issue=12|pages=1240–1250|doi=10.1021/ar7001057}}
- ^ {{cite journal | doi = 10.1021/cr0683663 | title = Asymmetric Catalysis at Chiral Metal Surfaces | year = 2007 | last1 = Mallat | first1 = T. | last2 = Orglmeister | first2 = E. | last3 = Baiker | first3 = A. | journal = Chemical Reviews | volume = 107 | issue = 11 | pages = 4863–90 | pmid = 17927256}}
- ^ 13.0 13.1 {{cite journal|last1=Adams|first1=Roger|last2=Voorhees|first2=V.|title=Apparatus for catalytic reduction|journal=Organic Syntheses|date=1928|volume=8|page=10|doi=10.15227/orgsyn.008.0010}}
- ^ {{cite journal | doi = 10.1016/0009-2509(82)80171-1 | title = Mechanically agitated gas–liquid reactors | year = 1982 | last1 = Joshi | first1 = J.B. | last2 = Pandit | first2 = A.B. | last3 = Sharma | first3 = M.M. | journal = Chemical Engineering Science | volume = 37 | issue = 6 | pages = 813}}




