索磷布韦
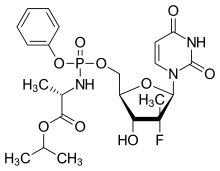
外观
 | |
| 临床资料 | |
|---|---|
| 商品名 | Sovaldi, others[1] |
| 其他名称 | PSI-7977; GS-7977 |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a614014 |
| 核准状况 |
|
| 怀孕分级 | |
| 给药途径 | By mouth[3] |
| 药物类别 | HCV polymerase inhibitor |
| ATC码 | |
| 法律规范状态 | |
| 法律规范 |
|
| 药物动力学数据 | |
| 生物利用度 | 92% |
| 血浆蛋白结合率 | 61–65% |
| 药物代谢 | Quickly activated to triphosphate (CatA/CES1, HIST1, phosphorylation) |
| 生物半衰期 | 0.4 hrs (sofosbuvir) 27 hrs (inactive metabolite GS-331007) |
| 排泄途径 | 80% urine, 14% feces (mostly as GS-331007) |
| 识别信息 | |
| |
| CAS号 | 1190307-88-0 |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.224.393 |
| 化学信息 | |
| 化学式 | C22H29FN3O9P |
| 摩尔质量 | 529.46 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
索磷布韦(英语:Sofosbuvir,又称索非布韦),常用商品名索华迪(英语:Sovaldi)是一种治疗丙型肝炎的药物[7],口服,通常结合利巴韦林、司美匹韦、雷迪帕韦等药物共同使用。索非布韦于2007年由美国化学家、Pharmasset科学家迈克尔·J·索菲亚发现,2013年在美国获批使用,该药列于《世界卫生组织基本药物标准清单》。迈克尔·J·索菲亚因此获得2016年拉斯克临床医学研究奖。2011年吉利德科学以110亿美元收购Pharmasset。
参考文献
[编辑]- ^ 引用错误:没有为名为
EcTimes2015的参考文献提供内容 - ^ Sofosbuvir (Sovaldi) Use During Pregnancy. Drugs.com. 16 December 2019 [5 February 2020]. (原始内容存档于2020-02-05).
- ^ 引用错误:没有为名为
AHFS2016的参考文献提供内容 - ^ 引用错误:没有为名为
UKlabel的参考文献提供内容 - ^ 引用错误:没有为名为
Sovaldi FDA label的参考文献提供内容 - ^ Sovaldi Access- sofosbuvir tablet, film coated. DailyMed. [26 January 2022]. (原始内容存档于2022-01-27).
- ^ Sofosbuvir Monograph for Professionals. Drugs.com. [2022-05-30]. (原始内容存档于2016-12-01) (英语).
