碳化鉭
| 碳化鉭 | |
|---|---|
| |

| |
| IUPAC名 Tantalum carbide | |
| 別名 | 碳化鉭(IV) |
| 識別 | |
| CAS號 | 12070-06-3 12070-07-4((TaC0.5)) |
| SMILES |
|
| InChI |
|
| InChIKey | DUMHRFXBHXIRTD-UHFFFAOYSA-N |
| 性質 | |
| 化學式 | TaC |
| 莫耳質量 | 192.96 g/mol g·mol⁻¹ |
| 外觀 | 棕灰色粉末 |
| 氣味 | 無臭 |
| 密度 | 14.3–14.65 g/cm3 (TaC) 15.1 g/cm3 (TaC0.5)[1] |
| 熔點 | 3,850—3,880 °C(4,120—4,150 K)(TaC)[2] 3,327 °C(6,021 °F;3,600 K) (TaC0.5)[1] |
| 沸點 | 4,780—5,470 °C(5,050—5,740 K)(TaC)[1][2] |
| 溶解性(水) | 不溶 |
| 溶解性 | 可溶於HF-HNO3的混合物[1] |
| 熱導率 | 21 W/m·K |
| 熱力學 | |
| ΔfHm⦵298K | −144.1 kJ/mol |
| S⦵298K | 42.29 J/mol·K |
| 熱容 | 36.71 J/mol·K[3] |
| 相關物質 | |
| 相關化學品 | 一氮化鋯 碳化鈮 碳化鋯 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
碳化鉭是一類二元化合物,由鉭和碳組成,實驗式TaCx,x 一般在 0.4 到1 之間。它們的硬度極大,脆,是耐火材料,具有金屬的電導率。它是一種棕灰色粉末,通常通過燒結處理。
作為重要的金屬陶瓷材料,碳化鉭在商業車刀中用於切削應用,有時會添加到碳化鎢合金中。[4]
取決於純度和測量條件,碳化鉭的熔點在約3880℃達到峰值。這個值是二元化合物里最高的。[5][6]只有碳化鉭鉿的熔點可能略高,大約為3942°C,[7]而碳化鉿的熔點與TaC相當。
製備
[編輯]TaCx粉末是由鉭和石墨的粉末在真空或惰性氣體(氬)里使用爐子或電弧熔化裝置在約2000℃的溫度下進行加熱。[8][9]鉭和石墨的量決定了x的值。另一種技術是在真空或氫氣氣氛中,在1500–1700℃的溫度下通過碳進行五氧化二鉭的還原。該方法於1876年用於獲得碳化鉭,[10]但它無法控制產物的化學計量。[6]自蔓延高溫合成法也是已報道的直接從單質製備TaC的方法之一。[11]
晶體結構
[編輯]
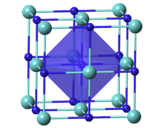
當 x = 0.7–1.0 時,TaCx有著立方結構 (岩鹽的結構) 。[12]碳化鉭的晶格常數會隨著x增長而增長。[13] TaC0.5有兩種結構。較穩定的具有反碘化鎘型三角結構,該結構在加熱至約2000℃時轉變為六方晶格,對碳原子來說已經沒有規律了。[8]
| 實驗式 | 對稱性 | 種類 | 皮爾遜符號 | 空間群 | No | Z | ρ (g/cm3) | a (nm) | c (nm) |
|---|---|---|---|---|---|---|---|---|---|
| TaC | 立方 | NaCl[13] | cF8 | Fm3m | 225 | 4 | 14.6 | 0.4427 | |
| TaC0.75 | 三方[14] | hR24 | R3m | 166 | 12 | 15.01 | 0.3116 | 3 | |
| TaC0.5 | 三方[15] | 反-CdI2 | hP3 | P3m1 | 164 | 1 | 15.08 | 0.3103 | 0.4938 |
| TaC0.5 | 六方[9] | hP4 | P63/mmc | 194 | 2 | 15.03 | 0.3105 | 0.4935 |
在這個表中,Z是每單位的配位數,ρ是由晶格常數計算而來的密度。
性質
[編輯]碳化鉭中鉭和碳原子之間的鍵是離子鍵,金屬鍵和共價鍵混合,是很複雜的鍵,並且由於強共價成分,這些碳化物是非常堅硬且易碎的材料。舉個例子,TaC的顯微硬度為1600-2000 kg/mm2 [16](〜9 Mohs)和285 GPa的彈性模量,而鉭的相應值為110 kg/mm2和186 GPa。碳化鉭的硬度,屈服和剪切應力隨TaCx中碳含量的增加而增加。[17]
碳化鉭無論是什麼大小和溫度都具有金屬導電性。TaC 可以在10.35 K以下轉變為超導體。[13]
TaCx的磁性能從x≤0.9的反磁性變為「 x」≥0.9的順磁性。儘管HfCx具有與TaCx相同的晶體結構,但仍觀察到了相反的行為(磁性隨x的增加而減少)。[18]
應用
[編輯]碳化鉭因其在熔點、硬度、彈性模量、導熱性、熱衝擊方面的優異物理性能而被廣泛用作超高溫陶瓷(UHTC)的燒結添加劑或高熵合金(HEA)的陶瓷增強材料抵抗力和化學穩定性,這使其成為航空航天工業中飛機和火箭的理想材料。
天然存在
[編輯]鉭碳礦是碳化鉭的天然存在形式。它屬立方晶系,並且非常稀有。[19]
參見
[編輯]參考資料
[編輯]- ^ 1.0 1.1 1.2 1.3 Lide, David R. (編). CRC Handbook of Chemistry and Physics 90th. Boca Raton, Florida: CRC Press. 2009. ISBN 978-1-4200-9084-0 (英語).
- ^ 2.0 2.1 5196273[失效連結]
- ^ Tantalum carbide in Linstrom, Peter J.; Mallard, William G. (eds.); NIST Chemistry WebBook, NIST Standard Reference Database Number 69, National Institute of Standards and Technology, Gaithersburg (MD), http://webbook.nist.gov (retrieved 2014-07-02)
- ^ Emsley, John. Nature's building blocks: an A-Z guide to the elements. Oxford University Press. 11 August 2003: 421– [2 May 2011]. ISBN 978-0-19-850340-8.
- ^ TaC0.89中4000°C的熔點聲稱不是基於實際測量,而是基於相圖的推斷,使用與NbC的類比,請參見Emeléus
- ^ 6.0 6.1 Emeléus, Harry. Advances in Inorganic Chemistry and Radiochemistry. Academic Press. 1968: 174–176 [3 May 2011]. ISBN 978-0-12-023611-4. (原始內容存檔於2017-03-24).
- ^ Agte, C.; Alterthum, H. Researches on Systems with Carbides at High Melting Point and Contributions to the Problem of Carbon Fusion. Zeitschrift für technische Physik. 1930, 11: 182–191. ISSN 0373-0093.
- ^ 8.0 8.1 Lonnberg, B; Lundstrom, T; Tellgren, R. A neutron powder diffraction study of Ta2C and W2C. Journal of the Less Common Metals. 1986, 120 (2): 239–245. doi:10.1016/0022-5088(86)90648-X.
- ^ 9.0 9.1 Rudy, Erwin; Brukl, C. E.; Windisch, Stephan. Constitution of Ternary Ta-Mo-C Alloys. Journal of the American Ceramic Society. 1968, 51 (5): 239–250. doi:10.1111/j.1151-2916.1968.tb13850.x.
- ^ Joly, A. Sur les azotures et carbures de niobium et de tantale. Compt. Rend. 1876, 82: 1195 [2020-07-14]. (原始內容存檔於2020-07-16) (法語).
- ^ Shuck, Christopher E.; Manukyan, Khachatur V.; Rouvimov, Sergei; Rogachev, Alexander S.; Mukasyan, Alexander S. Solid-flame: Experimental validation. Combustion and Flame. January 2016, 163: 487–493. doi:10.1016/j.combustflame.2015.10.025.
- ^ Lavrentyev, A; Gabrelian, B; Vorzhev, V; Nikiforov, I; Khyzhun, O; Rehr, J. Electronic structure of cubic HfxTa1–xCy carbides from X-ray spectroscopy studies and cluster self-consistent calculations. Journal of Alloys and Compounds. 2008, 462 (1–2): 4–10. doi:10.1016/j.jallcom.2007.08.018.
- ^ 13.0 13.1 13.2 Valvoda, V. X-ray diffraction study of Debye temperature and charge distribution in tantalum monocarbide. Physica Status Solidi A. 1981, 64: 133–142. doi:10.1002/pssa.2210640114.
- ^ Yvon, K.; Parthé, E. On the crystal chemistry of the close-packed transition-metal carbides. I. The crystal structure of the [zeta]-V, Nb and Ta carbides. Acta Crystallographica Section B. 1970, 26 (2): 149–153. doi:10.1107/S0567740870002091.
- ^ Bowman, A. L.; Wallace, T. C.; Yarnell, J. L.; Wenzel, R. G.; Storms, E. K. The crystal structures of V2C and Ta2C. Acta Crystallographica. 1965, 19: 6–9. doi:10.1107/S0365110X65002670.
- ^ Kurt H. Stern (1996). Metallurgical and Ceramic Protective Coatings. Chapman & Hall.
- ^ Oyama, S. Ted. The chemistry of transition metal carbides and nitrides. Springer. 1996: 29–30 [3 May 2011]. ISBN 978-0-7514-0365-7. (原始內容存檔於2020-07-14).
- ^ Gusev, Aleksandr; Rempel, Andrey; Magerl, Andreas. Disorder and order in strongly nonstoichiometric compounds: transition metal carbides, nitrides, and oxides. Springer. 2001: 513–516 [3 May 2011]. ISBN 978-3-540-41817-7. (原始內容存檔於2020-08-11).
- ^ Mindat, Tantalcarbide (頁面存檔備份,存於網際網路檔案館). [2020-07-27]
