氯甲酸苄酯
外觀
| 氯甲酸苄酯 | |
|---|---|

| |
| |
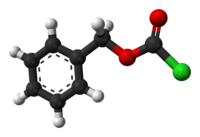
| IUPAC名 氯甲酸苄酯 | |
| 別名 | 甲酸氯苄酯 苄基碳酰氯 苯甲氧基甲酰氯 Cbz-Cl |
| 識別 | |
| CAS號 | 501-53-1 |
| PubChem | 10387 |
| ChemSpider | 9958 |
| SMILES |
|
| InChI |
|
| InChIKey | HSDAJNMJOMSNEV-UHFFFAOYAW |
| UN編號 | 1739 |
| RTECS | LQ5860000 |
| 性質 | |
| 化學式 | C8H7ClO2 |
| 摩爾質量 | 170.59 g·mol−1 |
| 外觀 | 透明液體 |
| 氣味 | 刺鼻 |
| 密度 | 1.195 g/cm3 |
| 沸點 | 103 °C(376 K)((20 Torr)) |
| 溶解性(水) | 分解 |
| 折光度n D |
1.519 (589 nm) |
| 危險性 | |
GHS危險性符號 
| |
| GHS提示詞 | Danger |
| H-術語 | H314, H400, H410 |
| P-術語 | P260, P264, P273, P280, P301+330+331, P303+361+353, P304+340, P305+351+338, P310, P321, P363, P391, P405, P501 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氯甲酸苄酯,化學式,是一種有機化合物。它是一種氯甲酸酯。氯甲酸苄酯是透明油狀液體,有刺激性氣味,而且遇水分解,遇熱分解成光氣等有毒氣體[1]。在有機合成上,它被用於引入苄氧羰基(Cbz),即是一種保護胺基的保護基。[2]同時,它可用作有機合成中間體。[1]
製備
[編輯]氯甲酸苄酯可以由苄醇與光氣反應而成。[3][2]反應式如下:
- PhCH2OH + COCl2 → PhCH2OC(O)Cl + HCl
反應需要用到過量的光氣來盡量減少生成碳酸酯(PhCH2O)2C=O。[3]
保護基
[編輯]在有機合成中,氯甲酸苄酯常被用於引入苄氧羰基。苄氧羰基是一個胺基的保護基,簡稱Cbz或Z。於1930年代初,化學家Leonidas Zervas製備了氯甲酸苄酯,並用它來引入苄氧羰基保護基。反應式如下:
後來他與另一科學家Max Bergmann以此作基礎,開發了一種新的方法來合成肽。[4][5]在1950年代之前,這是多肽合成最常用的步驟。[4]
除了多肽合成,氯甲酸苄酯亦常用於保護一般的胺基,使氮的鹼性與親核性減弱。
上保護基
[編輯]以下是常用的方法:
- 胺與氯甲酸苄酯、N,N-二異丙基乙基胺、乙腈和三氟甲磺酸鈧作用。[7]
脫保護基
[編輯]以下是常用的方法:
受保護的胺經過以上方法處理,首先生成氨基甲酸,再經過脫羧,生成原來的胺。
參考資料
[編輯]- ^ 1.0 1.1 氯甲酸苄酯. ChemicalBook. [2022-08-17]. (原始內容存檔於2022-08-17).
- ^ 2.0 2.1 氯甲酸苄酯. 化工百科. [2022-08-17].
- ^ 3.0 3.1 Hough, L.; Priddle, J. E. Carbonate derivatives of methyl α-D-mannopyranoside and of D-mannose. J. Chem. Soc. 1961, 1961: 3178–3181. doi:10.1039/JR9610003178.
- ^ 4.0 4.1 4.2 Katsoyannis, P. G. (編). The Chemistry of Polypeptides. New York: Plenum Press. 1973 [2022-08-17]. ISBN 978-1-4613-4571-8. S2CID 35144893. doi:10.1007/978-1-4613-4571-8. (原始內容存檔於2022-10-13).
- ^ 5.0 5.1 Bergmann, Max; Zervas, Leonidas. Über ein allgemeines Verfahren der Peptid-Synthese [On a general method of peptide synthesis]. Berichte der deutschen chemischen Gesellschaft. 1932, 65 (7): 1192–1201. doi:10.1002/cber.19320650722.
- ^ Dymicky, M. Preparation of Carbobenzoxy-L-Tyrosine Methyl and Ethyl Esters and of the Corresponding Carbobenzoxy Hydrazides. Organic Preparations and Procedures International. 1989-02-01, 21 (1): 83–90. ISSN 0030-4948. doi:10.1080/00304948909356350.
- ^ Aggarwal, Varinder K.; Humphries, Paul S.; Fenwick, Ashley. A Formal Asymmetric Synthesis of Anatoxin-a Using an Enantioselective Deprotonation Strategy on an Eight-Membered Ring. Angewandte Chemie International Edition. 1999, 38 (13–14): 1985–1986. doi:10.1002/(SICI)1521-3773(19990712)38:13/14<1985::AID-ANIE1985>3.0.CO;2-7.
- ^ Jakubke, Hans-Dieter; Sewald, Norbert. Peptides from A to Z: A Concise Encyclopedia. John Wiley & Sons. 2008. ISBN 978-3-527-62117-0.
- ^ Felpin, François-Xavier; Fouquet, Eric. A Useful, Reliable and Safer Protocol for Hydrogenation and the Hydrogenolysis of O-Benzyl Groups: The In Situ Preparation of an Active Pd0/C Catalyst with Well-Defined Properties. Chemistry – A European Journal. 2010-11-02, 16 (41): 12440–12445. ISSN 1521-3765. PMID 20845414. doi:10.1002/chem.201001377 (英語).
- ^ 邢, 其毅; 裴, 偉偉; 徐, 瑞秋; 裴, 堅. 第21章 氨基酸、多肽、蛋白質以及核酸. 基礎有機化學. 北京. 2017: 997. ISBN 9787301279434.




