原子序數
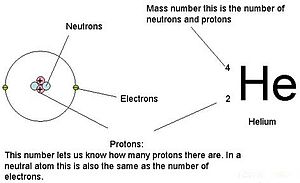
原子序數(atomic number)又稱原子序[1]、核電荷數[2](nuclear charge number),常以符號 Z 表示[3],是元素在週期表中排位的序號[4];擁有同一原子序數的原子屬於同一化學元素。原子序等於質子數(proton number,np),即一個原子核內質子的數目或核電荷數;原子序又等於原子電中性時的核外電子數目[5]。
由於每種元素的原子序數均固定,一般而言不需要特別為原子標示其原子序數。如果想明示原子的原子序數,可將其標示在元素符號的左下方,如:氫記作1H,碳記作6C。
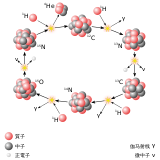
德米特里·門捷列夫在制定其元素週期表時發現,假如將元素按其原子核質量來排列會出現一些不規則的情況。比如碲的原子核比碘重,但從化學性質上來說,碲明顯是與氧、硫、硒一族的,而碘與氟、氯、溴是一族的,也就是說,碘要排在碲之後。1913年亨利·莫塞萊發現這個異常的解決方法不是按原子質量,而是按原子核的電荷數,即原子序來排列。
原子序數的符號
[編輯]原子序數一般會用 Z 表示,可能是來自原子序的德文 Atomzahl [6]。不過在1915年之前,德文 Zahl(數字)用來表示元素在週期表中的編號。
化學性質
[編輯]每個化學元素依其元素電中性時電子的個數(也就是原子序數)不同,會有獨特的化學性質。電子的電子排佈依照量子力學的原理,不同電子層的電子個數,特別是價電子的個數,是決定化學鍵特性的主要因素。因此元素可以定義為由許多有特定原子序數的任意原子混合而成的物質。
新的元素
[編輯]新發現的元素一般會用其原子序來表示,到2010年為止,已經發現原子序1至118的元素,第118號的元素是鿫。新元素的合成是用離子撞擊有高原子序的靶原子,而離子和靶原子的原子序和等於要發現元素的原子序。一般而言,當原子序越大,其半衰期越短,而原子序是偶數的半衰期會比原子序是奇數的長,不過可能針對特定質子數及中子數的同位素,會存在穩定島,其半衰期會較相同原子序的元素要長一些。
參見
[編輯]參考資料
[編輯]- ^ 存档副本. [2020-08-03]. (原始內容存檔於2020-12-19).
- ^ 存档副本. [2023-08-31]. (原始內容存檔於2023-08-31).
- ^ 存档副本. [2023-08-31]. (原始內容存檔於2023-08-31).
- ^ 术语在线—权威的术语知识服务平台. termonline.cn. [7 September 2023]. (原始內容存檔於2023-08-31).
元素在週期表中排列的序號。等於原子的核電荷數,即核內質子數。符號為Z。
- ^ 王昆林. 材料工程基础. 清華大學出版社有限公司. 2003: 24– [2014-03-30]. ISBN 978-7-302-07064-1. (原始內容存檔於2014-07-03).
- ^ Origin of symbol Z. [2014-03-29]. (原始內容存檔於2000-01-16).