多伦试剂
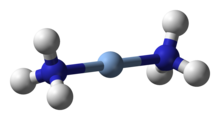
([Ag(NH3)2]+)的球棍模型。

银氨溶液,又称氢氧化二氨合银,俗称苛性银,是含有二氨合银(I)配离子([Ag(NH3)2]+)的水溶液,一般由硝酸银或其他银化合物与氨水反应制取,溶于水中能够完全离解出氢氧根离子,故属于强碱,具腐蚀性。
19世纪德国化学家伯恩哈德·多伦发现银氨溶液遇醛反应一段时间后,会形成“漂亮且闪亮的银镜”(ein sehr schön glänzender Silberspiegel),也就是金属银,可作为检验醛的试剂[1],因此银氨溶液也常被称为多伦试剂(英语:Tollens' reagent,又译多仑试剂、吐伦试剂或土伦试剂),而其和醛反应而析出银的过程后来则被称为银镜反应。
制备[编辑]
银氨溶液不可能在市面上买到,因为它的保质期太短了,只能在实验室现用现配。
- 向大概0.1mol的硝酸银溶液中加入几滴氢氧化钠稀溶液,此时氢氧化钠中的氢氧根离子会把银水配合物变成棕色的氧化银沉淀。
- 向溶液中滴加饱和的氨水,直至棕色沉淀刚好溶解。此时产生了银氨络合物,所得的溶液即为银氨溶液,含[Ag(NH3)2]NO3(aq)。而氢氧化钠就被恢复回来了。
反应方程式为:
- 2 AgNO3 + 2 NaOH → Ag2O (s) + 2 NaNO3 + H2O
- Ag2O (s) + 4 NH3 + 2 NaNO3 + H2O → 2 [Ag(NH3)2]NO3 + 2 NaOH
也可以直接向硝酸银溶液中滴加氨水,至沉淀恰好完全溶解。[2]
滴加氢氧化钠时首先产生白色的氢氧化银沉淀,非常不稳定,立即分解为棕色的氧化银和水。硝酸银也可由一些不溶的银盐代替,但制备时不需加入氢氧化钠,直接加入氨水将不溶物溶解即可。
用途[编辑]
银氨溶液与斐林试剂类似,具有微弱的氧化性,在自身被还原后,会在容器内壁附着上一层光亮的银层,即是所谓的银镜反应。一般用银镜反应来鉴定醛的存在,相应的氧化产物是羧酸根离子,酸化得到羧酸。甲醛或甲酸可被彻底氧化为二氧化碳。

银氨溶液与2,4-二硝基苯肼(Brady试剂)连用可以检出样品中醛基官能团的存在。若样品与2,4-二硝基苯肼作用呈阳性,产生黄色或红色的二硝基苯腙沉淀,则可证明样品为羰基化合物,可能是醛或酮。由于醛具还原性,而酮不具有还原性,此时再用银氨溶液测试,便可区分这二者官能团,醛将银氨溶液还原而产生银镜。此方法对醛糖和酮糖也基本有效。
银氨溶液也可用于鉴定末端炔烃,现象是产生了白色的炔化银(乙炔银、碳化银)沉淀。
生物学银染色[编辑]
银氨溶液在组织病理解剖的丰塔纳-马森法(英语:Fontana-Masson Stain)中被用来检测组织切片里的脂褐素、黑色素和嗜银细胞。黑色素和嗜铬细胞会把硝酸银还原成金属银。[2]
镀银[编辑]
银氨溶液也被用作在玻璃器具上镀银,如在真空保温瓶的内胆上涂银层。所用还原剂是带醛基的葡萄糖,要想镀银效果良好,需先清洁玻璃器具。为加快金属银的沉淀速度,沉淀对象玻璃需要先在稳定的氯化亚锡的盐酸溶液中预处理。[3]
在要尽可能高质量的镜面上——如望远镜的主镜,用氯化亚锡镀银就会产生纳米级的凹凸,并降低镜面的反射效果。[4][5]给主镜镀银需要加添加剂,如使用马丁法(英语:Martin's Method),添加含酒石酸和酒精的添加剂。[5]
安全[编辑]
银氨溶液应现配现用,并且使用后立即加盐酸销毁,还可利用银离子的氧化性与一些强还原剂如羟胺等反应以回收银单质(这也是分析化学中盐酸羟胺的应用范围)。它在储存时会转化为强爆炸性的黑色含银不溶物(成分是氮化银 Ag3N[6][7]),通常时间为一至三天,但天气炎热时数小时便会生成[8]
参考来源[编辑]
- ^ (德文)Tollens, B. Ueber ammon-alkalische Silberlösung als Reagens auf Aldehyd [记一种可作为醛之试剂的碱性氨银溶液]. Berichte der Deutschen Chemischen Gesellschaft. 1882, 15 (2): 1635–1639 [2020-05-14]. doi:10.1002/cber.18820150243. (原始内容存档于2022-06-13).
- ^ 2.0 2.1 Webpath website http://library.med.utah.edu/WebPath/HISTHTML/MANUALS/FONTANA.PDF (页面存档备份,存于互联网档案馆) Accessed 4 February 2009
- ^ Hart, M. Manual of scientific glassblowing. St. Helens, Merseyside [England]: British Society of Scientific Glassblowers. 1992. ISBN 0-9518216-0-1.
- ^ Chitvoranund, Natechanok; Jiemsirilers, Sirithan; Kashima, Dujreutai Pongkao. Effects of Surface Treatment on Adhesion of Silver Film on Glass Substrate Fabricated by Electroless Plating. Advanced Materials Research. 2013-02, 664: 566–573 [2021-01-07]. ISSN 1662-8985. doi:10.4028/www.scientific.net/AMR.664.566. (原始内容存档于2021-01-09).
- ^ 5.0 5.1 Curtis, Heber D. Methods of Silvering Mirrors. Publications of the Astronomical Society of the Pacific. 1911-02, 23: 13 [2021-01-07]. ISSN 0004-6280. doi:10.1086/122040. (原始内容存档于2021-03-05) (英语).
- ^ Shanley, Edward S.; Ennis, John L. The chemistry and free energy of formation of silver nitride. Industrial & Engineering Chemistry Research. 1991-11, 30 (11): 2503–2506 [2021-01-07]. ISSN 0888-5885. doi:10.1021/ie00059a023. (原始内容存档于2021-01-09) (英语).
- ^ Svehla, G.; Vogel, Arthur Anton. Vogel's qualitative inorganic analysis. New York: Longman. 1996. ISBN 0-582-21866-7.
- ^ 北京师范大学无机化学教研室等编. 无机化学 第四版 下册. 北京:高等教育出版社,2003
外部链接[编辑]
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
