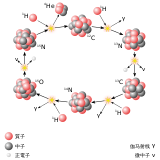
核素
核素(英语:nuclide)又称核种,是具有特定质子数(原子序数)、中子数、核能态,且其平均寿命长得足以能被观测的一类原子[1][2],分为稳定核素和放射性核素两类。英语 nuclide 与汉语译名虽侧重于原子核,但其最早定义即为以原子核组成为特征的原子种类[3][4]。译名“核种”是指原子的种类[5],译名“核素”是相对于元素,其概念晚于元素,因此元素的范围就扩大成了一些核电荷相等核素的杂化物[6]。
凡原子核构造不同的原子,例如质子数或中子数不同,皆视为不同的核素,例如氕、氘、碳-12、碳-14、铀-235、铀-238等皆为不同的核素。而有些原子的原子核虽然构造相同,但只要其所处的能态不同(基态或半衰期超过10−9秒的亚稳态),亦视为不同核素,例如锝-99和锝-99m[7]。
名称由来
[编辑]核素一词在英文中被叫做“nuclide”,这一单词来源于拉丁语 nucleus(核)和古希腊语 εἶδος [8][9](可见形态),是由这两个词复合而成的。
1947年美国科学家杜鲁门·保罗·寇曼提出“核素”一词,寇曼将它定义为:“具有给定质子数Z和中子数N的一类原子核所组成的元素”[10][11]。目前许多国家仍然在采用这一定义,但当涉及到活度的定义时,这种定义就显得不够完善了。
表示方法
[编辑]核素的名称通常以其所属元素加上其质量数来表示,例如氦-3、氦-4、碳-12、碳-14、铀-235、铀-238等[12]。当使用化学符号表示核素时,通常使用的形式,其中E为该核素所属元素的化学符号(氘和氚这二种核素有自己的符号:D和T);Z为该核素的质子数(即原子序数);A为该核素的质量数(即核子数,质子数和中子数之和);N为该核素的中子数(一般情况下不标出),例如3
2He
、4
2He
、12
6C
、14
6C
、235
92U
、238
92U
。由于从核素的所属元素便可推知其质子数,因此以符号表示核素时通常只会注明其上标的质量数,而省略下标的质子数,如3
He
、4
He
、12
C
、14
C
、235
U
、238
U
。若在核素符号的质量数后加上字母m,则表示其为核同质异能素,其原子核处于较高能级的亚稳态,但半衰期比一般的激发态原子核要长(通常达到100~1000倍的时间),例如99m
Tc
(锝-99m)、242m
Am
(镅-242m)等。当一基态核素的原子存在多个不同能级的核同质异能素时,则使用m1、m2、m3等,按照其激发能量从低到高进行标记,如177m2
Hf
(铪-177m2)等。
与同位素概念的区别
[编辑]核素的定义主要聚焦在原子核的层面,不仅考虑原子核内中子数与质子数的差异,同时也考虑了影响核性质的另一主要因素,即核能态的不同,对原子核的性质描述更深入,涉及核力、核结构及原子核的大小、自旋、宇称、电四极矩等。而同位素的概念则更加强调原子化学性质的异同,将质子数相同的原子归类为同一种元素的同位素。中子数对原子的核性质有很大的影响,但对大多数原子的化学性质之影响可忽略不计。尽管对于较轻的元素,其核内中子数与质子数之比在同位素之间变化较大,对其化学性质的影响通常也十分微小。
核素一词可用于称呼任何原子核构造或所处能态不同的原子种类,如质子数或中子数不同的原子,皆视为不同的核素。而同位素一词最初主要用于称呼质子数相同而中子数不同的原子,称其为同一种元素的不同同位素。然而,由于同位素一词在学界中使用历史较为悠久,比核素一词更广为人知,如今在核技术和核医学等许多领域中仍常用“同位素”指代任何具有特定质子数及中子数的原子种类,尽管在概念及语意上使用“核素”更为合适。
种类
[编辑]尽管核素和同位素这两个术语在一般语境中经常相互替代使用,但狭义上同位素专指质子数相同而中子数不同的核素。下表列出了其他描述核子数或核能态间具有特性关系的核素术语:
| 术语 | 特性关系 | 示例 | 备注 |
|---|---|---|---|
| 同位素 | 质子数(原子序数)相同的核素(Z1 = Z2) | 12 6C 、13 6C 、14 6C |
互为同位素的核素由于原子序相同,故属于同一种元素 |
| 同中子素 | 中子数相同的核素(N1 = N2) | 13 6C 、14 7N 、15 8O |
|
| 同量异位素 | 质量数相同的核素(Z1 + N1 = Z2 + N2) | 17 7N 、17 8O 、17 9F |
放射性核素及其发生β衰变后的子核素互为同量异位素 |
| 同差素 | 中子数与质子数之差相同的核素(N1 − Z1 = N2 − Z2) | 13 6C 、15 7N 、17 8O |
放射性核素及其发生α衰变后的子核素互为同差素[13] |
| 镜像核 | 中子数与质子数彼此互换的一对核素 (Z1 = N2 且 Z2 = N1) |
3 1H 、3 2He |
镜像核彼此互为同量异位素 |
| 核同质异能素 | 质子数和中子数皆相同,但核能态不同的核素 | 99 43Tc 、99m 43Tc |
m意为亚稳态(metastable),指寿命较长的激发态(半衰期>10−9秒) |
核同质异能素是指质子数及中子数相同,但原子核处于不同能级的核素。通常处于激发态的原子核会在无法直接测量的极短时间(约10−12秒)内发生γ衰变,转变成能级较低的原子核。不过有些激发态原子核的半衰期比常见的激发态原子核的半衰期要长(>10−9秒),因此被称作处于亚稳态,这种处于亚稳态的高能级原子核在核物理学上被视为和基态原子核不同的核素,称为核同质异能素,例如亚稳态的99m
43Tc
是基态的99
43Tc
的核同质异能素。由于核同质异能素的核子组成和基态核素完全相同,因此在定义上它们被算作同一种同位素,不过由于核能态的差异,他们仍被视为不同的核素。目前已知寿命最长的亚稳态核同质异能素是180m
73Ta
,其半衰期超过1000兆年,是原始核素之一,并且从未被观察到其衰变成基态。相比之下,其基态核素180
73Ta
的半衰期仅约8小时。
核稳定性
[编辑]原子核中不同数目的质子和中子的组合会影响其稳定性,因此每种核素的核稳定性各不相同。
目前已知的大多数核素原子核皆不稳定,具有放射性,会自发性地放出电离辐射并衰变成其他核素,称为放射性核素,例如3
1H
、14
6C
、40
19K
、60
27Co
、131
53I
、137
55Cs
和235
92U
等。每种放射性核素的核稳定性各不相同,因此发生衰变的半衰期也有长有短,原子核越不稳定的核素半衰期越短,放射性越强。目前已发现的放射性核素超过3000种[14],其中大部分不存在于自然界,只能借由人工合成的方式生成,称为人造放射性核素。至于天然存在的放射性核素则包括半衰期极长的原始放射性核素、原始放射性核素衰变生成的次生天然放射性核素以及宇宙射线作用产生的宇生放射性核素等。
原子核稳定、不会发生放射性衰变的核素则称为稳定核素,共有251种,皆自然存在于地球上,分别属于原子序1号(氢)至82号(铅)的化学元素(锝和钷除外)。稳定核素由于不会衰变成其他核素,自恒星核合成过程诞生后能以稳定的量恒久存在,因此构成了现今自然界中绝大多数的物质,大多数元素在地球和太阳系中同位素的丰度比例往往也是稳定同位素占绝大部分或全部。不过自然界中有三种元素(碲、铟和铼)虽然有着稳定同位素,但其丰度最高的同位素却是寿命极长的放射性同位素。
理论计算显示,许多表面上为“稳定”的核素在能量上容易受到一些已知衰变形式的影响,例如α衰变或双β衰变(不考虑尚未证实的质子衰变,因为这将使所有核素皆属不稳定),然而目前尚未观察到任何它们发生衰变的现象,因此这些核素被认为是“观测上稳定”的核素。这些核素的预测半衰期往往远超宇宙的估计年龄。此外,理论上所有比93
41Nb
重(含)的核素都有可能自发裂变,然而目前观测到会进行此衰变的最轻核素为232
90Th
。
影响核稳定性的因素
[编辑]核子数的比例
[编辑]
黑色 – 稳定核素
其他颜色 – 放射性核素,各颜色表示该核素的主要衰变形式
图中的对角线表示质子数与中子数相同(中子-质子比为1)的核素。由此图可归纳出:质子数超过20的稳定核素所含的中子数皆大于质子数,且核子数越多,中子-质子比越大。
原子核中的核子通过残留强力结合在一起(只有一个核子的氕 1
1H
除外)。由于质子带正电,故彼此相互排斥。而中子是电中性的,它能以两种方式稳定原子核:中子的存在能将核中的质子稍微间隔开,减少了质子间的静电斥力,且中子会对周遭核子施加吸引的核力。因此,两个以上的质子需要伴随一至多个中子才能结合成原子核。随着质子数量的增加,确保原子核稳定所需的中子-质子比(N/Z)也随之增大(见图)。例如3
2He
的中子-质子比为1/2,而高原子序的238
92U
之中子-质子比则超过3/2。许多较轻的元素具有中子-质子比为1(即Z = N)的稳定同位素,其中40
20Ca
是已知中子-质子比为1的稳定核素中质量最重的。所有比40
20Ca
重的稳定核素所含的中子数皆大于质子数(即中子-质子比>1),参看配图。
核子数的奇偶性
[编辑]| A | 偶数 | 奇数 | 总计 | ||
|---|---|---|---|---|---|
| Z与N | 偶偶核素 | 奇奇核素 | 偶奇核素 | 奇偶核素 | |
| 稳定核素 | 145 | 5 | 53 | 48 | 251 |
| 150 | 101 | ||||
| 长寿放射性核素 | 22 | 4 | 4 | 5 | 35 |
| 26 | 9 | ||||
| 原始核素 | 167 | 9 | 57 | 53 | 286 |
| 176 | 110 | ||||
中子-质子比并不是影响核稳定性的唯一因素。原子核的稳定性还会受到质子数(Z)、中子数(N)及质量数(A)是偶数还是奇数所影响。原子核中的质子或中子互相成对能相互抵消角动量,是形成稳定核的条件之一。Z、N或A为奇数往往会降低核结合能,从而使奇数核通常不太稳定。故大多数稳定核素皆为Z与N都是偶数(故A也是偶数)的偶偶核。也有部分稳定核素属于A为奇数的奇偶核(Z为奇数,N为偶数)或偶奇核(Z为偶数,N为奇数)。至于奇奇核(Z和N都是奇数)绝大多数都不稳定,属于奇奇核的稳定核素非常稀少[7]。
幻数原子核
[编辑]质子数或中子数为幻数的原子核会显现出较高的稳定性。目前已经确认的幻数皆为偶数,包括2、8、20、28、50、82和126这七个数目,而氦、氧、钙、镍、锡、铅等六个元素的质子数分别与2到82的幻数相对应,这些元素都具有多个稳定同位素,其中锡的稳定同位素多达10种,居所有元素之冠。至于质子数为126的元素Ubh目前尚未发现,预计其处于放射性超重元素稳定岛的中央。当原子核之质子数和中子数皆为幻数时,该情况称为“双幻数”,许多具有双幻数的核素都显得异常稳定,例如4
2He
、16
8O
、40
20Ca
和208
82Pb
都是密闭核排布的稳定核素,48
20Ca
则是寿命极长的原始放射性核素[7][15]。
存在及来源
[编辑]地球上大约有339种自然存在的核素[16],分属于94种化学元素(1号的氢至94号的钚),其中有251种为稳定核素,其余则是不稳定的放射性核素。
在这339种天然核素中,有286种是自太阳系形成之前恒星核合成过程中诞生的原始核素。原始核素包括251种稳定核素,以及35种半衰期极长(至少长于地球年龄的2%)的放射性核素[16]。由于这些放射性核素的半衰期非常长,衰变速率缓慢,因此它们的原子从形成之初经历数十亿年后仍得以相当的量存留到现在,其中最重的三种原始放射性核素在地壳中的衰变过程组成了现今自然界中三条最主要的衰变链,分别是以铀-238(t1⁄2=4.49×109年)为母体的铀系、以铀-235(t1⁄2=7.13×108年)为母体的锕系和以钍-232(t1⁄2=1.39×1010年)为母体的钍系[15]。除了前述三者外,还有约32种原始放射性核素并不属于上述三大衰变链之内,例如钾-40(t1⁄2=1.2×109年)、铷-87(t1⁄2=6.0×1010年)、铟-115(t1⁄2=6×1014年)、镧-138(t1⁄2=1.2×1011年)、钐-147(t1⁄2=2.5×1011年)、镥-176(t1⁄2=2.4×1010年)、铼-187(t1⁄2=4×1012年)和铋-209(t1⁄2=2.01×1019年)等。
除了286种原始核素外,自然界中还存在着50余种半衰期较短的放射性核素。这些寿命较短的天然放射性核素中,镭-226、氡-222和钋-210等质量数超过200的核素大多为钍和铀的衰变产物,是三大衰变链的中间产物。矿场和地下室的放射性危害通常是由这些短寿命核素造成的,尤其是容易扩散和被吸入的氡气,为本底辐射的主要来源,是仅次于吸烟的第二个造成肺癌的主要原因[17]。
天然核反应也会产生许多短寿命的放射性核素,例如宇宙射线作用产生的宇生放射性核素(氚、碳-14等)[15],以及地球上的原子发生自发裂变、中子捕获等作用产生的核生成核素(锝-99、钚-239等)。
还有约3000种放射性核素不存在于现今的自然界中,只能借由核反应堆和粒子加速器人工合成[15],这些人造核素大多半衰期极短,即使在地球形成的初期曾经存在,也早已全部衰变殆尽。不过许多在地球上不天然存在的短寿命核素却可在宇宙的光谱中观测到,它们是在恒星或超新星中自然产生的,例如铝-26在自然界中极为罕见,仅有宇宙射线散裂产生的痕量存在,但其在宇宙中的含量却达到天文规模。
依稳定性分级的核素统计表
[编辑]请注意,下表中的数据并不一定准确,在未来可能会发生变化(比如某些观测上稳定的核素可能具有放射性,但半衰期极长而难以观测其衰变)。
| 核稳定性等级 | 核素数量 | 累积总计 | 注释 |
|---|---|---|---|
| 稳定(不考虑质子衰变) | 90 | 90 | 包含周期表中前40种元素的所有稳定同位素。 目前尚未观测到质子衰变的现象。 |
| 理论上对一或多种已知的衰变模式不稳定,但尚未观测到其发生衰变(即观测上稳定) | 161 | 251 | 通常认定的稳定核素总数即为251种。 理论上比93 41Nb 重(含)的稳定核素都有可能自发裂变。 |
| 放射性原始核素 | 35 | 286 | 半衰期至少超过108 年(1亿年)的长寿放射性核素。 |
| 半衰期超过1小时的放射性核素 | 619 | 905 | |
| 半衰期短于1小时的放射性核素 | >2400 | >3300 |
参见
[编辑]参考文献
[编辑]- ^ 核素. 术语在线. 全国科学技术名词审定委员会. (简体中文)
- ^ IUPAC. Nuclide. A. D. McNaught; A. Wilkinson (编). Compendium of Chemical Terminology. Blackwell Scientific Publications. 1997 [2023-08-08]. ISBN 978-0-632-01765-2. doi:10.1351/goldbook.N04257. (原始内容存档于2016-12-01).
- ^ Kohman, Truman P. Proposed New Word: Nuclide. American Journal of Physics. 1947, 15 (4): 356–7. Bibcode:1947AmJPh..15..356K. doi:10.1119/1.1990965.
- ^ Belko, Mark. Obituary: Truman P. Kohman / Chemistry professor with eyes always on stars. Pittsburgh Post-Gazette. 1 May 2010 [29 April 2018]. (原始内容存档于14 December 2019).
- ^ 核種. 乐词网. 国家教育研究院. (繁体中文)
- ^ 金若水. “原子量”“分子量”历史由来及建议[J]. 中国科技术语, doi: 10.3969/j.issn.1673-8578.2005.04.004.
- ^ 7.0 7.1 7.2 叶锡溶 蔡长书. 放射化學(第二版). 台湾台北县: 新文京开发出版股份有限公司. 2008-03-26. ISBN 978-986-150-830-6 (中文(台湾)).
- ^ 存档副本. [2021-11-20]. (原始内容存档于2021-11-20).
- ^ 存档副本. [2021-11-20]. (原始内容存档于2021-11-20).
- ^ Kohman, Truman P. Proposed New Word: Nuclide. American Journal of Physics. 1947, 15 (4): 356–7. Bibcode:1947AmJPh..15..356K. doi:10.1119/1.1990965.
- ^ Belko, Mark. Obituary: Truman P. Kohman / Chemistry professor with eyes always on stars. Pittsburgh Post-Gazette. 1 May 2010 [29 April 2018]. (原始内容存档于2019-12-14).
- ^ IUPAC (Connelly, N. G.; Damhus, T.; Hartshorn, R. M.; and Hutton, A. T.), Nomenclature of Inorganic Chemistry – IUPAC Recommendations 2005 (页面存档备份,存于互联网档案馆), The Royal Society of Chemistry, 2005; IUPAC (McCleverty, J. A.; and Connelly, N. G.), Nomenclature of Inorganic Chemistry II. Recommendations 2000, The Royal Society of Chemistry, 2001; IUPAC (Leigh, G. J.), Nomenclature of Inorganic Chemistry (recommendations 1990), Blackwell Science, 1990; IUPAC, Nomenclature of Inorganic Chemistry, Second Edition 互联网档案馆的存档,存档日期2016-03-03., 1970; probably in the 1958 first edition as well
- ^ Sharma, B.K. Nuclear and Radiation Chemistry 7th. Krishna Prakashan Media. 2001: 78. ISBN 978-81-85842-63-9.
- ^ NuDat 2 Description. [2 January 2016]. (原始内容存档于2016-12-23).
- ^ 15.0 15.1 15.2 15.3 魏明通. 核化學. 五南图书出版股份有限公司. 2005. ISBN 978-957-11-3632-5.
- ^ 16.0 16.1 Radioactives Missing From The Earth.[失效链接]
- ^ Radon and Cancer: Questions and Answers - National Cancer Institute (USA). [2010-04-05]. (原始内容存档于2015-02-08).