氢氧化锶
外观
| 氢氧化锶 | |
|---|---|
| |
| 英文名 | Strontium hydroxide |
| 识别 | |
| CAS号 | 18480-07-4(无水) 1311-10-0(八水) |
| PubChem | 87672 |
| ChemSpider | 79094 |
| SMILES |
|
| InChI |
|
| InChIKey | UUCCCPNEFXQJEL-NUQVWONBAP |
| Gmelin | 847042 |
| EINECS | 242-367-1 |
| ChEBI | 35105 |
| 性质 | |
| 化学式 | Sr(OH)2 |
| 摩尔质量 | 无水:121.63 g mol−1 一水:139.65 g mol−1 八水:265.76 g·mol⁻¹ |
| 外观 | 无色潮解晶体 |
| 密度 | 3.625 g/cm3 (无水) 1.90 g/cm3 (八水) |
| 熔点 | 375 °C (无水) |
| 沸点 | 710 °C 分解 (无水) |
| 溶解性(水) | 0.41 g/100 mL (0°C) 1.77 g/100 mL (20°C) 21.83 g/100 mL (100°C)[1] |
| 溶解性 | 难溶于丙酮, 可溶于水、酸和氯化铵溶液 |
| pKb | 0.3 (第一个 OH−), 0.83 (第二个 OH−) [2] |
| 结构 | |
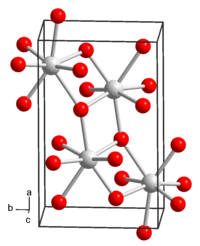
| 晶体结构 | 四方 (八水合物) |
| 危险性 | |
| 警示术语 | R:R22, R36, R37, R38 |
| 闪点 | 不可燃 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
性质[编辑]
氢氧化锶有无水物、一水合物和八水合物三种。八水合物是无色四方透明潮解晶体,有腐蚀性。水合物加热脱水得无水物。露置于空气中时吸收二氧化碳生成碳酸锶和碳酸氢锶。
氢氧化锶微溶于冷水,易溶于热水,在水中的溶解度随温度的变化较大,因此可以在水溶液中用结晶法与氢氧化钙和氢氧化钡分离。它可溶于酸和氯化铵溶液中,难溶于丙酮。可以与甘油和蔗糖形成不溶性配合物,与有机酸形成不溶性金属皂。
制备[编辑]
由硝酸锶、氯化锶或硫酸锶与氢氧化钠饱和溶液反应,冷却结晶析出八水合物,然后过滤、加热脱水得无水氢氧化锶。[3]
应用[编辑]
氢氧化锶在欧洲广泛用于甜菜糖的精炼加工,它先生成不溶性的双糖盐,经过分离、精炼后,在通入二氧化碳时,又把糖释出,同时生成难溶的碳酸锶。此外它也用作聚乙烯塑料的稳定剂,用于制取各种锶盐和锶润滑蜡,以及改进干性油和油漆的干燥性等。
参见[编辑]
参考资料[编辑]
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0070494398
- ^ Sortierte Liste: pKb-Werte, nach Ordnungszahl sortiert. – Das Periodensystem online. [2019-01-15]. (原始内容存档于2018-11-16).
- ^ Brauer, Georg. Handbook Of Preparative Inorganic Chemistry. Academic Press. 1963: 935.
| |||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|

