Fc受体:修订间差异
Pixel cube(留言 | 贡献) 无编辑摘要 |
Pixel cube(留言 | 贡献) 无编辑摘要 |
||
| 第142行: | 第142行: | ||
跨内皮/上皮层转移IgG |
跨内皮/上皮层转移IgG |
||
|} |
|} |
||
== 作用 == |
|||
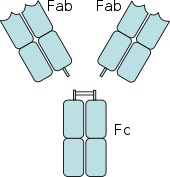
[[File:2fab_fc.svg|left|thumb|177x177px|抗体具有[[Fab]](抗原结合片段)和[[可结晶片段区域|Fc(可结晶片段区域)]]。 Fc受体与Fc区结合。]] |
|||
Fc受体存在于免疫系统的许多细胞上,包括巨噬细胞和单核细胞等吞噬细胞、中性粒细胞和嗜酸性粒细胞等粒细胞,以及[[先天免疫系統|先天免疫系统]](自然杀伤细胞)或[[后天免疫系统|适应性免疫系统]](B细胞)的淋巴细胞。<ref>{{cite journal |vauthors=Selvaraj P, Fifadara N, Nagarajan S, Cimino A, Wang G |year=2004 |title=Functional regulation of human neutrophil Fc gamma receptors |journal=Immunologic Research |volume=29 |issue=1–3 |pages=219–30 |doi=10.1385/IR:29:1-3:219 |pmid=15181284 |s2cid=85351071}}</ref><ref>{{cite journal |vauthors=Sulica A, Chambers WH, Manciulea M, Metes D, Corey S, Rabinowich H, Whiteside TL, Herberman RB |year=1995 |title=Divergent signal transduction pathways and effects on natural killer cell functions induced by interaction of Fc receptors with physiologic ligands or antireceptor antibodies |journal=Natural Immunity |volume=14 |issue=3 |pages=123–33 |pmid=8832896}}</ref><ref>{{cite journal |vauthors=Sarfati M, Fournier S, Wu CY, Delespesse G |year=1992 |title=Expression, regulation and function of human Fc epsilon RII (CD23) antigen |journal=Immunologic Research |volume=11 |issue=3–4 |pages=260–72 |doi=10.1007/BF02919132 |pmid=1287120 |s2cid=83698996}}</ref>它们允许这些细胞与附着在微生物或微生物感染细胞表面的抗体结合,并帮助这些细胞识别和消除[[微生物]][[病原体]]。Fc受体在其Fc区(或尾部)结合抗体,这种相互作用可激活拥有Fc受体的细胞。<ref>{{cite journal |vauthors=Raghavan M, Bjorkman PJ |year=1996 |title=Fc receptors and their interactions with immunoglobulins |url=https://authors.library.caltech.edu/980/1/BJOarcdb96.pdf |journal=Annual Review of Cell and Developmental Biology |volume=12 |pages=181–220 |doi=10.1146/annurev.cellbio.12.1.181 |pmid=8970726}}</ref>激活吞噬细胞是Fc受体最常见的功能。例如,巨噬细胞在与Fcγ受体结合后开始通过吞噬作用摄取并杀死IgG包被的病原体。<ref name="swanson">{{cite journal |vauthors=Swanson JA, Hoppe AD |date=December 2004 |title=The coordination of signaling during Fc receptor-mediated phagocytosis |journal=Journal of Leukocyte Biology |volume=76 |issue=6 |pages=1093–103 |doi=10.1189/jlb.0804439 |hdl=2027.42/141562 |pmid=15466916 |s2cid=13912335 |hdl-access=free}}</ref>另一个涉及Fc受体的过程称为[[ADCC作用|抗体依赖的细胞介导的细胞毒性作用(ADCC)]]。在ADCC期间,自然杀伤细胞表面的Fcγ受体III刺激自然杀伤细胞从其[[颗粒体]]中释放细胞毒性分子以杀死抗体覆盖的细胞。<ref>{{cite journal |vauthors=Sun PD |year=2003 |title=Structure and function of natural-killer-cell receptors |url=https://zenodo.org/record/1236303 |journal=Immunologic Research |volume=27 |issue=2–3 |pages=539–48 |doi=10.1385/IR:27:2-3:539 |pmid=12857997 |s2cid=29921323}}</ref> |
|||
Fcε受体I具有不一样的功能。Fcε受体I是[[粒细胞]]上的Fc受体,参与过敏反应和抵御寄生虫感染。当存在合适的过敏抗原或寄生虫时,至少两个IgE分子及其Fc受体在粒细胞表面的交联将触发细胞从其颗粒体中快速释放预先形成的介质。<ref name="fridman" /> |
|||
== 参见 == |
== 参见 == |
||
2022年12月3日 (六) 10:11的版本
| 免疫球蛋白样受体 | |
|---|---|
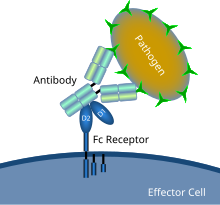 示意图显示了Fc受体与抗体包被的微生物病原体的相互作用 | |
| 鑑定 | |
| 標誌 | Fc受体 |
| 膜蛋白數據庫 | 10 |
Fc受体(英文:Fc Receptor)是在某些细胞表面发现的蛋白质,其中包括B淋巴球、滤泡树突细胞、自然杀伤细胞、巨噬细胞、中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、人类血小板和肥大细胞——它们都有助于免疫系统的保护功能。它的名字来源于它对被称为Fc(可结晶片段区域)的抗体的一部分的结合特异性。Fc受体与附着在受感染细胞或入侵的病原体上的抗体结合。它们的活性通过抗体介导的吞噬作用或抗体依赖的细胞介导的细胞毒性刺激吞噬细胞或细胞毒性细胞破坏微生物或感染细胞。一些病毒(如黄病毒)使用Fc受体来帮助它们感染细胞,这种机制被称为抗体依赖性增强感染。[1]
分类
有几种不同类型的Fc受体,它们根据它们识别的抗体类型进行分类。与最常见的一类抗体IgG结合的称为Fcγ受体,与IgA结合的称为Fcα受体,与IgE结合的称为Fcε受体。Fc受体的类别还通过表达它们的细胞(巨噬细胞、粒细胞、自然杀伤细胞、T细胞和B细胞)和每个受体的信号传导特性来区分。[2]
Fcγ受体
所有的Fcγ受体都属于免疫球蛋白超家族,是调理素(标记)微生物吞噬作用最重要的Fc受体。[3]该家族包括几个成员,Fcγ受体I(CD64)、Fcγ受体IIA(CD32)、Fcγ受体IIB(CD32)、Fcγ受体IIIA(CD16a)、Fcγ受体IIIB(CD16b),由于其不同的分子结构,它们的抗体亲和力不同。[4]例如,Fcγ受体I与IgG的结合比Fcγ受体II或Fcγ受体III更强。Fcγ受体I还具有由三个免疫球蛋白样结构域组成的细胞外部分,比Fcγ受体II或Fcγ受体III多一个结构域。这种特性允许Fcγ受体I结合单个IgG分子(或单体),但所有Fcγ受体必须结合免疫复合物中的多个IgG分子才能被激活。[5]
不同的Fcγ受体对IgG的亲和力各不相同,同样的,不同的IgG亚类对每种Fcγ受体都有独特的亲和力。这些相互作用由IgG CH2-84.4位置的聚糖(寡糖)进一步调节。 例如,通过产生位阻,含有CH2-84.4聚糖的岩藻糖会降低IgG对Fcγ受体IIIA的亲和力。相反,缺乏半乳糖并以GlcNAc部分终止的G0聚糖对Fcγ受体IIIA的亲和力会增加。
另一种Fc受体在多种细胞类型上表达,在结构上与MHC I类分子相似。该受体也结合IgG并参与该抗体的保存。[6]然而,由于这种Fc受体还参与将IgG从母亲通过胎盘转移到胎儿或通过乳汁转移到哺乳期婴儿,因此它被称为新生儿Fc受体(FcRn)。[7][8]最近,研究表明该受体在IgG血清水平的稳态中发挥作用。
Fcα受体
只有一种Fc受体属于Fcα受体亚组,称为Fcα受体I(CD89)。[9]Fcα受体I存在于中性粒细胞、嗜酸性粒细胞、单核细胞、一些巨噬细胞(包括库普弗细胞)和一些树突状细胞的表面。[9]它由两个细胞外Ig样结构域组成,是免疫球蛋白超家族和多链免疫识别受体(MIRR)家族的成员。[3]它通过与两条Fc受体γ信号链结合发出信号。[9]另一种受体也可以结合IgA,尽管它对另一种称为IgM的抗体具有更高的亲和力。[10]这种受体称为Fcα/μ受体(Fcα/μR),是一种I型跨膜蛋白。这种Fc受体在其细胞外部分有一个Ig样结构域,它也是免疫球蛋白超家族的一员。[11]
Fcε受体
已知有两种类型的Fcε受体:[3]
- 高亲和力受体Fcε受体I是免疫球蛋白超家族的成员(它有两个 Ig 样结构域)。Fcε受体I存在于表皮朗格汉斯细胞、嗜酸性粒细胞、肥大细胞和嗜碱性粒细胞中。[12][13]由于其细胞分布,该受体在控制过敏反应中起主要作用。Fcε受体I也在抗原呈递细胞上表达,并控制促炎性细胞因子的重要免疫介质的产生。[14]
- 低亲和力受体Fcε受体II(CD23)是一种C-型凝集素。Fcε受体II作为膜结合或可溶性受体具备多种功能:它能控制B细胞的生长和分化,并阻断嗜酸性粒细胞、单核细胞和嗜碱性粒细胞的IgE结合。[15]
汇总表
| 受体名称 | 主要抗体配体 | 对配体的亲和力 | 细胞分布 | 与抗体结合后的效果 |
| Fcγ受体I(CD64) | IgG1和IgG3 | 高(Kd~10−9M) | 巨噬细胞中性粒细胞嗜酸性粒细胞树突状细胞 | 吞噬作用
细胞活化 激活呼吸爆发 诱导杀灭微生物 |
| Fcγ受体IIA(CD32) | IgG | 低(Kd>10−7M) | 巨噬细胞 | 吞噬作用
脱颗粒(嗜酸性粒细胞) |
| Fcγ受体IIB1(CD32) | IgG | 低(Kd>10−7M) | B细胞肥大细胞 | 无吞噬作用
抑制细胞活性 |
| Fcγ受体IIB2(CD32) | IgG | 低(Kd>10−7M) | 巨噬细胞
中性粒细胞 嗜酸性粒细胞 |
吞噬作用
抑制细胞活性 |
| Fcγ受体IIIA(CD16) | IgG | 低(Kd>10−6M) | 自然杀伤细胞巨噬细胞(某些组织) | 诱导抗体依赖的细胞介导的细胞毒性作用(ADCC)
巨噬细胞诱导细胞因子释放 |
| Fcγ受体IIIB(CD16) | IgG | 低(Kd>10−6M) | 嗜酸性粒细胞
巨噬细胞 中性粒细胞 肥大细胞 滤泡树突细胞 |
诱导杀灭微生物 |
| Fcε受体I | IgE | 高(Kd~10−10M) | 肥大细胞
嗜酸性粒细胞 嗜碱性粒细胞 朗格汉斯细胞 单核细胞 |
脱颗粒
吞噬作用 |
| Fcε受体II(CD23) | IgE | 低(Kd>10−7M) | B细胞
嗜酸性粒细胞 朗格汉斯细胞 |
有可能的粘附分子
IgE跨肠上皮细胞转运 增强过敏性致敏的正反馈机制(B细胞) |
| Fcα受体I(CD89) | IgA | 低(Kd>10−6M) | 单核细胞
巨噬细胞 中性粒细胞 嗜酸性粒细胞 |
吞噬作用
诱导杀灭微生物 |
| Fcα/μ受体(CD351) | IgA和IgM | IgM为高,IgA为中等 | B细胞
系膜细胞 巨噬细胞 |
胞吞作用诱导杀灭微生物 |
| Fcμ受体[16] | IgM | 未知 | 人类Fcμ受体主要由淋巴细胞表达,但不由吞噬细胞表达[17] | 功能尚未完全阐明/多样化[18] |
| 新生儿Fc受体 | IgG | 在酸性细胞内体,高
在pH中性细胞外环境,低 |
单核细胞 | 通过胎盘将IgG从母亲转移到胎儿
通过乳汁将IgG从母亲转移到婴儿 保护IgG免于降解 跨内皮/上皮层转移IgG |
作用
Fc受体存在于免疫系统的许多细胞上,包括巨噬细胞和单核细胞等吞噬细胞、中性粒细胞和嗜酸性粒细胞等粒细胞,以及先天免疫系统(自然杀伤细胞)或适应性免疫系统(B细胞)的淋巴细胞。[19][20][21]它们允许这些细胞与附着在微生物或微生物感染细胞表面的抗体结合,并帮助这些细胞识别和消除微生物病原体。Fc受体在其Fc区(或尾部)结合抗体,这种相互作用可激活拥有Fc受体的细胞。[22]激活吞噬细胞是Fc受体最常见的功能。例如,巨噬细胞在与Fcγ受体结合后开始通过吞噬作用摄取并杀死IgG包被的病原体。[23]另一个涉及Fc受体的过程称为抗体依赖的细胞介导的细胞毒性作用(ADCC)。在ADCC期间,自然杀伤细胞表面的Fcγ受体III刺激自然杀伤细胞从其颗粒体中释放细胞毒性分子以杀死抗体覆盖的细胞。[24]
Fcε受体I具有不一样的功能。Fcε受体I是粒细胞上的Fc受体,参与过敏反应和抵御寄生虫感染。当存在合适的过敏抗原或寄生虫时,至少两个IgE分子及其Fc受体在粒细胞表面的交联将触发细胞从其颗粒体中快速释放预先形成的介质。[3]
参见
参考文献
- ^ Anderson R. Manipulation of cell surface macromolecules by flaviviruses. Advances in Virus Research. 2003, 59: 229–74. ISBN 9780120398591. PMC 7252169
 . PMID 14696331. doi:10.1016/S0065-3527(03)59007-8.
. PMID 14696331. doi:10.1016/S0065-3527(03)59007-8.
- ^ Owen J, Punt J, Stranford S, Jones P. Immunology 7th. New York: W.H. Freeman and Company. 2009: 423. ISBN 978-14641-3784-6.
- ^ 3.0 3.1 3.2 3.3 Fridman WH. Fc receptors and immunoglobulin binding factors. FASEB Journal. September 1991, 5 (12): 2684–90. PMID 1916092. S2CID 16805557. doi:10.1096/fasebj.5.12.1916092.
- ^ Indik ZK, Park JG, Hunter S, Schreiber AD. The molecular dissection of Fc gamma receptor mediated phagocytosis. Blood. December 1995, 86 (12): 4389–99. PMID 8541526. doi:10.1182/blood.V86.12.4389.bloodjournal86124389
 .
.
- ^ Harrison PT, Davis W, Norman JC, Hockaday AR, Allen JM. Binding of monomeric immunoglobulin G triggers Fc gamma RI-mediated endocytosis. The Journal of Biological Chemistry. September 1994, 269 (39): 24396–402. PMID 7929100. doi:10.1016/S0021-9258(19)51097-3
 .
.
- ^ Zhu X, Meng G, Dickinson BL, Li X, Mizoguchi E, Miao L, Wang Y, Robert C, Wu B, Smith PD, Lencer WI, Blumberg RS. MHC class I-related neonatal Fc receptor for IgG is functionally expressed in monocytes, intestinal macrophages, and dendritic cells. Journal of Immunology. March 2001, 166 (5): 3266–76. PMC 2827247
 . PMID 11207281. doi:10.4049/jimmunol.166.5.3266.
. PMID 11207281. doi:10.4049/jimmunol.166.5.3266.
- ^ Firan M, Bawdon R, Radu C, Ober RJ, Eaken D, Antohe F, Ghetie V, Ward ES. The MHC class I-related receptor, FcRn, plays an essential role in the maternofetal transfer of gamma-globulin in humans. International Immunology. August 2001, 13 (8): 993–1002. PMID 11470769. doi:10.1093/intimm/13.8.993
 .
.
- ^ Simister NE, Jacobowitz Israel E, Ahouse JC, Story CM. New functions of the MHC class I-related Fc receptor, FcRn. Biochemical Society Transactions. May 1997, 25 (2): 481–6. PMID 9191140. doi:10.1042/bst0250481.
- ^ 9.0 9.1 9.2 Otten MA, van Egmond M. The Fc receptor for IgA (FcalphaRI, CD89). Immunology Letters. March 2004, 92 (1–2): 23–31. PMID 15081523. doi:10.1016/j.imlet.2003.11.018.
- ^ Shibuya A, Honda S. Molecular and functional characteristics of the Fcalpha/muR, a novel Fc receptor for IgM and IgA. Springer Seminars in Immunopathology. December 2006, 28 (4): 377–82. PMID 17061088. S2CID 23794895. doi:10.1007/s00281-006-0050-3.
- ^ Cho Y, Usui K, Honda S, Tahara-Hanaoka S, Shibuya K, Shibuya A. Molecular characteristics of IgA and IgM Fc binding to the Fcalpha/muR. Biochemical and Biophysical Research Communications. June 2006, 345 (1): 474–8. PMID 16681999. doi:10.1016/j.bbrc.2006.04.084. hdl:2241/102010
 .
.
- ^ Ochiai K, Wang B, Rieger A, Kilgus O, Maurer D, Födinger D, Kinet JP, Stingl G, Tomioka H. A review on Fc epsilon RI on human epidermal Langerhans cells. International Archives of Allergy and Immunology. 1994,. 104 Suppl 1 (1): 63–4. PMID 8156009. doi:10.1159/000236756.
- ^ Prussin C, Metcalfe DD. 5. IgE, mast cells, basophils, and eosinophils. The Journal of Allergy and Clinical Immunology. February 2006, 117 (2 Suppl Mini–Primer): S450–6. PMID 16455345. doi:10.1016/j.jaci.2005.11.016.
- ^ von Bubnoff D, Novak N, Kraft S, Bieber T. The central role of FcepsilonRI in allergy. Clinical and Experimental Dermatology. March 2003, 28 (2): 184–7. PMID 12653710. S2CID 2080598. doi:10.1046/j.1365-2230.2003.01209.x.
- ^ Kikutani H, Yokota A, Uchibayashi N, Yukawa K, Tanaka T, Sugiyama K, Barsumian EL, Suemura M, Kishimoto T. Structure and function of Fc epsilon receptor II (Fc epsilon RII/CD23): a point of contact between the effector phase of allergy and B cell differentiation. Ciba Foundation Symposium. Novartis Foundation Symposia. 1989, 147: 23–31; discussion 31–5. ISBN 9780470513866. PMID 2695308. doi:10.1002/9780470513866.ch3.
- ^ FCMR Fc mu receptor [Homo sapiens (Human)] - Gene - NCBI.
- ^ Kubagawa H, Oka S, Kubagawa Y, Torii I, Takayama E, Kang DW, et al. Identity of the elusive IgMFc receptor (FcmuR) in humans. J. Exp. Med. 2009, 206 (12): 2779–93. PMC 2806608
 . PMID 19858324. doi:10.1084/jem.20091107.
. PMID 19858324. doi:10.1084/jem.20091107.
- ^ Liu J, Wang Y, Xiong E, Hong R, Lu Q, Ohno H, Wang JY. Role of the IgM Fc Receptor in Immunity and Tolerance. Frontiers in Immunology. 2019, 10: 529. PMC 6438924
 . PMID 30967868. doi:10.3389/fimmu.2019.00529
. PMID 30967868. doi:10.3389/fimmu.2019.00529  .
.
- ^ Selvaraj P, Fifadara N, Nagarajan S, Cimino A, Wang G. Functional regulation of human neutrophil Fc gamma receptors. Immunologic Research. 2004, 29 (1–3): 219–30. PMID 15181284. S2CID 85351071. doi:10.1385/IR:29:1-3:219.
- ^ Sulica A, Chambers WH, Manciulea M, Metes D, Corey S, Rabinowich H, Whiteside TL, Herberman RB. Divergent signal transduction pathways and effects on natural killer cell functions induced by interaction of Fc receptors with physiologic ligands or antireceptor antibodies. Natural Immunity. 1995, 14 (3): 123–33. PMID 8832896.
- ^ Sarfati M, Fournier S, Wu CY, Delespesse G. Expression, regulation and function of human Fc epsilon RII (CD23) antigen. Immunologic Research. 1992, 11 (3–4): 260–72. PMID 1287120. S2CID 83698996. doi:10.1007/BF02919132.
- ^ Raghavan M, Bjorkman PJ. Fc receptors and their interactions with immunoglobulins (PDF). Annual Review of Cell and Developmental Biology. 1996, 12: 181–220. PMID 8970726. doi:10.1146/annurev.cellbio.12.1.181.
- ^ Swanson JA, Hoppe AD. The coordination of signaling during Fc receptor-mediated phagocytosis. Journal of Leukocyte Biology. December 2004, 76 (6): 1093–103. PMID 15466916. S2CID 13912335. doi:10.1189/jlb.0804439. hdl:2027.42/141562
 .
.
- ^ Sun PD. Structure and function of natural-killer-cell receptors. Immunologic Research. 2003, 27 (2–3): 539–48. PMID 12857997. S2CID 29921323. doi:10.1385/IR:27:2-3:539.
拓展阅读
- Janeway CA, Travers P, Waldport M, Shlomchik MJ. Chapter 9. The Humoral Immune Response. Immunobiology: The Immune System in Health and Disease
 5th. New York: Garland. 2001. ISBN 978-0-8153-3642-6.
5th. New York: Garland. 2001. ISBN 978-0-8153-3642-6. - Abbas AK, Lichtman AH, Pillai S. Chapter 12: Effector Mechanisms of Humoral Immunity. Cellular and molecular immunology 7th. Philadelphia: Elsevier/Saunders. 2012. ISBN 978-1-4377-1528-6.
- Gerber JS, Mosser DM. Stimulatory and inhibitory signals originating from the macrophage Fcgamma receptors. Microbes and Infection. February 2001, 3 (2): 131–9. PMID 11251299. doi:10.1016/s1286-4579(00)01360-5.
- Maverakis E, Kim K, Shimoda M, Gershwin ME, Patel F, Wilken R, Raychaudhuri S, Ruhaak LR, Lebrilla CB. Glycans in the immune system and The Altered Glycan Theory of Autoimmunity: a critical review. Journal of Autoimmunity. February 2015, 57: 1–13. PMC 4340844
 . PMID 25578468. doi:10.1016/j.jaut.2014.12.002.
. PMID 25578468. doi:10.1016/j.jaut.2014.12.002.
