分子結構
此條目需要精通或熟悉相關主題的編者參與及協助編輯。 (2015年12月14日) |
此條目需要補充更多來源。 (2013年3月5日) |
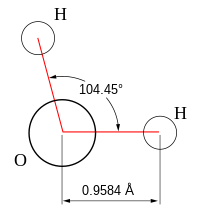
分子結構,或稱分子立體結構、分子形狀、分子幾何、分子幾何構型,建立在光譜學數據之上,用以描述分子中原子的三維排列方式。分子結構在很大程度上影響了化學物質的反應性、極性、相態、顏色、磁性和生物活性。[1][2][3]
分子結構最好在接近絕對零度的溫度下測定,因為隨着溫度升高,分子轉動也增加。量子力學和半實驗的分子模擬計算可以得出分子形狀,固態分子的結構也可通過X射線晶體學測定。體積較大的分子通常以多個穩定的構象存在,勢能面中這些構象之間的能壘較高。
分子結構涉及原子在空間中的位置,與鍵結的化學鍵種類有關,包括鍵長、鍵角以及相鄰三個鍵之間的二面角。
溫度對其的影響
[編輯]由於分子中原子的運動由量子力學決定,因此「運動」這個概念也必須要建立在量子力學基礎之上。總體(外部)的量子力學運動——如平移和旋轉幾乎不改變分子的結構(由旋轉導致的科里奧利力和離心扭曲以及由此導致的形狀變化在此可以忽略)。內部運動包括振動,隸屬於諧波,即原子即使在絕對零度仍會在平衡間振盪。此時所有原子都處于振動基態,具有零點能量,振動模式的波函數也不是一個尖峰,而是有限寬度的指數。隨着溫度升高,振動模式(自由度)被熱激發,用通俗的話講是分子振動加快,而它們仍然只在分子特定部分振盪。
玻爾茲曼分佈可以量度溫度對分子振動的影響:,其中是振動模式的激發能,是玻爾茲曼常數,是絕對溫度。在298K(25 °C)下,典型的玻爾茲曼因子值為:ΔE = 500 cm-1 → 0.089;ΔE = 1000 cm-1 → 0.008;ΔE = 1500 cm-1 → 7 * 10-4。即,如果激發能為500 cm-1,那麼大約9%的分子在室溫時會處於熱激發態。對水分子而言,其彎曲模式具有最低的激發能,大約為1600 cm-1,因此室溫下水分子中振動速度比絕對零度時快的分子占不到0.07%。
雖然轉動很難影響分子結構,但作為一個量子力學運動,相對振動而言它在低溫下熱激發程度較高。從經典力學角度來看即是,更多分子在高溫下轉動更快(它們具有更大的角速度和角動量);而從量子力學角度看則是,隨溫度升高,更多角動量較大的本徵態開始聚集。典型的轉動激發能數量級在幾cm-1。
由於涉及轉動態,很多光譜學的實驗數據都被擴大了。而轉動運動隨溫度升高而變得激烈,因此,低溫下的分子結構數據往往更加可靠,而從高溫下的光譜很難得出分子結構。
成鍵
[編輯]根據定義,分子中的原子是由共價鍵連結起來的,包括單鍵、雙鍵、叄鍵等(另一種原子的成鍵方法被成為離子鍵,並且涉及一個正的陽離子和一個負的陰離子)。
因此分子形狀可通過鍵長、鍵角和二面角這些參數來闡明。鍵長被定義為任何分子中,兩個原子中心間的平均距離;鍵角是相鄰三個原子兩條鍵之間的夾角;而二面角,或稱扭轉角,則相對於四個相鄰原子而言,是前三個原子所形成的平面與剩下一根鍵之間所成的角度。
電子的量子力學性質決定分子結構,因此可通過價鍵理論近似來理解化學鍵類型對結構的影響。雜化軌態理論認為,先有原子軌態間的雜化,才有化學鍵的生成。至於化學鍵,其中兩種最常見的為σ鍵和π鍵,而含離域電子的結構可藉助分子軌態理論來理解。
研究原子和分子中電子的類波行為隸屬於量子化學的範疇。
異構體
[編輯]具有相同化學式但不同結構的物質被稱為異構體,它們常有不同的性質。
- 純淨物只由異構體中的一種構成,因此所有分子結構相同。
- 結構異構體中原子排列順序不同,性質也常有不同,例如正丙醇和異丙醇。
- 立體異構體物理性質可能類似(例如熔點和沸點),但生化活性一般不同。這是由於它們具有手性,必須要有特定的立體結構才可以與其他底物結合。一對立體異構體可使偏振光偏轉相同的角度,但是在相反方向上。
- 蛋白質摺疊關係到高分子蛋白質的構象取向問題。
分子結構類型
[編輯]分子有六種基本形狀類型:
- 直線型:所有原子處在一條直線上,鍵角為180°,例如二氧化碳。
- 平面三角形:所有原子處在一個平面上,三個周邊原子均勻分佈在中心原子周圍,鍵角120°,例如三氟化硼。
- 四面體:四個周邊原子處在四面體的四個頂點,中心原子位於四面體中心。理想鍵角,例如甲烷。
- 八面體:六個周邊原子處在八面體的六個頂點,中心原子位於四面體中心。理想鍵角90°,例如六氟化硫SF6。
- 錐形
- 角形:與直線型相對,兩條鍵的三個原子不在一條直線上。例如水H2O,鍵角104.5°。
除了上述的基本類型外,也存在以下的分子結構:
- T形:此分子構型描述其中央原子有着三個配基的化合物形狀,二個鍵位於一直線上,另一個鍵則和上述二個鍵垂直,因此形成T形的結構,例如三氟化氯。根據價層電子對互斥理論,T形分子構型是三個配基和兩個中央原子的孤電子對相互作用造成的結果。
- 三帽三角稜柱:分子構型描述有九個原子、原子基團或配基被安排在一個中心原子周圍的形狀,利用三側錐三角柱(一個有着和三個矩形面相接觸的額外原子的三角柱)定義此種分子的頂點。這和帽狀方形反稜柱分子構型非常相似,並且在某些分子中對於此特定的幾何構型展現出一些爭議。九氫合錸(VII)酸鉀中的九氫合錸(VII)酸根離子通常被視為擁有三帽三角稜柱分子構型,雖然有時此幾何構型用帽狀方形反稜柱分子構型所取代。
- 三角稜形:分子構型描述有六個原子、原子基團或配基被安排在一個中心原子周圍的形狀,利用三角柱定義此種分子的頂點。
- 五角平面:分子構型描述有五個原子、原子基團或配基被安排在一個中心原子周圍的形狀,利用五角型定義此種分子的頂點。
- 五角錐:分子構型描述有六個原子、原子基團或配基被安排在一個中心原子周圍的形狀,利用五角錐形定義此種分子的頂點。這是有着不均勻鍵角的少數分子鍵的其中一種。
- 帽狀方形:反稜柱分子構型描述有八個原子、原子基團或配基被安排在一個中心原子周圍的形狀,利用正四角錐反角柱定義此種分子的頂點。 正四角錐反角柱是一種有着正四角反稜柱的四角錐去連接到方形的底部。在這方面,這可以被看成「覆蓋的」正四角反稜柱(一個有着錐體豎立在某個方形面的正四角反稜柱)。這和三帽三角稜柱分子構型非常相似,並且在某些分子中對於此特定的幾何構型展現出一些爭議。九氫合錸(VII)酸根有時被視為擁有帽狀方形反稜柱分子構型,雖然有時她的幾何構型用三帽三角稜柱分子構型所取代。
- 扭曲或覆蓋孤電子對的八面體:分子構型描述有六個原子、原子基團或配基被安排在一個中心原子周圍的形狀(有着一電子對覆蓋着八面體),利用兩個倒立相連的三角錐形定義此種分子的頂點。這種形狀有着分子對稱性。
- 方形反稜柱分子構型:有八個原子、原子基團或配體連接在一個中心原子周圍的分子構型,其分子形狀類似正四角反稜柱。像八氟合氙(VI)酸亞硝酰中的八氟合氙(VI)酸根離子離子即為此構型。
- 蹺蹺板形:或稱蝴蝶骨型,是一種和中央原子有四個鍵結並擁有C2v對稱性的分子構型,名稱"蹺蹺板"的來源是因為其在觀察中看起來像蹺蹺板。和中央原子有四個鍵結的構型中,最常見的為四面體,或是較少見的,方形平面構型,所以蹺蹺板形分子構型就像他的名字一樣,是很少見的。
| 鍵連原子 | 孤對電子 | 電子對數 | 形狀 | 理想鍵角 | 例子 | 圖片 |
|---|---|---|---|---|---|---|
| 2 | 0 | 2 | 直線形 | 180° | CO2 | |
| 3 | 0 | 3 | 平面三角形 | 120° | BF3 | |
| 2 | 1 | 3 | 角形 | 120° (119°) | SO2 | |
| 4 | 0 | 4 | 四面體形 | 109.5° | CH4 | 
|
| 3 | 1 | 4 | 三角錐形 | 107° | NH3 | |
| 2 | 2 | 4 | 角形 | 109.5° (104.5°) | H2O | |
| 5 | 0 | 5 | 三角雙錐形 | 90°, 120°, 180° | PCl5 | 
|
| 4 | 1 | 5 | 變形四面體形 | 180°, 120°, 90° (173.1°, 101.6°) | SF4 | |
| 3 | 2 | 5 | T字形 | 90°, 180° (87.5°, < 180°) | ClF3 | |
| 2 | 3 | 5 | 直線形 | 180° | XeF2 | |
| 6 | 0 | 6 | 八面體形 | 90°, 180° | SF6 | 
|
| 5 | 1 | 6 | 四角錐形 | 90° (84.8°), 180° | BrF5 | |
| 4 | 2 | 6 | 平面四方形 | 90°, 180° | XeF4 | |
| 7 | 0 | 7 | 五角雙錐形 | 90°, 72°, 180° | IF7 | 
|
| 7 | 0 | 7 | 截角八面體 | MoF7− | 
| |
| 7 | 0 | 7 | 側錐三角柱 | TaF72− | ||
| 6 | 1 | 7 | 五角錐形 | 72°, 90°, 144° | XeOF5− | |
| 6 | 1 | 7 | 變形八面體 | XeF6 | 
| |
| 5 | 2 | 7 | 平面五角形 | 72°, 144° | XeF5− | |
| 8 | 0 | 8 | 四方反稜柱形 | XeF82− | ||
| 8 | 0 | 8 | 十二面體 | Mo(CN)84− | 
| |
| 8 | 0 | 8 | 雙帽三稜柱 | ZrF84− | ||
| 9 | 0 | 9 | 三側錐三角柱形 | ReH92− | 
| |
| 9 | 0 | 9 | 單帽四角反稜柱 | [LaCl(H2O)7]24+ | 
| |
| 10 | 0 | 10 | 雙四角錐反角柱 | Th(C2O4)42− [4] | 
| |
| 11 | 0 | 11 | 五角錐反角柱 | [ThIV(NO3)4(H2O)3] [4] | 
| |
| 12 | 0 | 12 | 二十面體 | Mg[Th(NO3)6].8H2O 裏的 Th(NO3)62−離子[5] |

|
參考文獻
[編輯]- ^ McMurry, J. (1992). Organic Chemistry (3rd Edn.), Belmont:Wadsworth. ISBN 0-534-16218-5
- ^ Cotton, F. Albert; Wilkinson, Geoffrey; Murillo, Carlos A.; Bochmann, Manfred (1999). Advanced Inorganic Chemistry (6th Edn.) New York:Wiley-Interscience. ISBN 0-471-19957-5.
- ^ Alexandros Chremos; Jack F. Douglas. When does a branched polymer become a particle?. J. Chem. Phys. 2015, 143 (11): 111104. Bibcode:2015JChPh.143k1104C. PMID 26395679. doi:10.1063/1.4931483
 .
.
- ^ 4.0 4.1 Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
參見
[編輯]外部連結
[編輯]- 共價鍵和分子結構 (頁面存檔備份,存於互聯網檔案館)
- 超分子形狀 (頁面存檔備份,存於互聯網檔案館)(蛋白質、DNA和RNA)http://swift.cmbi.ru.nl/(頁面存檔備份,存於互聯網檔案館)
- 3D化學 (頁面存檔備份,存於互聯網檔案館)——化學,結構和3D分子
- IUMSC——印第安納州大學分子結構中心
- 分子結構
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|















