氯金酸鈉
外觀
| 氯金酸鈉 | |
|---|---|
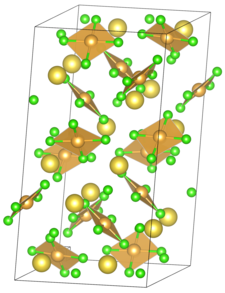
| |
| IUPAC名 Sodium tetrachloroaurate(III) | |
| 別名 | 氯化金鈉 黃色氯化金 |
| 識別 | |
| CAS號 | 15189-51-2(無水) 13874-02-7(二水) |
| PubChem | 27127 |
| ChemSpider | 25247 |
| SMILES |
|
| InChI |
|
| 性質 | |
| 化學式 | NaAuCl4 |
| 摩爾質量 | 361.756 g·mol⁻¹ |
| 外觀 | 橙色粉末 |
| 密度 | 3.81 g·cm−3[2] |
| 溶解性(水) | 139 g/100 ml (10°C) 151 g/100 ml (20°C) 900 g/100 ml (60°C)[3] 150 g/100 ml(10 °C,二水) |
| 溶解性 | 難溶於乙醚[4] |
| 危險性[5] | |
GHS危險性符號 
| |
| GHS提示詞 | Danger |
| H-術語 | H315, H319, H335 |
| P-術語 | P261, P264, P271, P280, P302+352, P332+313, P305+351+338, P337+313, P304+340, P312, P330, P333+313, P363, P403+233 |
| 相關物質 | |
| 其他陽離子 | 氯金酸 氯金酸鋰 氯金酸鉀 氯金酸銨 氯金酸銫 氯金酸銀 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氯金酸鈉是一種無機化合物,化學式 NaAuCl4。它是由 Na+ 和AuCl4−離子組成的。在室溫下,它是金橙色的固體。它的無水物和二水物可以商購。
製備
[編輯]製備四氯金酸鈉的常規方法包括將氯金酸溶液加入氯化鈉或碳酸鈉中,以形成混合物。將混合物在100℃下攪拌,然後蒸發、冷卻、結晶和乾燥,得到橙色的氯金酸鈉晶體。[4][6]
- H[AuCl
4] + NaCl → Na[AuCl
4] + HCl
- 2 H[AuCl
4] + Na
2CO
3 → 2 Na[AuCl
4] + H
2O + CO
2
用處
[編輯]氯金酸鈉是乙炔氫氯化反應的催化劑,也用於硫化物的氧化。[4]
參考資料
[編輯]- ^ PubChem. Sodium tetrachloroaurate. pubchem.ncbi.nlm.nih.gov. [2019-05-19]. (原始內容存檔於2021-11-09) (英語).
- ^ Jones, P. G.; Hohbein, R.; Schwarzmann, E. Anhydrous sodium tetrachloroaurate(III). Acta Crystallographica Section C Crystal Structure Communications (International Union of Crystallography (IUCr)). 1988-07-15, 44 (7): 1164–1166. ISSN 0108-2701. doi:10.1107/s0108270188002756.
- ^ Perry, Dale L. Handbook of Inorganic Compounds. CRC Press; 2 edition (May 18, 2011). 2011: 380. ISBN 9781439814611.
- ^ 4.0 4.1 4.2 Westcott, Stephen A., Sodium Tetrachloroaurate(III), Encyclopedia of Reagents for Organic Synthesis, American Cancer Society, 2001, ISBN 9780470842898, doi:10.1002/047084289x.rs108 (英語)
- ^ Sodium Tetrachloroaurate. www.espimetals.com. [2019-05-20]. (原始內容存檔於2016-05-01).
- ^ 20180208476,LU, Lin; Chen-hsiang Wang & Kuei-sheng Fan et al.,「Method of Making Inorganic Gold Compound」,發行於2018-07-26 (頁面存檔備份,存於網際網路檔案館) 存档副本. [2021-11-08]. 原始內容存檔於2022-01-28.
