离子键
此条目没有列出任何参考或来源。 (2019年3月13日) |
此条目可参照英语维基百科相应条目来扩充。 |
离子键又被称为盐键,是化学键的一种,通过两个或多个原子或化学基团失去或获得电子而成为离子后形成。带相反电荷的原子或基团之间存在静电吸引力,两个带相反电荷的原子或基团靠近时,周围水分子被释放为自由水中,带负电和带正电的原子或基团之间产生的静电吸引力以形成离子键。是离子化合物中发生的主要相互作用。它是与共价键和金属键一起的主要键合类型之一。
此类化学键往往在金属与非金属间形成。失去电子(形成阳离子/正离子)的往往是金属元素的原子,而获得电子(形成阴离子/负离子)的往往是非金属元素的原子。带有相反电荷的离子因电磁力而相互吸引,从而形成化学键。离子键较氢键强,其强度与共价键接近。
仅当总体的能级下降的时候,反应才会发生(由化学键联接的原子较自由原子有着较低的能级)。下降越多,形成的键越强。
现实中,原子间并不形成“纯”离子键(即:其中一个原子或分子将电子完全转移给另一个)。所有的键都或多或少带有共价键的成分。成键原子之间电平均程度越高,离子键成分越低。
一般说来,以离子键键合的化合物(即“离子化合物”)在固态下不导电,在液态下或形成溶液后导电;它们的熔点一般比较高——这决定于组成它们的离子的电荷:电荷越高,熔点越高;反之亦然。

|
|
|
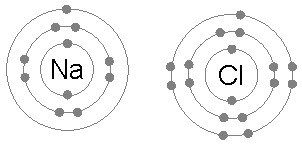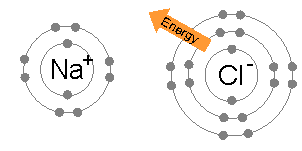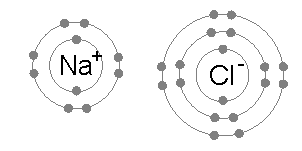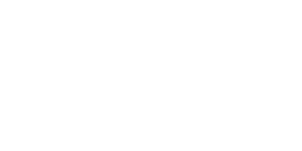
上图表示锂原子和氟原子的电子分布。锂原子只有一个外层电子,原子核对该电子的束缚十分弱(表现为其第一电离能很小)。而氟原子有7个外层电子。如果锂原子的外层电子进入氟原子的外层轨道,则两个原子就都有了类似惰性气体原子的电子分布。键能(源自两个带有相反电荷的离子因的电磁力的吸引作用)的存在(其值为负数)使得成键后的总体能量水平低于未成键的状态。 |
两个离子间的吸引(例如和)形成离子键。电子轨道一般不会重叠(因而没有形成分子轨道),因为两个离子都达到了最低的能级,而键的完全形成(理想状态下)是因为正负离子间的电磁相互作用。 |
参见
[编辑]
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||
|







