二氧化锔
外观
| 二氧化锔 | |
|---|---|
| |
| 别名 | 氧化锔(IV) |
| 识别 | |
| CAS号 | 12016-67-0 |
| SMILES |
|
| EC编号 | 234-612-6 |
| 性质 | |
| 化学式 | CfO2 |
| 摩尔质量 | 283 g·mol−1 |
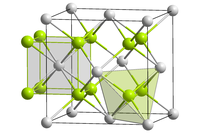
| 外观 | 黑色固体[1] |
| 熔点 | 380 °C(分解)[2] |
| 结构 | |
| 空间群 | Fm3m (No. 225) |
| 晶格常数 | a = 536 pm |
| 相关物质 | |
| 其他阴离子 | 四氟化锔 |
| 相关化学品 | 三氧化二锔 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
二氧化锔是锔的一种氧化物,化学式 CmO2。由于所有锔的同位素都是人造的,所以它不存在于自然界。在核反应堆中,它可以由中子照射二氧化铀 (UO2) 或二氧化钚 (PuO2)而成。
制备
[编辑]它也可以由草酸锔 (Cm2(C2O4)3) 或硝酸锔 (Cm(NO3)3) 热分解而成。
它也可以由三氧化二锔 (Cm2O3) 在 650 °C的氧气气氛下反应而成。[4]
性质
[编辑]物理性质
[编辑]二氧化锔是一种黑色固体,为萤石结构,空间群 Fm3m (No. 225),晶格参数 536 pm。[5]
化学性质
[编辑]二氧化锔在380 °C 分解成 CmO1,95,然后在430 °C进一步分解成三氧化二锔。[2]不过在氧气气氛下,二氧化锔在更高的温度也是稳定的(见#制备)。
参考资料
[编辑]- ^ Gregg J. Lumetta, Major C. Thompson, Robert A. Penneman, P. Gary Eller: Curium, in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 1397–1443 (doi:10.1007/1-4020-3598-5_9).
- ^ 2.0 2.1 W. C. Mosley: Phases and Transformations in the Curium-Oxygen System, in: J. Inorg. Nucl. Chem., 1972, 34 (2), S. 539–555 (doi:10.1016/0022-1902(72)80434-2).
- ^ Asprey, L. B.; Ellinger, F. H.; Fried, S.; Zachariasen, W. H. Evidence for Quadrivalent Curium: X-Ray Data on Curium Oxides. Journal of the American Chemical Society. 1955-03, 77 (6): 1707–1708 [2021-08-29]. ISSN 0002-7863. doi:10.1021/ja01611a108. (原始内容存档于2021-08-29) (英语).
- ^ Noé, M.; Fuger, J. Self-radiation effects on the lattice parameter of 244CmO2. Inorganic and Nuclear Chemistry Letters. 1971-05, 7 (5): 421–430 [2021-08-29]. doi:10.1016/0020-1650(71)80177-0. (原始内容存档于2020-08-01) (英语).
- ^ Wallmann, J.C. A structural transformation of curium sesquioxide. Journal of Inorganic and Nuclear Chemistry. 1964-12, 26 (12): 2053–2057. doi:10.1016/0022-1902(64)80149-4 (英语).
扩展阅读
[编辑]- Gregg J. Lumetta, Major C. Thompson, Robert A. Penneman, P. Gary Eller: Curium (页面存档备份,存于互联网档案馆), in: Lester R. Morss, Norman M. Edelstein, Jean Fuger (Hrsg.): The Chemistry of the Actinide and Transactinide Elements, Springer, Dordrecht 2006; ISBN 1-4020-3555-1, S. 1397–1443 (doi:10.1007/1-4020-3598-5_9).
| |||||||||||||||||

![{\displaystyle {\ce {Cm + O2 ->[\Delta T] CmO2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d46ff3d0ced7dfbbc28d3abd37b5362af12d0782)
![{\displaystyle {\ce {2 Cm2O3 + O2 ->[\Delta T] 4 CmO2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d3ad302409428ad21aff1d0b37d5564a4ab617d9)