二氟化氧
| 二氟化氧 | |
|---|---|

| |
| |
| 别名 | 氟化氧 次氟酸酐 |
| 识别 | |
| CAS号 | 7783-41-7 |
| PubChem | 24547 |
| ChemSpider | 22953 |
| SMILES |
|
| InChI |
|
| InChIKey | UJMWVICAENGCRF-UHFFFAOYAI |
| EINECS | 231-996-7 |
| ChEBI | 30494 |
| RTECS | RS2100000 |
| 性质 | |
| 化学式 | OF2 |
| 摩尔质量 | 53.9962 g·mol⁻¹ |
| 外观 | 無色氣體,冷凝后得到淡黃色液體 |
| 密度 | -145°C液态下为1.9 g/cm3 |
| 熔点 | −223.8 °C |
| 沸点 | −144.8 °C |
| 溶解性(其他溶劑) | 一升水能溶解68毫升二氟化氧(0℃) |
| 热力学 | |
| ΔfHm⦵298K | 24.5 kJ mol−1 |
| 相关物质 | |
| 相关化学品 | HFO O2F2 NHF2 NF3 SCl2 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
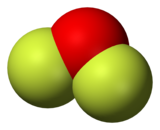
二氟化氧是化学式为OF2的化合物,结构与水分子相似,但化学性质非常不同,是强氧化剂。
制备[编辑]
二氟化氧于 1929年首次被报告。它是由溶蚀的氟化钾和含有少量水的氢氟酸电解而成的。[1][2]现在的制备方法是将氟气通入氢氧化钠溶液中,可得二氟化氧和副产物氟化钠。
- 2F2 + 2NaOH → OF2 + 2NaF + H2O
反应[编辑]
二氟化氧中的氧具有不寻常的+2氧化态[3][4] ,具有强氧化性。200°C时二氟化氧分解成氧气和氟气。
二氟化氧与许多金属反应,生成氧化物和氟化物。也能与一些非金属反应:
二氟化氧与水缓慢反应,生成氢氟酸:
- OF2(aq) + H2O(aq) → 2HF(aq) + O2(g)
- OF2 + SO2 → SO3 + F2
有紫外线照射时,产物变为硫酰氟(SO2F2)和焦硫酰氟(S2O5F2):
- OF2 + 2SO2 → S2O5F2
安全性[编辑]
二氟化氧因其极强的氧化性,被认为是一种不安全的气体。OF2与水水解产生的氢氟酸具有很强的腐蚀性和毒性,能够导致坏死,从骨骼中浸出钙,并造成心血管损伤,以及其他一系列隐性影响。
大众文化[编辑]
Robert L. Forward的科幻小说《30K卡美洛》(Camelot 30K)中,二氟化氧被生活在柯伊伯带的虚构生物用作生化溶剂。OF2在30K下是固体,这种虚构生物可以吸热,通过放射性加热保持较高的体温和液态OF2血液。
参考文献及注释[编辑]
- ^ Lebeau, P.; Damiens, A. Sur un nouveau mode de préparation du fluorure d'oxygène [A new method of preparation of oxygen fluoride]. Comptes rendus hebdomadaires des séances de l'Académie des Sciences. 1929, 188: 1253–1255 [February 21, 2013]. (原始内容存档于2017-12-08) (法语). (页面存档备份,存于互联网档案馆)
- ^ Lebeau, P.; Damiens, A. Sur l'existence d'un composé oxygéné du fluor [The existence of an oxygen compound of fluorine]. Comptes rendus hebdomadaires des séances de l'Académie des Sciences. 1927, 185: 652–654 [February 21, 2013]. (原始内容存档于2020-04-14) (法语). (页面存档备份,存于互联网档案馆)
- ^ 通常氧呈-2价,但这里氧为正价,氟为负价(因為氟的電負性大於氧),因此二氟化氧是氟化物而非氧化物。
- ^ https://www.nature.com/articles/120842a0
外部链接[编辑]
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
