氰化钙
| 氰化钙 | |
|---|---|
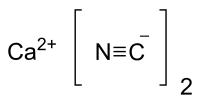
| |
| IUPAC名 Calcium cyanide | |
| 识别 | |
| CAS号 | 156-62-7 |
| PubChem | 4685067 |
| ChemSpider | 10669887 |
| SMILES |
|
| InChI |
|
| InChIKey | STRTXDFFNXSZQB-UHFFFAOYAA |
| UN编号 | 1403 |
| EINECS | 205-861-8 |
| RTECS | GS6000000 |
| 性质 | |
| 化学式 | CaCN2 |
| 摩尔质量 | 80.102 g/mol g·mol⁻¹ |
| 外观 | 白色固體(不純時呈灰黑色) |
| 氣味 | 無味 |
| 密度 | 2.29 g/cm3 |
| 熔点 | 1340 °C [1] |
| 沸点 | 1150-1200 °C (昇華) |
| 溶解性(水) | 反應 |
| 危险性 | |
| 警示术语 | R:R22 R37 R41 |
| 安全术语 | S:S2 S22 S26 S36/37/39 |
| MSDS | ICSC 1639 |
| 欧盟编号 | 615-017-00-4 |
| 欧盟分类 | 有害 (Xn) 刺激性 (Xi) |
| NFPA 704 | |
| 闪点 | 非易燃 |
| 相关物质 | |
| 相关化学品 | 氰化钠 氰氨化钙 電石 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
氰化鈣(化學式:Ca(CN)2),無色或白色粉末,工業品呈灰黑色,味苦,有劇毒。
性質[编辑]
溶於水和弱酸,生成氰化氫(HCN);暴露於潮濕空氣中也會放出劇毒氣體。
和硫反应产生硫氰酸钙:
- Ca(CN)2 + S → Ca(SCN)2
製備[编辑]
可用氰氨化鈣與碳共熱至1000℃以上而得。
安全[编辑]
攝入後會和其他的氰化物一樣,當這化合物被吸收進血液時,當中的氰離子即時進入所有細胞中,而且抑制在細胞中的線粒體中的細胞色素氧化酶(a3),引致在呼吸作用中,電子傳遞鏈不能順利進行,從而使細胞無法藉需氧呼吸獲得能量,引致細胞只能進行缺氧呼吸以維持生命活動,造成細胞窒息。
此外,由於所有細胞都只能進行缺氧呼吸,肝臟細胞又無法進行需氧呼吸以把缺氧呼吸得出的乳酸氧化或轉變成糖原,引致乳醱積累在血液中,造成血液的pH值下降,引致代謝性醱中毒。血液中pH值的進一步下降更加把身體細胞中大部份的酶進一步抑制,使身體機能癱瘓,引致死亡。
吸入、口服或經皮吸收可引起急性中毒,大劑量吸入會死亡。
参考资料[编辑]
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0070494398
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

