克腦文蓋爾縮合反應
| 克腦文蓋爾縮合反應 | |
|---|---|
| 命名根據 | 克腦文蓋爾 |
| 反應類型 | 偶聯反應 |
| 標識 | |
| 有機化學網站對應網頁 | 克腦文蓋爾縮合 |
| RSC序號 | RXNO:0000044 |
Knoevenagel縮合反應(爾文格反應;克諾維那蓋爾縮合反應;柯諾瓦諾格反應;克爾文蓋爾縮合反應),又稱Knoevenagel反應
含有活潑亞甲基的化合物與醛或酮在弱鹼催化下,發生失水縮合生成α,β-不飽和羰基化合物及其類似物。

Z 基是吸電子基團,一般為 CHO、COR、COOR、COOH、CN、NO2 等基團。兩個 Z 基可以相同,也可以不同。NO2 的吸電子能力很強,有一個就足以產生活潑氫。
常用的催化劑有哌啶、吡啶、喹啉和其他一級胺、二級胺等。常用的活潑亞甲基化合物有丙二酸二乙酯、米氏酸、乙醯乙酸乙酯、硝基甲烷和丙二酸等,但事實上任何含有能被鹼除去氫原子的 C-H 鍵化合物都能發生此反應。
Knoevenagel 反應是對Perkin反應的改進,活潑亞甲基化合物的存在,使得弱鹼作用下,就能產生足夠濃度的碳負離子進行親核加成。弱鹼的使用避免了醛酮的自身縮合,因此除芳香醛外,酮和脂肪醛均能進行反應,擴大了適用範圍。
Knoevenagel 反應是製備 α,β-不飽和化合物的常用方法之一。
歷史[編輯]
這個反應最早是由德國化學家亞瑟·漢斯發現的,1885年,他用乙酰乙酸乙酯、苯甲醛和氨反應,發現生成了對稱的縮合產物 2,6-二甲基-4-苯基-1,4-二氫吡啶-3,5-二甲酸二乙酯,也生成了少量的 2,4-二乙酰基-3-苯基戊二酸二乙酯,這是有關 Knoevenagel 反應的最早紀錄。[1][2][3]
1894年,德國化學家 Emil Knoevenagel 從多個方面對這一反應作了進一步研究,他發現任何一級和二級胺都可以促進反應進行;反應可以分步進行;而且丙二酸酯可以代替乙酰乙酸乙酯作為活性的亞甲基化合物。[4][5]
兩年之後,Knoevenagel 又開始了對這個反應的研究,他發現,在室溫或 0 °C 時,苯甲醛與過量乙酰乙酸乙酯在催化量的哌啶作用下,會生成雙加成物 2,4-二乙酰基-3-苯基戊二酸二乙酯。他的一個助手重複了這個實驗,在冷卻一步上消耗了更少的時間,結果發現得到的產物與之前的產物不同,這次的產物是縮合產物苄叉乙酰乙酸乙酯與上述雙加成物的混合物。進一步的研究又發現,如果使用等摩爾的苯甲醛和乙酰乙酸乙酯,將反應溫度控制在 0 °C,那麼兩者之間的反應便可以定量生成縮合產物苄叉乙酰乙酸乙酯,而基本上不產生加成物。[6] 這便是現今所看到的 Knoevenagel 反應的雛形,縮合產物苄叉(或烷叉)乙酰乙酸乙酯也被稱為 Knoevenagel 產物。但實際上,Claisen 等早在十餘年前就已經通過其他方法得到該類型的化合物了,[7][8] 只不過 Knoevenagel 所用的方法和條件更溫和一些而已。
此後的研究表明,如果用原始反應條件處理苄叉乙酰乙酸乙酯,又可得到雙加成物,從而證實了苄叉乙酰乙酸乙酯是雙加成物生成過程中的中間產物。
反應機理[編輯]
Knoevenagel 是由鹼催化的縮合反應,類似於羥醛反應。根據所用鹼種類的不同,可以有兩種可行的機理。一種是認為醛或酮先與胺縮合為亞胺,然後再與碳負離子加成。

這個機理與 Knoevenagel 最初提出的機理(下圖)有些類似。在 Knoevenagel 發現這個反應之前,就已知苯甲醛可以與兩分子的哌啶縮合,生成苄叉二哌啶縮氨醛。而且苄叉二哌啶縮氨醛與乙酰乙酸乙酯在乙醇中作用時,可以高產率得到下圖中的最終產物雙加成物。[9] 因此 Knoevenagel 認為,反應的機理應是胺與醛先縮合為縮氨醛,受乙酰乙酸乙酯進攻,產生 β-氨基二羰基化合物中間產物,然後消除哌啶得到 α,β-不飽和羰基化合物,並最後與另一分子乙酰乙酸乙酯進行Michael加成,得最終的雙加成產物。
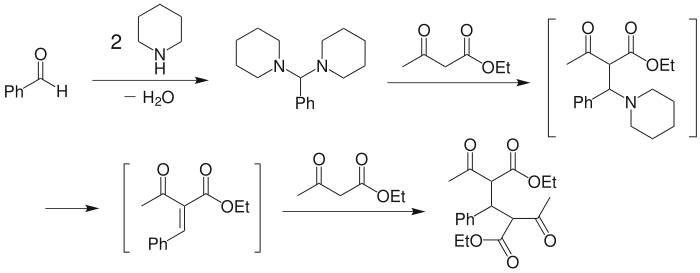
另一種機理(Hann–Lapworth 機理)則認為,首先是丙二酸二乙酯與醛在鹼作用下羥醛加成為 β-羥基二羰基化合物中間產物,然後再消除水得到縮合產物。

上述兩種機理中的中間產物 β-氨基二羰基化合物[10] 和 β-羥基二羰基化合物[11] 都已從不同的反應中分離出來。一般認為,當反應用鹼為三級胺時,Hann–Lapworth 機理占主導地位;而當反應用鹼為一級或二級胺時,兩種機理都有可能發生。
改進法[編輯]
Doebner改進法,又稱Verley–Doebner改進法
用丙二酸或丙二酸酯作原料時,反應產生的烷叉丙二酸(酯),(經水解)可在吡啶作用下繼續脫去一個羧基,生成單羧酸。[12] 例如,丙烯醛與丙二酸在吡啶中反應,可得脫羧產物反式-2,4-戊二烯酸。[13]

應用[編輯]
1、2-甲氧基苯甲醛與二乙基硫代巴比妥酸在乙醇中發生 Knoevenagel 反應,以哌啶作鹼,可得電荷轉移絡合物 (3)。[14]

2、抗瘧疾藥物本芴醇(lumefantrine)製取中的最後一步。[15] 反應最初產物是 E/Z 異構體的 50:50 混合物,但最終會轉化為熱力學上更穩定的 Z 型異構體。
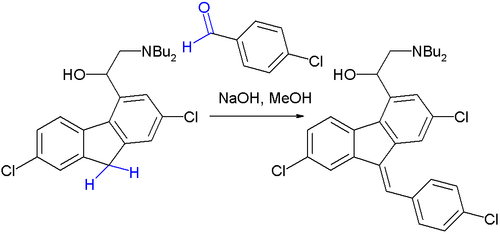
3、微波促進的環己酮、丙二腈和3-氨基-1,2,4-三唑之間發生的多組分反應。[16]

參見[編輯]
參考資料[編輯]
- ^ Dr. Arthur Hantzsch. Ueber die Synthese pyridinartiger Verbindungen aus Acetessigäther und Aldehydammoniak. Justus Liebigs Ann. Chem. 1882, 215 (1): 1–82. doi:10.1002/jlac.18822150102.
- ^ A. Hantzsch. Ueber die Condensation von Acetessigsäuremethyläther mit Aldehydammoniak. Ber. Dtsch. Chem. Ges. 1883, 16 (2): 1946–1948. doi:10.1002/cber.18830160282.
- ^ A. Hantzsch. Versuche zur Constitutionsbestimmung der synthetischen Hydropyridinderivate. Ber. Dtsch. Chem. Ges. 1885, 18 (2): 2579–2586. doi:10.1002/cber.188501802158.
- ^ E. Knoevenagel. 1,5-Diketone. Justus Liebigs Ann. Chem. 1894, 281 (1): 25–126. doi:10.1002/jlac.18942810104.
- ^ E. Knoevenagel. Ueber eine Darstellungsweise der Glutarsäure. Ber. Dtsch. Chem. Ges. 1894, 27 (2): 2345–2346. doi:10.1002/cber.189402702229.
- ^ E. Knoevenagel. Ueber eine Darstellungsweise des Benzylidenacetessigesters. Ber. Dtsch. Chem. Ges. 1896, 29 (1): 172–174. doi:10.1002/cber.18960290133.
- ^ L. Claisen. Condensationen der Aldehyde mit Acetessig- und Malonsäureäther. Ber. Dtsch. Chem. Ges. 1881, 14 (1): 345–349. doi:10.1002/cber.18810140181.
- ^ L. Claisen, L. Crismer. Ueber die Einwirkung von Benzaldehyd auf Malonsäure und Malonsäureäther. Justus Liebigs Ann. Chem.: 129–144. doi:10.1002/jlac.18832180203.
- ^ Emil Knoevenagel. Condensation von Malonsäure mit Aromatiachen Aldehyden durch Ammoniak und Amine. Ber. Dtsch. Chem. Ges. 1898, 31: 2596–2619. doi:10.1002/cber.18980310308.
- ^ Rikuhei Tanikaga, Tadashi Tamura, Yoshihito Nozaki and Aritsune Kaji. Selective synthesis of α-sulphenyl-, α-sulphinyl-, and α-sulphonyl-α,β-unsaturated carbonyl compounds by the knoevenagel reaction. J. Chem. Soc., Chem. Commun. 1984, (2): 87–88. doi:10.1039/C39840000087.
- ^ Genji Iwasaki, Seitaro Saeki and Masatomo Hamana. A Novel Nucleophilic Substitution of the Formyl Group in p-Nitrobenzaldehyde with Some Carbanions. Chem. Lett. 1986, 15 (2): 173–176. doi:10.1246/cl.1986.173.
- ^ O. Doebner. Ueber die der Sorbinsäure homologen, ungesättigten Säuren mit zwei Doppelbindungen. Ber. Dtsch. Chem. Ges. 1902, 35: 1136–1136. doi:10.1002/cber.190203501187.
- ^ Peter J. Jessup, C. Bruce Petty, Jan Roos, and Larry E. Overman (1988). "1-N-Acylamino-1,3-dienes from 2,4-pentadienoic acids by the curtius rearrangement: benzyl trans-1,3-butadiene-1-carbamate". Org. Synth.; Coll. Vol. 6: 95.
- ^ Abdullah Mohamed Asiria, Khaled Ahmed Alamrya Abraham F. Jalboutb, Suhong Zhang. 1,3-Diethyl-5-(2-methoxybenzylidene)-2-thioxodihydropyrimidine-4,6(1H,5H)-dione. Molbank. 2004: M359 [2009-09-11]. (原始內容存檔於2011-07-09).
- ^ Ulrich Beutler, Peter C. Fuenfschilling, and Andreas Steinkemper. An Improved Manufacturing Process for the Antimalaria Drug Coartem. Part II. Org. Process Res. Dev. 2007, 11 (3): 341–345. doi:10.1021/op060244p.
- ^ Anshu Dandia, Pritima Sarawgi, Kapil Arya, and Sarita Khaturia. Mild and ecofriendly tandem synthesis of 1,2,4-triazolo[4,3-a]pyrimidines in aqueous medium (PDF). Arkivoc. 2007, (06-2251BP): 83–92 [2009-09-11]. (原始內容 (PDF)存檔於2007-09-29).
