三氧化二锰
外观
| 三氧化二锰 | |
|---|---|
| |

| |
| IUPAC名 dimanganese trioxide | |
| 别名 | 氧化锰(III) |
| 识别 | |
| CAS号 | 1317-34-6 |
| PubChem | 14824 |
| SMILES |
|
| RTECS | OP915000 |
| 性质 | |
| 化学式 | Mn2O3 |
| 摩尔质量 | 157.8743 g/mol g·mol⁻¹ |
| 外观 | 棕色或黑色晶体 |
| 密度 | 4.5 g/cm3 |
| 熔点 | 888 °C(1,161 K)(α型) 940 °C(1,210 K)(β型)(分解) |
| 溶解性(水) | 0.00504 g/100 mL (α型) 0.01065 g/100 mL (β型) |
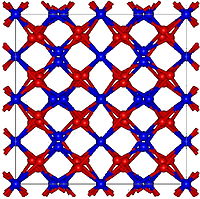
| 结构 | |
| 晶体结构 | 立方晶系, Ia3(308 K以上) 正交晶系, Pcab(308 K以下)[1] |
| 热力学 | |
| ΔfHm⦵298K | −971 kJ·mol−1[2] |
| S⦵298K | 110 J·mol−1·K−1[2] |
| 危险性 | |
| NFPA 704 | |
| 相关物质 | |
| 其他阴离子 | 三氟化锰、三乙酸锰 |
| 其他阳离子 | 三氧化二铬、三氧化二铁 |
| 相关化学品 | 一氧化锰、四氧化三锰、 二氧化锰、七氧化二锰 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
三氧化二锰是一种无机化合物,化学式为Mn2O3,其中锰处于+3氧化态。[3]
制备
[编辑]在800℃以下将二氧化锰于空气中灼烧可以得到α-Mn2O3(更高温度得到Mn3O4)[4],在600-800℃空气中加热Mn2+的硝酸盐、草酸盐或碳酸盐也能得到α-Mn2O3[5]。γ-Mn2O3由氢氧化锰(II)的脱水氧化制得。[4] 很多制备纳米晶体Mn2O3的方法已有报道,如通过氧化Mn2+盐或还原MnO2制备。[6][7][8]
需要注意的是,Mn2O3和MnOOH并不是相同的,MnOOH在空气中加热,会在约300 °C时产生MnO2。[9]
结构及物理性质
[编辑]三氧化二锰和其它过渡金属氧化物不同,并不采取刚玉(Al2O3)的结构[4]。已知它有常见的α型和γ型[10],和在高压下有着CaIrO3结构的晶型。[11]α-Mn2O3是黑色固体,为斜方晶系,晶格常数a=941.2 pm、b=941 pm、c=942.3 pm,奈耳温度约为80K。[5]γ-Mn2O3则是立方密排结构,奈耳温度为39K。[12]
化学性质
[编辑]- Mn2O3 + 6 HCl(稀) —Δ→ 2 MnCl2 + Cl2↑ + 3 H2O
- 2 Mn2O3 + H2SO4(浓) —Δ→ 4 MnSO4 + O2↑ + 4 H2O
三氧化二锰也能氧化有机物,如在硫酸的水溶液中将4-氟甲苯氧化为4-氟苯甲醛,[14]将4,4'-二甲基-2,2'-联吡啶氧化为2,2'-联吡啶-4,4'-二甲醛,[15]以及将4-甲基苯磺酸氧化为4-甲酰基苯磺酸。[16]
三氧化二锰和氧化镧在高温反应,可以得到正交晶系的LaMnO3,这种化合物与GdFeO3异构。[17]它也能直接和六氟乙酰丙酮在环己烷中回流下反应,生成三(六氟乙酰丙酮)合锰(III)。[18]
应用
[编辑]三氧化二锰在无机上可以用作一氧化氮选择性还原的催化剂[19],在有机合成中用作氧化剂[14][20],它也能用作钯铂合金的载体[21]或电极材料[22]。
参考文献
[编辑]- ^ Grant, R. W.; Geller, S.; Cape, J. A.; Espinosa, G. P. Magnetic and Crystallographic Transitions in theα−Mn2O3−Fe2O3 System. Physical Review. 1968, 175 (2): 686–695. ISSN 0031-899X. doi:10.1103/PhysRev.175.686.
- ^ 2.0 2.1 Zumdahl, Steven S. Chemical Principles 6th Ed.. Houghton Mifflin Company. 2009: A22. ISBN 0-618-94690-X.
- ^ Catherine E. Housecroft, Alan G. Sharpe. Inorganic Chemistry (Second Edition). Pearson Education Limited, 2005. pp 614-615. Manganese(III). ISBN 0130-39913-2
- ^ 4.0 4.1 4.2 Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ 5.0 5.1 谢高阳 等. 无机化学丛书 第九卷 锰分族 铁系 铂系. 科学出版社, 2012.3. pp 31
- ^ Shuijin Lei, Kaibin Tang, Zhen Fang, Qiangchun Liu, Huagui Zheng. Preparation of α-Mn2O3 and MnO from thermal decomposition of MnCO3 and control of morphology. Materials Letters. 2006, 60: 53. doi:10.1016/j.matlet.2005.07.0.
- ^ Yuan, Zhong-Yong; Ren, Tie-Zhen; Du, Gaohui; Su, Bao-Lian. A facile preparation of single-crystalline α-Mn2O3 nanorods by ammonia-hydrothermal treatment of MnO2. Chemical Physics Letters. 2004, 389 (1-3): 83–86. ISSN 0009-2614. doi:10.1016/j.cplett.2004.03.064.
- ^ Chandra, Navin; Bhasin, Sanjeev; Sharma, Meenakshi; Pal, Deepti. A room temperature process for making Mn2O3 nano-particles and γ-MnOOH nano-rods. Materials Letters. 2007, 61 (17): 3728–3732. ISSN 0167-577X. doi:10.1016/j.matlet.2006.12.024.
- ^ Kohler, Thomas; Armbruster, Thomas; Libowitzky, Eugen. Hydrogen Bonding and Jahn–Teller Distortion in Groutite,α-MnOOH, and Manganite,γ-MnOOH, and Their Relations to the Manganese Dioxides Ramsdellite and Pyrolusite. Journal of Solid State Chemistry. 1997, 133 (2): 486–500. ISSN 0022-4596. doi:10.1006/jssc.1997.7516.
- ^ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
- ^ High Pressure Phase transition in Mn2O3 to the CaIrO3-type Phase Santillan, J.; Shim, S. American Geophysical Union, Fall Meeting 2005, abstract #MR23B-0050
- ^ Kim S. H, Choi B. J,Lee G.H., Oh S. J., Kim B., Choi H. C., Park J, Chang Y. Ferrimagnetism in γ-Manganese Sesquioxide (γ−Mn2O3) Nanoparticles. Journal of the Korean Physical Society. 2005, 46 (4): 941.
- ^ 13.0 13.1 曹忠良, 王珍云. 无机化学反应方程式手册. 湖南科学技术出版社, 1985.9. pp.302 【Mn2O3】
- ^ 14.0 14.1 张启蒙, 薛叙明, 马金花, 李玉辉, 马伟刚. 三氧化二锰氧化法合成对氟苯甲醛的绿色工艺 (页面存档备份,存于互联网档案馆). 精细化工中间体, 2010, 40(3):47-49.
- ^ Wang, Yong; Zhang, Lipan; Guo, Liangqi; Wu, Ji; Wang, Fayun; Guo, Yanchun. Process for preparation of [2,2'-bipyridine]-4,4'-dicarboxaldehyde [P]. 2011. CN 102295596 A
- ^ 严新, 宋萌, 林周, 王遵尧. 用Mn2O3氧化法合成对羰基苯磺酸 (页面存档备份,存于互联网档案馆). 江苏化工, 2004, 32(4):31-33.
- ^ van Roosmalen, J.A.M.; van Vlaanderen, P.; Cordfunke, E.H.P.; IJdo, W.L.; IJdo, D.J.W. Phases in the Perovskite-Type LaMnO3+δ Solid Solution and the La2O3-Mn2O3 Phase Diagram. Journal of Solid State Chemistry. 1995, 114 (2): 516–523. ISSN 0022-4596. doi:10.1006/jssc.1995.1078.
- ^ Zhang, Haitao; Li, Bo; Dikarev, Evgeny V. Mn(III) Hexafluoroacetylacetonate as an Oxidative Agent in the Synthesis of Heterobimetallic β-Diketonates. Journal of Cluster Science. 2007, 19 (1): 311–321. ISSN 1040-7278. doi:10.1007/s10876-007-0174-1.
- ^ Tang, Xingfu; Li, Junhua; Sun, Liang; Hao, Jiming. Origination of N2O from NO reduction by NH3 over β-MnO2 and α-Mn2O3. Applied Catalysis B: Environmental. 2010, 99 (1-2): 156–162. ISSN 0926-3373. doi:10.1016/j.apcatb.2010.06.012.
- ^ Sihaib, Z.; Puleo, F.; Garcia-Vargas, J.M.; Retailleau, L.; Descorme, C.; Liotta, L.F.; Valverde, J.L.; Gil, S.; Giroir-Fendler, A. Manganese oxide-based catalysts for toluene oxidation. Applied Catalysis B: Environmental. 2017, 209: 689–700. ISSN 0926-3373. doi:10.1016/j.apcatb.2017.03.042.
- ^ 徐鹏, 吴志星, 邓积光, 刘雨溪, 谢少华, 郭广生, 戴洪兴. 有序介孔三氧化二锰负载PdPt合金:一种高效的甲烷催化燃烧催化剂 (页面存档备份,存于互联网档案馆). 催化学报, 2017, 38(1):92-105.
- ^ 张杰, 许家胜. 一种三氧化二锰多孔微米片/泡沫镍复合电极材料的制备方法[P], CN105355468 A. 2016.
拓展阅读
[编辑]
- Ovsyannikov, Sergey V.; Abakumov, Artem M.; Tsirlin, Alexander A.; Schnelle, Walter; Egoavil, Ricardo; Verbeeck, Jo; Van Tendeloo, Gustaaf; Glazyrin, Konstantin V.; Hanfland, Michael; Dubrovinsky, Leonid. Perovskite-like Mn2O3: A Path to New Manganites. Angewandte Chemie International Edition. 2013, 52 (5): 1494–1498. ISSN 1433-7851. doi:10.1002/anie.201208553.
- Vanderah, T.A.; Lufaso, M.W.; Adler, A.U.; Levin, I.; Nino, J.C.; Provenzano, V.; Schenck, P.K. Subsolidus phase equilibria and properties in the system Bi2O3:Mn2O3±x:Nb2O5. Journal of Solid State Chemistry. 2006, 179 (11): 3467–3477. ISSN 0022-4596. doi:10.1016/j.jssc.2006.07.014.
- Oelerich, W.; Klassen, T.; Bormann, R. Hydrogen Sorption of Nanocrystalline Mg at Reduced Temperatures by Metal-Oxide Catalysts. Advanced Engineering Materials. 2001, 3 (7): 487–490. ISSN 1438-1656. doi:10.1002/1527-2648(200107)3:7<487::AID-ADEM487>3.0.CO;2-0.
| |||||||||||||||||||||||||||||||||||||

