硬水軟化
外觀
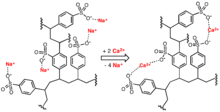
硬水軟化是去除硬水中的鈣、鎂和某些其他金屬陽離子,可以將硬水軟化為軟水。硬水軟化可以提高水使用的安全性。產生的軟水在相同的清潔工作中需要更少的肥皂,因為肥皂不會浪費與鈣離子的結合。軟水還可以減少或消除管道和配件中的水垢積聚,從而延長管道的使用壽命。水軟化通常使用石灰軟化或離子交換樹脂來實現,但越來越多地使用奈米過濾或逆滲透膜來實現。
基本原理
[編輯]水中某些金屬離子(例如鈣和鎂)的存在(主要是碳酸氫鹽、氯化物和硫酸鹽)會導致各種問題。[1]
硬水會導致水垢堆積,從而污染管道並促進電偶腐蝕。[2][3]
在軟水中洗滌時產生的滑溜感是由於水中的礦物質含量被剝奪後,肥皂對水離子的吸引力減弱而引起的。人體皮膚表面帶有輕微的電荷,肥皂容易與這些電荷結合,需要更多的努力和更多的水才能去除。[4]硬水含有鈣或鎂離子,與肥皂反應後會形成不溶性鹽,在浴缸和淋浴表面留下一層不溶性硬脂酸鹽,通常稱為肥皂浮渣。[4][5]
硬水軟化的方法
[編輯]常見硬水軟化主要方法有煮沸、蒸餾、離子交換樹脂法等,工業上也有用藥劑軟化。
煮沸法
[編輯]將水煮沸,可將部分鈣鎂離子轉化為水垢。
石灰蘇打法
[編輯]將氧化鈣CaO(生石灰)和碳酸鈉Na2CO3(蘇打)加到水中,去除Ca2+和Mg2+離子,使它們沉澱
蒸餾法
[編輯]通過加熱的方法使水由液態轉為氣態。最後將水冷卻為液態得到蒸餾水。這是實驗室常用的淨化水的方法。
陽離子交換法
[編輯]通過在水中加入十水合碳酸鈉,將與碳酸根離子化合的碳酸鎂和碳酸鈣固體沉澱出來。
Ca2+(aq)+CO32−(aq) -> CaCO3(s)
Mg2+(aq)+CO32−(aq) -> MgCO3(s)
參見
[編輯]參考文獻
[編輯]- ^ Hard water. Encyclopædia Britannica. 20 July 1998 [4 March 2015]. ISBN 9781593392925.
- ^ Stephen Lower. Hard water and water softening. July 2007 [2007-10-08].
- ^ Rowe, Gary. Well Contamination By Water Softener Regeneration Discharge Water. Journal of Environmental Health. 1988, 50 (5): 272–276. JSTOR 44541189.
- ^ 4.0 4.1 Why can't I rinse the soap off my hands?. USGS. [7 October 2019].
- ^ Soap. [2011-08-16]. (原始內容存檔於2011-08-17).
